Minden egyes sérültről meg kell állapítani az egyéni thrombosis rizikót, amikor a kezelést megkezdjük. A rizikók csökkentésére kell törekedni. Ehhez a mechanikus és a gyógyszeres prophylaxis minden lehetséges módszerét és kombinációját igénybe kell venni az előnyök és a mellékhatások gondos mérlegelése után. A fractionált heparinok jól beváltak a traumatológiai beteganyagon, könnyű kezelésük, kevés szövődményük és főleg magas hatékonyságuk révén első helyen ajánlhatók a gyógyszeres prophylaxisra. Fontos új szempont a posthospitalis prophylaxis, valamint az ambulanter kezelt sérültek prophylaxisa, amelyek általánossá tétele egyik legfontosabb feladatunk. Tisztában kell lenni azzal, hogy hatásos thrombosisprophylaxis ellenére is létrejöhet thrombosis. A maradék rizikóról ugyanúgy, mint magának a prophylaxisnak a céljairól a beteget tájékoztatni kell.
Érbetegségek: 2001/3. 73. oldal
KULCSSZAVAK
Thrombosis prophylaxis, trauma és thrombosis, fractionált heparin és trauma, prophylaxis traumában
A vénás trombózisok és szövődményeik nincsenek kellő súlyuk szerint a köztudatban, nagyfokú elterjedésük az egészségügyi kultúra fokmérőjeként is tekinthető. Amíg 1970-ben Magyarország 10,8/100 000-es mortalitással a fejlett országokhoz viszonyítottan még a közepesen érintett országok közé tartozott, addig 1990-re a mortalitás a kétszeresére nőtt, 19,8/100 000 lett. Összehasonlítva a fejlett országokban ugyanezen 20 év alatt jelentősen csökkent a mortalitás (például Ausztriában 80°10-kel, Finnországban 70%kal stb.). A nem megnyugtató hazai helyzet hátterében döntően a korszerű trombózis prophylaxis elterjedésének hiánya áll (8). Átlagos, normál populációban évente 160/100 000 mélyvénás trombózis (MVT), 20/100 000 szimptómás, nem halálos tüdőembólia (PE), 50/100 000 halálos, boncolással igazolt PE fordul elő (8). A lábszárfekély betegség 300/100 000 lakost érint. Pető és Sas szerint hazánkban évi 6000 vénás elégtelenség miatt munkaképtelenné váló és elnyomorodó beteg van (11).
Nagyszámú az a betegcsoport, aki megelőző vénás keringési problémák nélkül egyszer csak posttrombotikus szindrómatüneteivel jelentkezik. Ez a diagnosztizált MVT esetek 85%-ban 3-4 év múlva manifesztálódik. Átlagban 7,5 évvel korábban válnak nyugdíjassá ezek a betegek, és évi 2 hónapot töltenek átlagosan betegen. A thromboemboliás betegségek kezelési költsége az összes betegségre fordított költségvetés 0,3%-a Svédországban (ez egymagában 95 millió dollárt jelent). 1976-ban Magyarországon a lakosság 2 ezrelékének volt lábszárfekélye és a postthrombotikus syndroma miatti táppénzkiadások akkor évi 400 millió Ft-ot tettek ki (11). Azóta a lábszárfekély incidencia megnégyszereződött, a betegek több mint harmadát leszázalékolták {2).
Magyarországon a trombózisok számának emelkedését az okozza, hogy nem eléggé elterjedten, nem eléggé korszerű módszerekkel végezzük és főleg túl korán abbahagyjuk a trombózis prophylaxist!
Szakmánk magas rizikót jelent, mert úgy az operatív, mint a konzervatív kezelés, és különösen az alsó végtagi traumák a legerősebb kiváltó faktoroknak számítanak. Ha a kiváltó faktorokat összevetjük, akkor első helyen az alsó végtagi gipszkezelés áll (36-szoros), a második helyen a mozgásszervi műtét (16-szoros), negyedik helyen pedig az immobilizáció áll (7-szeres) rizikó fokozódással. A traumatológiai beteganyagban a legmagasabb trombózis előfordulást a gerincsérülteknél (68%) és az alsóvégtagi sérülteknél (66%) találtak. Az alsó végtagi sérültek közül magas trombózis rizikót jelentenek az Achilles-ín sérültek (33%), a bokatörések (14,8%). Jelentős különbség van az MVT előfordulásában azok között, akiket végig ambulánsan lehetett kezelni (2%) és azok között, akik először kórházi felvételt igényeltek és gipszrögzítésben távoztak (12%), feltehetően a trauma súlyosságával összefüggésben. (I. táblázat.)

I. táblázat.
A trombózis előfordulási gyakorisága prophylaxis nélküli alsó végtagi gipszrögzítéskor.
Fontos tudni, hogy nem csak a sérült oldal van veszélyben. Csípőtáji törötteknél prophylaxis nélkül 40%-ban fordul elő trombózis a törés oldalán és 23%-ban az ép oldalon! A trombózis létrejöttéhez diszpozíciós (intrinsic, vagy hajlam) és expozíciós (triggering, kiváltó) faktorok jelenléte kell. A kettő szinergista módon erősíti egymást, és ha átlépik az ún. manifesztációs küszöböt, a trombózis megjelenik. Ebbő1 következik, hogy egy adott traumatológiai beteg/sérült esetén individuális kockázattal kell számolnunk, amely a sérülés jellege, localisatioja és másrészről a betegfüggő rizikófaktorok által meghatározott. A II. táblázat mutatja az irodalom szerint leggyakoribb hajlamosító faktorokat, amelyek lehetnek veleszületettek és szerzettek, valamint a kiváltófaktorokat a képviselt rizikó erőssége szerint.

II. táblázat.
A hajlamosító és a kiváltó faktorok.
Patológia
A trombózis keletkezésének mechanizmusát az ún. Virchow triásszal a legegyszerűbb magyarázni. A coagulatio fokozódása, a stasis és az érfalkárosodás mind jelen vannak a sérülést követően. Patológiailag meg kell különböztetni distalis (lábszári) vénás trombózist (DVT) és proximlis (femoralis) vénás trombózist (PVT). A pulmonalis embolizáció az utóbbival mutat szorosabb összefüggést. Megkülönböztetünk felszínes és mélyvénás trombózist.
A trombózis kezdete elektív műtéteknél perioperatív, azonban sérült anyagon adott annak lehetősége, hogy a trombózis a sérüléskor, vagyis praehospitalisan jöjjön létre. Klinikailag a trombózis az esetek többségében a sérülést követő első héten jelentkezik. A kezelés 7-10 napja között már csak az összes eset 1/5-e manifesztálódik. Az utóbbi évek fontos felismerése, hogy az MVT és a PE sokkal gyakoribb kórházból való távozás után, mint azt korábban hittük. A PE-k fele a sérülést követő első két hétben jelentkezik, de előfordult PE még 4 hónappal a trauma után is (5). A kórházból való távozás utáni 4-6, nap a legveszélyeztetettebb. Ebből következik, hogy egyrészt a trombózis profilaxissal az MVT kezdetét csak kitoltuk, másrészt a kórházi távozás után a heparin-prophylaxis leállítása (vagy a heparin-Colfarit-váltás) súlyos következménnyel jár.
Az alsó végtagi immobilizáció során a thromboemboliás szövődmény rizikója a 3-4. hét végéig fokozott, míg ezt követően a rizikó csökken.
Az MVT rendszerint a lábszárvénákban kezdődik, többnyire a trauma magasságában, a soleus izom sinusaiban, illetve a gastrocnemius izom nagy vénáiban. Kezelés nélkül 20-30%-ban propagál proximálisan, egy része ennek végül tüdőembóliába torkollhat. Ez alól éppen a csípőtáji sérültek, illetve a csípőtáji elektív műtöttek kivételek. Itt ugyanis az esetek közel 40%-ában primeren a proximális femoralis vénaszakaszban van a thrombus, a distalis vénaszakaszok érintettsége nélkül. Boncoláskor a legtöbb trombózis a mindkét oldali lábszár-vénákban került felfedezésre, amely azt támasztja alá, hogy a statist kell a legerősebb kiváltó oknak tekintenünk. Ugyanakkor az is kiderül ebből, hogy éppen a vádli vénáinak trombózisa a leggyakrabban tünetmentes.
Egy friss MVT kimenetelének öt lehetséges útja van; 1. spontán fibrinolysis, 2, thrombusnövekedés, 3. embolisatio, 4. postthrombotikus syndroma, 5. thrombosis recidíva.
Klinikum
A klinikai jelek nem megbízhatóak. Az MVT-ok csupán 30%-a okoz tüneteket (minden boncolás során felfedezett 3 MVT közül csak 1 okozott klinikai tüneteket). A rettegett szövődmény, a tüdőembólia is csupán 20%-ban okoz tüneteket és ebből is csupán 2-4%-a halálos végű. Jelentős számú embólia húzódik meg a műtét utáni tüdőgyulladások mögött, melyek valójában infarktpneumóniák.
Bár a tüneteket döntően meghatározza a vénás stop szintje és kiterjedése, három jel kötelezően megjelenik. Ezek az oedemás duzzanat, a cyanosis és a fájdalom. Korai tünet a nehézségérzés, görcskészség (különösen a lábikrában), a talpfájdalom és a húzó fájdalom a vénák mentén. A Homans-jel, a vádli összenyomási - Lowenberg-jel és a talp nyomás-érzékenysége - Payer-jel nem specifikusak, értékük kétes.
Differenciál diagnózisában minden olyan kórkép szóba jön, ahol fájdalmas, duzzadt lábat látunk. Ezek hátterében musculoskeletális betegség, vénás-, vagy nyirok elvezetési zavar, továbbá popliteális cysta lehet.
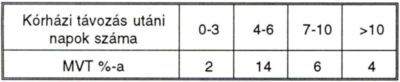
III. táblázat.
A mélyvénás thrombosis előfordulási gyakorisága a kórházból való távozás óta eltelt idő függvényében.
Diagnosztika
A műszeres diagnosztika lehet noninvazív. Ilyen a Doppler, amely a lábszáron csak 20-30%-os találati arányt biztosít. A color duplex sonographia eléri a 95%-os megbízhatóságot, de a lábszárvénák distalis szintjén szintén elégtelen. További eljárás az impedancia plethysmographia.
Az invazív diagnosztikához a jódszcintigráfia és a ma is standardnak tartott phlebographia tartozik. Utóbbi továbbra is őrzi alapvető helyét a diagnosztikában.
Jelenleg az ultrahang-vizsgálat a választandó első diagnosztikai kísérlet, a phlebographia problémás, kétséges esetben következik.
Profilaxis
A profilaxis célja az MVT kialakulásának és következményeinek (PE, postthrombosisos syndroma) megelőzése. (IV. táblázat.)
A traumatológiai sérültek trombózis szempontjából feltétlen nagyrizikójú betegeknek minősülnek, és megelőző kezelésben kell részesülniük. Primer trombózis profilaxis alatt azokat a törekvéseinket értjük, amelyek a trombózis létrejöttét akadályozzák (szemben a secunder profilaxissal, ahol a már létrejött trombózis további növekedését és esetleges embolisatióját igyekszünk megelőzni).
A prehospitalis profilaxiskor a sérülés pillanatától, a baleset helyszínén indul a profilaxis. Ez számos diagnosztikai nehézséget rejt, egyben iatrogén károsítás veszélyét hordozza magában. Ugyanakor monotraumás végtag sérülteken (pl. csípőtáji törések, lábszártörések) volna indikációja annak, hogy az első észlelő orvos megkezdje a profilaxist.
Az intrahospitalis profilaxis egyértelműen elfogadott és évtizedek óta gyakorlat a traumatológiai osztályokon. A már említett monotraumás alsóvégtagi sérülteken, amennyiben kontraindikáció nincs, akkor szintén bevált gyakorlat a preoperatív profilaxis.
A posthospitalis profilaxis ma a trombózis megelőzés legtöbbet hangsúlyozott, új és rendkívül lényeges területe. Fontosságát jól mutatja a trombózis előfordulás gyakoriságának alakulása a kórházi távozást követően (III. táblázat). Megfelelő profilaxishoz az egyéni trombózisrizikó meghatározása elengedhetetlen. A mindennapos gyakorlatban minél egyszerűbb megoldás szükséges. A több létező séma közül javasolható az István professzor és mtsai által módosított kérdőív (V. táblázat).

IV. táblázat.
A distalis, a proximalis vénás trombózisok és a pulmonalis emboliák gyakorisága a rizikó mértékének függvényében.

V. táblázat.
Kérdőív az egyéni thrombosis rizikó felmérésére. (István és munkatársai.)
A profilaxis módjai lehetnek mechanikusak: például rugalmas pólya műtét előtt, alatt és után. A sérült végtag megemelésével a stasist jelentősen csökkenthetjük. A passzív mozgatás (pl. elektromos sínen), vagy a ciklikus (intermittáló) pneumatikus kompressio és az ún, antithrombosis harisnyák előnyös hatása bizonyított, de sajnos a konzervatívan kezelteknél alig alkalmazható. Fekvőgipsz-rögzítésekhez fejlesztettek ki egy újabb pneumatikus kompressziós pumpát, az ún. AV-impulse rendszert, amelyet a gipszrögzítés alatt a lábra kell erősíteni. Ez a plantaris vénás plexusra hatva fokozza a vénás visszaáramlást az immobilizált alsóvégtagban (Bulitta és mtsai. 1996). A profilaxis a kezelést magát is jelentősen befolyásolhatja, amennyiben olyan módszerrel rögzítjük a törést, hogy korai mobilizációt, esetleg korai funkcionális kezelést tegyen lehetővé. Ilyen szempontból különösen nagy jelentőségű, ha mód nyílik korai izomtorna, keringés javító gyakorlatok elvégzésére. Elektív esetben természetesen lehetőség van a vénás zavarok megelőző sebészi kezelésére (varicectomia). A legelterjedtebb módszer a gyógyszeres profilaxis. Ezen belül a dextran-, a heparin- és a kumarin-félék nyertek tért. A thrombocyta aggregatiot gátló szerek (Aspirin, Colfarit, Ticlid) a mélyvénás trombózisok megelőzésére nem alkalmasak (Nemes 1999).
Dextran
A Dextran, amely glucose polymer, 40 000, valamint 70 000 átlag molekulasúlyú változatban létezik. Prophylacticumként csak kisfokban hatékony. A magasabb molekulasúlyú változattal gyakoribbak az allergiás reakciók. Az .egyéb mellékhatások között a keringés túlterhelését, a keringési elégtelenséget említik. Ebből fakadóan kontraindikált használata cardialis decompensatioban, tüdőoedemában és krónikus veseelégtelenségben. Vérzésveszély nincs, de a magasabb költségek és az intravénás adagolás okozta nehezebb kezelhetőség miatt nem ideális prophylacticum.
Heparin
A kis dózisú heparin (2-3x 5000 NE) csak kis fokban hatásos. Az illesztett dózisú heparin emeli a hatékonyságot, de így megnőnek a költségek is. A kismolekulasúlyú (frakcionált, LMWH) heparinok mai ismereteink szerint a leghatékonyabbak, traumatológiai betegeken hatásosabbak, mint a nem frakcionált heparin mind az MVT, mind a PE megelőzésében (Nurmohamed és mtsai.1992). Így a traumatológióban hatékonyságuk, egyszerűségük, biztonságosságuk és a kényelmes, egyszeri adagolás biztosította előnyök alapján a frakcionált, vagy kismolekulasúlyú heparin adása a javasolt. Localis suffusio, haematoma, illetve postoperatív vérzés ritkább, mint más heparin-fajták után. Laboratóriumi kontroll szükségessége minimális. Tartós alkalmazáskor csak nagyon ritkán okoz thrombocytopeniát.

VI. táblázat.
A hazánkban forgalomban lévő frakcionált (LMWH) heparinok.
A Magyar Konszenzus Nyilatkozat szerint a frakcionált heparint is testsúly kg-ra illesztve kell adagolni, legalább 6 hétig. Gipszrögzítéskor a prophylaxist a gipszeltávolítás utáni hetedik napig kell végezni. (VI. táblázat.)
Az LMWH 30%-os MVT-rizikó csökkenést okoz a nem frakcionált heparinhoz viszonyítva, sőt PVT vonatkozásában ez a redukció 58%-os.
A heparin mellékhatása a vérzés, a postoperatív haematomák veszélye, illetve konzervatív kezelésnél a törési haematomák növekedése. A valóságban ez a veszély igen csekély, a frakcionált heparinok esetében a vérzésveszély nem nagyobb a nemfrakcionált heparinéhoz képest. (Mindezzel szemben a Syncumar kezelt betegeken ismert a törési haematomák jelentős fokozódása, amely akár műtéti feltárást igényelhet. Éppen ezért Syncumar kezelés alatt álló - elsősorban csípő, medence törött sérülteknél - a kezelés felfüggesztése és valamelyik heparinfajtára való átállítása szükséges).
A heparin thrombocytopeniát okozhat, ezért kezelés alatt a thrombocyta-számot ellenőrizni kell. Amennyiben ez a szám 50%-os csökkenést mutat, a kezelést fel kell függeszteni. Meg lehet kísérelni a frakcionált heparinra való átállást, de ha a frakcionált heparin mellett következett be a thrombocytopenia, akkor hirudinra szükséges áttérni.
A heparin, vagy LMWH prophylaxis kontraindikált intracraniális, intraspinális vérzés, aktív gastrointestinális fekély, véres széklet, nem rendezett coagulopathia esetén. Heparin indukálta thrombocytopeniában a heparin-adagolás azonnali felfüggesztése szükséges. Erősen mérlegelendő a heparin adagolása súlyos anaemia, thrombocytopenia és intracraniális tumor esetén. Relatív kontrainidicatio a rosszul beállított hypertonia (tartósan 180/115 Hgmm feletti értékeknél), a haemorrhagiás hajlam, az anamnesisben szereplő fekélybetegség, alkoholos anamnesis és a retinopathia.
Hirudin
A hirudin, amely a pióca nyálából nyerhető anticoagulans, ma már rekombináns DNS technikával is termelhető igen hatékony trombózis-gátló.
Kifejlesztés alatt állnak a rekombináns humán Xa-faktor, valamint a 7E3, amely egy egér monoclonális antigén, szintén trombózis-gátló hatású.
Cumarin
Hazánkban a cumarin-típusú orális anticoagulansok közül a Syncumar tejredt el. Leggyakrabban valamelyik heparinfajtával megkezdett prophylaxisról térünk át az orális kezelésre. Előnye éppen az orális kezelésből adódik, hátránya a frakcionált heparinhoz képest gyakoribb vérzésveszély, illetve a gyakoribb laboratóriumi kontroll igény. Amennyiben a konzervatív kezelésről mégis operatív kezelésre- szükséges áttérni, akkor leállítása és a heparinra való visszaállítás további időveszteséget jelent a törés kezelésében. Az orális anticoaguláns kezelés költséghatékonyságáról folytatott vita még nem zárult le az irodalomban.
A trombózis profilaxis indikációja
A fentiekből kiderült, hogy az immobilizáció az egyik legerősebb trombózis kiváltó faktor. A traumatológiában mind a konzervatív kezelés során, mind a postoperátív nyugalomba helyezés végett rendszeresen alkalmazunk gipszrögzítést. Az alsóvégtag traumája és immobilizációja a trombózis profilaxis egyik fő indikációja. Schreiber egyenesen úgy fogalmaz, hogy a fenti esetekben a profilaxis elhagyása már műhiba. Számos adat igazolja az MVT és a PE gyakoriságát a kórházból való távozás után, a PE-k egyharmada otthon következik be.
Németországban egy kérdőíves felmérés azt mutatta, hogy mind a kórházból távozottak, mind az eleve ambulánsan kezeltek körében - alsóvégtagi gipszrögzítés bármely formája esetén - rendszeresen történik prevenció, függetlenül attól, hogy járógipsz-e a rögzítés (Schmidt és Hackenbroch 1995). Hangsúlyozom, hogy ez ellentétes az általános magyar gyakorlattal, ahol a terhelés engedélyezése egyet jelent a prevenció felfüggesztésével. A német gyakorlat jelentős statisztikai eredményt mutat (a klinikailag észlelt thromboemboliás szövődmények száma 4,5%-ról 0%-ra, illetve az ultrahanggal észlelt MVT 17,1 %-ról 6,1 %-ra csökkenését).
A halálos PE rizikója 1/4-1/3-ára csökkent a gipszrögzítéssel ellátott ambuláns betegeken, amennyiben LMWH profilaxisban részesültek. A vélemények egyedül ott oszlottak meg, ahol gipszrögzítés nélkül ugyan, de csak részterhelést és mankózást engedtek. Itt az esetetek egy negyedében történt prevenció és egyedi mérlegelés javasolható.
Külbokaszalag sérültek konzervatív kezelése esetén, amennyiben 40 évnél fiatalabbak és egyéb rizikó tényezővel nem bírnak, a rizikó csak minimálisan emelkedett (1,2-szeres), így a prevenció egyéni mérlegelés tárgya. A prevenciót az alsóvégtagi gipsz eltávolítását egy héttel követően kell megszüntetni. Részterhelés melletti profilaxist a teljes terhelés elérése után lehet abbahagyni.
Tanulságul megemlítem, hogy megjelentek már Németországban a prevenció elmulasztása miatti kártérítési perek.
Összegezve
- Minden egyes betegről meg kell állapítani az egyéni trombózis-rizikót, amikor a konzervatív kezelést megkezd jük.
- A rizikók csökestésére kell törekedni. Ehhez a mechanikus és a gyógyszeres profilaxis minden lehetséges módszerét és kombinációját igénybe kell venni az előnyök és a mellékhatások gondos mérlegelése után.
- Tisztában kell lenni azzal, hogy hatásos trombózisprofilaxis ellenére is trombózis létrejöhet. A maradék rizikóról ugyanúgy, mint maga a profilaxis céljairól a beteget tájékoztatni kell.
Irodalom
- Andreas, M., Debong, B.: Thromboseprophylaxe bei Gehgips. Urteil des Bundegeriehtshofs. Chirurg BDC. 36:2.53-54, 1997.
- Blaskó Gy., Pál A., Erős L.: Anticoaguláns kezelés Magyaror szágon, Egészségpiac 1999.
- Browner, B. D., Jupiter; J. B., Levinie, A. M. , Trafton, P. G.: Skeletal trauma. Saunders Co. Philadelphia 1992.
- Bulizta, C., Kock, H. J., Hanke, J., et al.: Förderung des venösen Rückstroms im Liegegipsverband durch das AV-Impulssystem. Unfallchirurgie. 22: 145-152. 1996.
- Haas, S.: Thrombosis a baleseti és ortopéd sebészetben. Unfall chirurg 100:307-319. 1997.
- Kock, H. J., Schmith-Neuerburg, K. P.: Thromboseprophylaxie bei ambulanten Padesten mit Gipsimmobilisation. Thrombose Schriftenreihe. Springer. Berlin. 1998.
- Magyar Thrombosis és Haemosta.sis Társaság: A thromboembo liák megelőzése és kezelése. (Magyar Konszenzus Nyilatkozat) Budapest. 1998.
- Molnár L., Sándor T., Monos E., Acsády Gy.: A vénás betegsé gek mortalitásának feltűnő növekedése Magyarországon. Orvosi Hetilap 138.43: 2727-2732. 1997.
- Nemes A.: Mélyvénás thrombosis. Kórház VI. l. 29-32. 1999.
- Nurmochamed, M. T., Rosendaal, F. R., Büller, H. R., and al.: Low-molecular-wieght heparin versus standard heparin in ge neral and orthopaedic surgery: a meta-analysis. Lancet. 340: 152-156. 1992.
- Pető L, Paksi A., Kovács A., Sas G.: Mélyvénás trombózis nép egész.~égügyi vonatkozásai. Népegészségügy. 61: 159-160. 1980.
- Rák K : Heparin terápia: 1998 (A nyolcvanéves heparin mai al kalmazása). Orvosi Hetilap. 140 (2) 59-66. 1999.
- Schmidt, J., Hackenbroch, M. H.: Prevention of deep venous thrombosis in ambulatory or discharged orthopaedic patients. Arch. Orthop. Trauma Surg. 114: 226-228. 1995.
- Weinmann, E. E., Salzman, E. W.: Deep-vein thrombosis. New England J. Medicine. 331: 1630-1b40. 1994.
- Zagrodnick, J., Kaufner, H. K.: Ambulante Thromboembolie prophylaxe in der Traumatologie durch Selbstinjektion von Heparin. Unfallchirurg. 93: 331-333.
Dr. Detre Zoltán
Országos Traumatológiai Intézet
1081 Budapest, Fiumei út 17.
Érbetegségek: 2000/3. 83-90. oldal


