Bevezetés. A krónikus vénás betegségek (KVB) hőablációjának egyes problémái indokolják a technológia változtatását, melynek során kisebb hőmennyiség alkalmazását és kedvezőbb energia közlési algoritmus bevezetését tartjuk indokoltnak. Véleményünk szerint az endovénás hegesztés (EVH) optimálisabb, mint az eddigi eljárások, melynek során a paraméterek automatikus generálásával, a nagyfrekvenciás modulált áram hatása alatt, a véna fal denaturálásával végeztük az ablációt.
Célkitűzés. a krónikus vénás betegségben szenvedők kezelésében az endovénás hegesztés alkalmazása, és eredményeinek tanulmányozása.
Beteganyag. Az EVH-t 26 beteg 40 műtétje során alkalmaztuk, akik CEAP C3 ? C5- stádiumban voltak (9 férfi és 17 nő, 30 és 65 év közöttiek). A beavatkozást a v. saphena magnán (VSM) 34, a v. saphena parván (VSP) 6 esetben végeztük, A VSM és VSP junkcionális szakaszainak átmérője 12,8 és 24,3 mm, illetve 6,2 és 9,4 mm közötti volt. Az eredményeket 1, 3 és 6 hónap után értékeltük: posztoperatív fájdalom, ultrahang (UH) adatok és szövődmények jelenléte vagy hiánya vonatkozásában.
Módszerek. Az EVH készülék egy EK 300M (Svarmed, Ukrajna) generátorból és egy hegesztőeszközből áll, amelynek munkarésze egy legfeljebb 3 mm átmérőjű és legfeljebb 5 cm hosszúságú bipoláris kialakítású elektróda volt. A hegesztési periódus 10 és 100 V közötti árammal, 50-500 kHz frekvenciájú, 0,1-től 250 kHz-ig modulált váltakozó árammal történt, a mért szövet - ellenállás 0,1-től 1000 Ohm-os volt. A hegesztés időtartamát a relatív rezisztencia együtthatója határozta meg a következő képletnek megfelelően: k = Ri(ti)/R0(t0), ahol Ri(ti) az áramlásellenállás, R0(t0) a kezdeti ellenállás. A k bizonyos értékének elérésekor a készülék befejezi a hegesztést.
Az EVH hatását a VSM 16 különböző szegmensében végzett, 4,5?23 mm átmérőjű vénák elővizsgálata során tanulmányoztuk. Az elektromos és hőmérsékleti adatok dinamikáját Matcad software alkalmazásával értékeltük. Haematoxin-eozin, Van Gieson és elastica szövettani festést alkalmaztunk.
A hegesztést, vagyis a véna szúrását, az eszköz bevezetését és pozicionálását, valamint a tumescent érzéstelenítést az általánosan elfogadott módszereknek megfelelően UH irányítás alatt végeztünk. A VSM beömlésében a hegesztő eszköz munkarészének disztális pólusa a v. epigasztrica szintjében helyezkedett el, míg a VSP beömlésében ez a mélyvénától 1 cm-re volt. Az ablációt 5 cm-es szakaszonként ismételtük.
Eredmények. Az elővizsgálatok során az egyes véna - szakaszokat 5-12 másodpercig 55-80 °C-ra melegítettük. A beavatkozás során függetlenül a vénák átmérőjétől és a lumenben lévő maradék vér mennyiségétől a véna fal denaturálódott. Paravasalis zsírszövet károsodást nem figyeltünk meg, még az ismételt hegesztéssel össze - függésben sem.
A patomorfológiai vizsgálatok megállapították: a véna fal elsősorban az intima és media rétegekben változik meg. Az endothel koagulálódik és elpusztul, a kollagén és a simaizomrostok homogenizálódnak, az adventicia leválik.
A hegesztés során, az abláció ultrahang jeleinek kialakulását megfigyeltük. Nem volt posztoperatív fájdalom 17 esetben (65,4%), közepes fokú fájdalom 9 (34.6%) betegnél volt. Egy hónap után a kezelt vénszegmensek minden betegnél elzáródtak; 7 betegnél (26,9%) már a fibrózis jelei is látszottak; 3 hónap után 12 esetben (46,2%) a vénaszegmensek egyértelmű fibrózisát észleltük; 6 hónap elteltével 26 esetben (100%) az UH ?termikus crossectomiát? mutatott. Minden betegnek kielégítő kozmetikai eredménye volt; szövődmény nem lépett fel.
Megbeszélés. Az EVH módszer az esetek 100% - ában mutatta a limitált ablációt, beleértve a nagy véna - átmérőjű eseteket is. Kimutattuk, hogy más termikus ablációs módszerekkel ellentétben az EVH minimális szöveti hőkárosodással fenyeget, elkerüli az égési sérüléseket és a paresztéziákat. A korlátozott számú beteg és rövid megfigyelési idő azonban indokolja a további vizsgálatokat.
Következtetések. 1. Az EVH lehetővé teszi a vénák szabályozott elektrotermikus ablációjának elvégzését a véna fal összetevőinek denaturálása révén.
2. Az EVH klinikai alkalmazásának első eredményei biztatóak: a VSM és a VSP fibrózisa a 6 hónapos megfigyelési időszak alatt bekövetkezett, valamint a betegek 100% - ánál kielégítő volt a kozmetikai eredmény is.
3. A hegesztési periódus automatikus vezérlési módja, a vénák és a paravasalis szövetek viszonylag alacsony hevítését eredményezi, kiküszöböli a szubjektív tényezők hatását, és ez a vezérlés lehetővé teszi az EVH használatát nagy átmérőjű vénák esetén is.
Érbetegségek: 2020/1. - 13-22. oldal
KULCSSZAVAK
krónikus vénás betegségek (KVB), endovénás thermalis abláció, élőszövet hegesztés, endovénás hegesztés (EVH).
Bevezetés
Az endovaszkuláris lézeres (EVLA) és rádiófrekvenciás abláció (RFA) használata a magas hőmérsékleti expozíció, az égési kockázat, a trombotikus és neurológiai szövődmények, valamint a problematikus módszertani és gazdasági vonatkozások miatt okoz problémát a krónikus vénás betegségek (KVB) kezelésében. Ez indokolja további kutatások végzését az energiaparaméterek jobb kiválasztása (12, 13), a szövetek kíméletesebb melegítése és kifinomultabb irányítási algoritmusa irányába. Úgy véljük, hogy a javasolt módszer az endovenás hegesztés (EVH) a leginkább megfelel ezeknek a kritériumoknak.
A KVB electrotermikus kezelését elsőként K. Firt, L. Heigal és D. Jrivora 1959-ben javasolta. A módszert endovénás elektrokoagulációnak nevezték, ez olyan monopolaláris katéter használatát jelentette, amely elektromos áram hatására felmelegedett, és a véna fal koagulációját okozta (7). A módszert azonban számos komplikáció miatt, széles körben nem fogadták el. A bipoláris katéterek és a továbbfejlesztett nagyfrekvenciás áram - generátorok használata később csökkentette a szövődmények előfordulását. Az elektrotermikus hatások szabályozása azonban továbbra is teljes mértékben szubjektív tényezőktől függött, az eredmények égési sérülések és súlyos hegesedések, amelyek az elektroko - aguláció jellegzetes és gyakori szövőd - ményei voltak (7).
Az EVH módszere, amelyet mi javaslunk, szintén endovénás elektrotermikus hatást alkalmaz. E módszer és az elektrokoaguláció közötti lényeges különbség az, hogy a vénák megszüntetését itt az élőszövet-hegesztési technológia alkalmazásával hajtjuk végre.
Az élőszövet-hegesztési technológia a modulált nagyfrekvenciás elektromos áram hatásának mérésére alapul, amelynek paraméterei automatikusan generálódnak a szövet specifikus ellenállásától függően (6). Az élő szövetek hegesztett varratának kialakulása a fehérjemolekulák elektrotermikus denaturálásán alapul. A hegesztés területén a sejtmembránok egy amorf fehérje képződésével pusztulnak el; amely lehűlés után egy közös denaturált fehérje réteggel szorosan és hermetikusan összeköti a biológiai anyagokat (5,6).
A szövethegesztés problémája a KVB kezelése során az endovaszkuláris felhasználási technológia testreszabásához kapcsolódott. Az elektródák, amelyek egymáshoz szorítják és rögzítik a hegesztett szövetet, azok bipoláris elrendezése a sebészeti hegesztő műszerek jellemzője. Ez áram csatornát alkot az elektromosság szöveteken történő átvezetéséhez és a szövetek kompressziójához, ami a hegesztés egyik alapelve (5). Nyilván ilyen feltételek megteremtése a vénák lumenében technikailag nem kivitelezhető. Ezért az hegesztés klasszikus módja nem volt alkalmas a vénák elzárására, ezért új konstruktív meg - közelítés vált szükségessé.
A probléma megoldása az EVH módszer volt, amelyet 2015?2017-ben fejlesztettek ki a P.L. Shupyk-ról elnevezett, a Nemzeti Orvostudományi Akadémia sebészeti és érsebészeti osztályán végzett kutatás során (4,8). A hegesztőeszköz ezt követő finomítása és egy adaptált vezérlési algoritmus kifejlesztése létrehozta az EVH-módszer automatikus üzemmódban történő alkalmazásának lehetőségét (1,3).
Célok
Meghatározni azokat az eseteket, amikor a KVB-ben szenvedő betegek kezelésében az endovenás hegesztés alkalmazható, és az így elért eredmények tanulmányozása.
Beteganyag
Az EVH módszer alkalmazását két klinikán elvégzett betegvizsgálatok során tanulmányoztuk ? a Kijevi Városi Klinikai Kórház 8-as számú kórházának minimál invazív műtéti és flebológiai osztályán és az Ogyesszai Nemzeti Orvostudományi Egyetemi Klinikán. A vizsgálatban 47 beteg 62 műtétje vett részt.
A 6 hónapos megfigyelési időszak alatt 26 CEAP C3 ? C5 osztályba tartozó beteg 40 műtétjének eredményeit értékeltük: 30 és 65 év közötti életkorú 9 férfi és 17 nő. A VSM EVH-ét 34 esetben, míg vena saphena parva (VSP) kezelést? 6 esetben végeztünk el. Két végtagon együlésben 14 betegnél történtek műtétek. A VSM junkcionális szegmentumának átmérője 12,8 és 24,3 mm közötti volt, vsp ? 6,2 és 9,4 mm közötti. A kezelt VSM-szegmensek hossza 22,5 és 40,6 cm közötti, vsp ? 8,7 és 31,4 cm között.
A posztoperatív időszakban a szövődményeket és a posztoperatív fájdalom intenzitását szubjektív értékelés szerint, egy 10 pontos vizuál analóg skála szerint határoztuk meg. Az EVH eredményeit ultrahanggal (elzáródás, fibrózis, kinyílás és reflux) mind a műtét során, mind a 2, 7, 14 napon és az 1, 3 és 6 hónap után értékeltük.
Anyagok és módszerek
A klinikai használat előtt az EVH hatásmechanizmusát és tulajdonságait alapvizsgálatok során tanulmányoztuk, melynek során a hegesztés elektromos paramétereinek dinamikáját és a véna fal valamint a paravasalis zsírszövet hőmérsékletét regisztráltuk. A vizsgálati anyag 14 beteg (6 férfi, 8 nő 38 és 66 év közötti) 16 vena saphena magna (VSM) szegmense volt, amelyet a műtét során, a környező zsírral együtt távolítottunk el, ezek 10-40 cm hosszúságúak, átmérőjük 4,5-23 mm volt.
A bioszimulációs modell létrehozásához a VSM szegmenseket vérrel töltöttük fel, sós közegbe helyeztük, és termosztátban melegítettük, olyan körülmények között, amelyek során a biológiai anyag kezdeti hőmérséklete 36? 37 °C volt. 4% nátrium-citrát oldatot 1: 4 arányban a vér stabilizálására használtunk. A hegesztő eszköz munkarészének és a véna falának optimális érintkezése érdekében a vénaszegmenseket kívülről mechanikusan komprimáltuk.
Az EVH hatásának eredményeit a VSM szegmensek vizuális és morfológiai változásai alapján ítéltük meg. A hegesztés elektromos paramétereinek dinamikáját (hatásos teljesítmény és ellenállás) érintés nélküli USB-kompatibilis érzékelőkkel mértük. A hegesztési varrat területén a véna fal és a paravasalis zsírszövet hőmérsékletét kontakt hőmérőkkel határoztuk meg. Az adatok feldolgozására és grafikus megjelenítésére Matcad alkalmazáscsomagot használtuk.
A pathomorphológiai vizsgálat során a véna darabokat 10%-os neutralis, pufferolt formalinban rögzítettük. Készítményeket azután haematoxylin és eozin festéssel, valamint Van Gieson szerinti (a kollagén és sima izom - rostok) festéssel, elastikus rost festéssel (Elastic Stain Kit, Richard-Allan Scientific, Subsidiary of Thermo Fisher Scientific) értékeltük (11). A pathomorfológiai vizsgálatot és a fényképarchiválást "ZEISS" (Németország) fényoptikai mikroszkóppal "Axio Imager" segítségével végeztük el. "A2" adatfeldolgozó rendszerrel a lencsék nagyítása 5x, 10x, 20x, 40x, továbbá 1,5-es binokuláris fejjel és 10-es szemlencsés ERc 5s kamerával - ZEISS (Németország), továbbá Primo Star adatfeldolgozó rendszerrel, speciális kromatikus lencsékkel és ZEISS "Plan-Achromat" 4x, 10x, 40x xioCam 105 színes kamerával vizsgáltuk.
A biológiai anyagok mintavételét és a klinikai vizsgálatok ban való részvételt a betegek önkéntes, tájékoztatáson alapuló beleegyezése alapján döntöttük el. A programot és a tanulmánytervet a National Medical Academy of P. L. Shupykról elnevezett Posztgraduális Oktatás bioetika bizottsága hagyta jóvá (protokoll No. 5, mint a május 5, 2015).
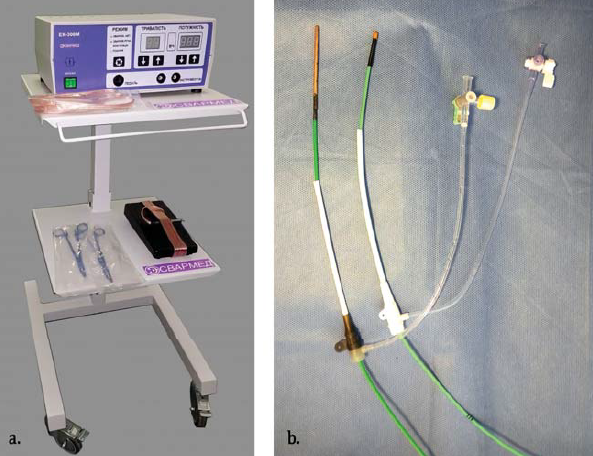
1. ábra. Élő szövetek hegesztésére szolgáló generátor
(a.) EK 300M ("Svarmed", Ukrajna) és
(b.) hegesztő eszközök 9 -10 Fr-es bevezetővel.
a. A műszer jellemzői. Az EVH eszköz egy áram - fejlesztőből ? az EK 300M ?Svarmed? (Ukrajna) és élő szövetek hegesztésére szolgáló multifunkcionális eszközből áll (2) (1. ábra). A generator az információfeldolgozás és vezérlés céljából egy mikroprocesszorral van felszerelve, ezáltal 4 üzemmódban használható: koaguláció, vágás, kézi és automatikus hegesztés. A hegesztőfej egy munkarészből, a főkábelből és a fogantyúból áll (2. ábra). A hegesztő munkarésze egy 2-3 mm átmérőjű és akár 5 cm hosszú bipoláris elektróda. A 9?10 Fr méretű intro - ducert a műszer bevezetésére használjuk.
b. Az EVH automatikus üzemmódjának működési rendszere. A kiválasztott ?automatikus hegesztési? módnak megfelelően nagyfrekvenciás feszültség keletkezik; a feszültségkülönbséget a hegesztő munkarész elektródáira kell alkalmazni. Az elektródákon és a véna falon áthaladó áram a bekapcsolási ciklus során hevít, ami a véna fal fehérjeösszetevőinek kiszáradása és denaturálása következtében spazmushoz és vénaelzáródáshoz vezet.
Az áram 10 és 100 V közötti feszültségű, 50-500 kHz-es frekvenciával 0,1-től 250 kHz-es modulációval váltakozik, a szövet ellenállás 0,1-től 1000 Ohm-ig terjed, ami a véna falat rendszerint 55?80 °C-ra melegíti, a hőeloszlás mélysége 1,5 ?2 mm-ig terjed. Az áramhatás időtartamát a relatív rezisztencia együtthatója határozza meg a következő képlet szerint: k = Ri(ti)/R0(t0), - ahol Ri(ti) az áramlási ellenállás, az R0(t0) a kezdeti ellenállás. Az adatfeldolgozási és ellenőrzési egység által rögzített k érték bizonyos szintjének elérésekor a készülék kikapcsol.
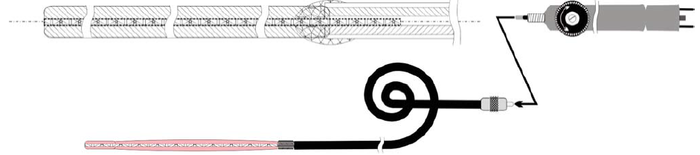
2. ábra. A hegesztőeszköz sematikus terve: 1 ? munkarész; 2 ? rugalmas kábel; 3 ? fogantyú; 4 ? kábelcsatlakozó; 5 ? munkarész elektródák.
c. Az EVH klinikai alkalmazásának technikája. A hegesztő részt, a refluxos véna szakasz distalis végén, UH irányítás mellett vezetjük be. A hegesztőfej proximális végét a sapheno-femoralis junkcióban a vena epigastrica beömlésénél helyezzük el. A parvo-poplitealis junkcióban pedig, 1 cm-re a poplitealis vénától (3. ábra).
A tumescens érzéstelenítőt az elfogadott módon, UH ellenőrzés alatt, Klein oldattal, vagy 0,125% bupivacain oldattal, 1 cm-es szakaszonként 5-10 ml -t injektálva végezzük. Így az érzéstelenítés mellett a vénák külső összenyomása is megtörténik. Ez adja az optimális érintkezést a véna fal és a műszer között.
A műszer aktív fejének helyzetét ultrahanggal ismét ellenőrizzük, majd a kezelő aktiválja a készüléket, amelyet hangjelzés kísér, ez a kezelés során végig hallható. Az elektrotermikus abláció a kijelölt vénán belül történik, a kezelés hossza megegyezik a műszer munkarészének hosszával, ez 1,5-5 cm lehet. A folyamatot UH-al kontrolláljuk. Az adott szakasz kezelése után, a kezelő fejet továbbvezetjük a következő kezelésre váró szakaszba, ahol a leírt folyamatot megismételjük.
A hegesztés befejezése után a kezelő fejet el kell távolítani a vénából. A beavatkozást mini-phlebectomiával vagy szkleroterápiával lehet kiegészíteni. A végtagok rugalmas kompressziójának alkalmazása után a beteg önállóan hagyja el a műtőt, a továbbiakban aktív lábhasználatra, járásra bíztatjuk.
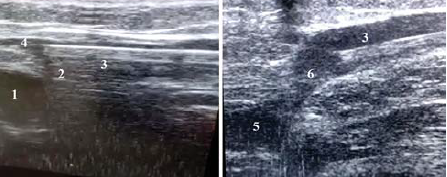
3. ábra. A hegeszt.eszköz elhelyezese: 1 . femoralis vena; 2 . sapheno-femoralis junkcio; 3 . hegeszt.eszkoz; 4 . vena ?upigastrica;
Eredmények
Az alapvizsgálatok eredményei. A véna hegesztéses vizsgálatok minden esetben a vénák összetapadását eredményezték, amelyet a leírt elektromos hegesztési áram paraméterekkel, ill ennek hatására bekövetkező véna fal hőmérséklet változással értünk el (4. ábra).
Az energia leadás elején jelentős véna spasmus lépett fel. Ez 2-3 mm-re túlért a hegesztő-fej munkarészének disztális pólusán, amelyet a hatásos teljesítmény gyors növekedése kísért. Ezután a kiszáradás jelenségeit, a gőz felszabadulását és a véna fal megvastagodását észleltük. Ekkor érjük el a hatásos teljesítmény maximális és az ellenállás minimális értékét. Az energia leadás meg - szüntetése a véna fal denaturálódásának kialakulásakor történt (5. ábra). Ezt maximális elektromos ellenállásnövekedés kísérte.
Az alkalmazás időtartama a különböző véna szakaszokon, függetlenül azok átmérőjétől és a fal vastagságától, 5-12 mp között volt. Véna fal perforációt, vagy a hegesztőfej munka felületén biológiai anyagok rátapadását ill. karbonizálódását nem észleltük.
A kontakt hőmérés adatai szerint a hegesztési területen a véna fal hőmérséklete rendszerint 55?80 °C volt. Az aktív ciklusban, a maximális hőmérsékleti érték 150?200 °C volt, és 0,02?0,6 másodpercig tartott. Az aktivitás után, a véna lehűlése a hegesztési terület kezdeti hőmérsékletére 5?7 másodpercen belül megtörtént. A hő terjedését a paravasalis zsírszövetben a véna faltól 1,5-2 mm távolságban mértük. A paravasalis zsírszövet csúcshőmérséklete elérte a 85?90 °C-ot, és 0,1?0,2 másodpercig tartott. A paravasalis zsírszövet károsodásának jeleit nem észleltük, beleértve az ismételten, ugyanabban a vénarészben végzett kezeléseket is (6. ábra).
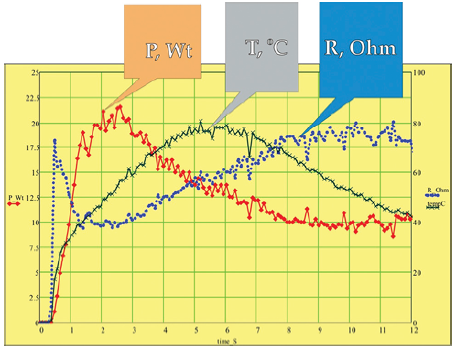
4. ábra. A hőmérséklet- és elektromos paraméterek változásainak dinamikája az endovénás hegesztés automatikus ciklusa alatt.
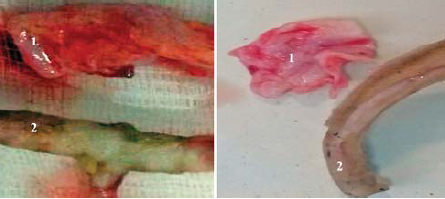
5. ábra. Az endovénás hegesztés hatásának eredményei:
1 ? kezeletlen v. saphena magna;
2 ? v. saphena magna részlet egyetlen kezelési ciklus után.
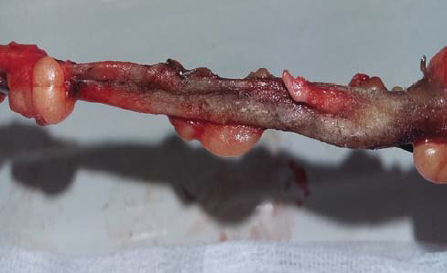
6. ábra. A v. saphena magna részlete 3 kezelési ciklus expozíciója után: a paravasalis zsírszövet nem sérült.
Haematoxilin-eosin festés során, a véna fal minden rétegében dismukoidosis, az endothel koagulációja és invaginációja miatt a lumen beszűkülése és csillagszerű deformációja volt látható. Az ér egyenetlen spasmusát, a fal rétegződését és az adventicia leválását okozó bullosus szerkezetét találtunk (7. ábra).
A véna fal belső és középső rétegeiben, e struktúrák különböző festései során a kollagén és simaizomrostok pusztulását és homogenizálódását észleltük (8. ábra).
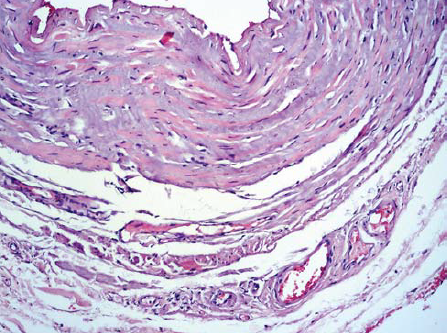
7. ábra. A v. saphena magna szövettani metszetének részlete az endovénás hegesztés után: az endothelium lelapulása és a véna fal rétegződése a bullosus elváltozás miatt, minden réteg nyilvánvaló dismukoidosisa és stasis a vasa vasorumban.
Festés hematoxin-eozinnal. Nagyítás: 100x.
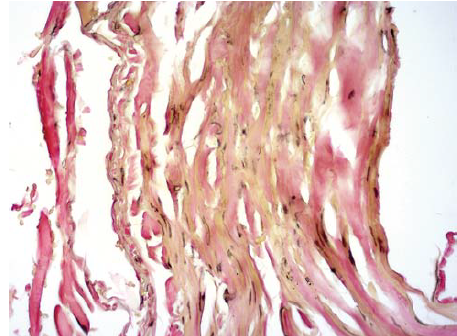
8. ábra. A v. saphena magna részlete az endovénás hegesztés után: az endothelium koagulációja és lelapulása, a vénafal rétegződése, kollagén és simaizomrostok homogenizálódása.
Van Gieson szerinti festés. Nagyítás: 200 x.
Az adventícia rétegében a rugalmas rostok pusztulásának és delaminációjának jeleit találtuk. Más rétegekben a rugalmas szerkezetek megsemmisülnek. Az adventicia rétegében, egyes gócokban a vasa vasorum spasmusa látható, az idegtörzsek ép részletekben megmaradtak, míg a zsírszövet részletek túlnyomórészt megőrződtek (9. ábra).
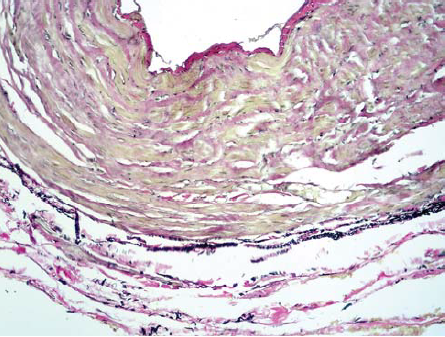
9. ábra. A v. saphena magna részlete az endovénás hegesztés után: a kollagén és a simaizomrostok destrukciója és homogenizálása a mediában, a rugalmas rostok körülírt destrukciója és rétegződése az adventitiában.
Festés "elastic stain kit".
Nagyitás x 100.
A klinika-alapú vizsgálatok eredményei. A kezelés időtartama, a VSM és a VSP különböző részein, a műtéten belül 5 és 12 másodperc között váltakozott. Ez idő alatt az elzáródás UH jeleinek kialakulását (spasmus, a véna fal meg - vastagodása és a vénát borító hang - visszaverő massza kialakulása) észleltük (10. ábra).
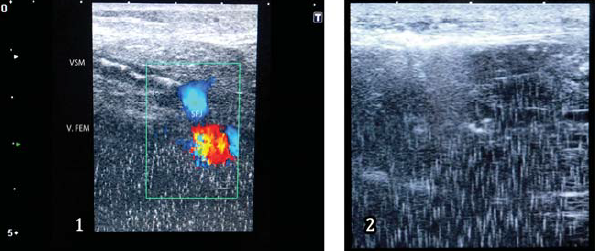
10. ábra. Endovénás hegesztés ultrahang képe:
1 ? a sapheno-femoralis junkció;
2 ?a v. saphena magna törzs (középső harmad).
A kezelés befejezése után az elzáródás UH jelei mellett a véna spasmus és a véna elzáródás jelei, továbbá a kezelő fej eltávolításakor az ellenállás érzése, valamint a kezelő fej ellenkező irányú mozgatásának akadályozottsága igazolják a kezelt érszakasz elzáródását.
A műtétek után sem az általános állapot, sem a gyaloglási teherbírás nem romlott a betegek körében. Nem volt fájdalma 17 betegnek (65,4%), míg további 9 (34,6%) azt 3 pontra értékelte (mérsékelt fájdalom), melynek időtartama nem haladta meg a 12 órát.
A 2,, 7,, és 14. műtét utáni napon a kezelt VSM és VSP szakaszok UH képe, azok elzáródását mutatta, minden esetben (11. ábra).
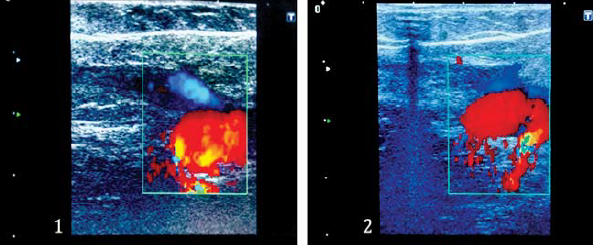
11. ábra. Endovénás hegesztés eredményei a sapheno- femoralis junkcióban:
1 ? a műtét után 2 nappal, 2 ? a műtét után 14 nappal.
A műtétek után 1 hónappal, 7 esetben (26,9%) fibrózis UH jeleit lehetett látni, míg 3 hónap elteltével 12 betegnél (46,2%) észleltük a vénák fibrózisát (12. ábra).
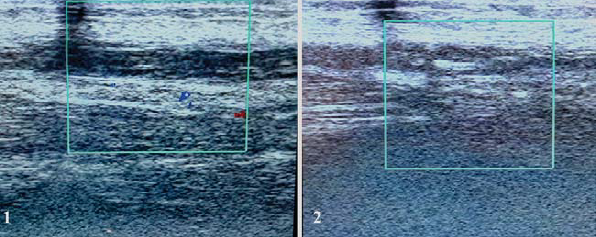
12. ábra. A comb v. saphena magna endovénás hegesztésének eredményei:
1 ? a műtét után 1 hónappal; 2 ? a műtét után 3 hónappal.
A 6 hónapos megfigyelési időszak alatt a kezelt véna szegmensek fibrózisát 26 betegnél (100%) észleltük. Minden betegnél tipikus "termikus crossectomia" -t értünk el (13. ábra).
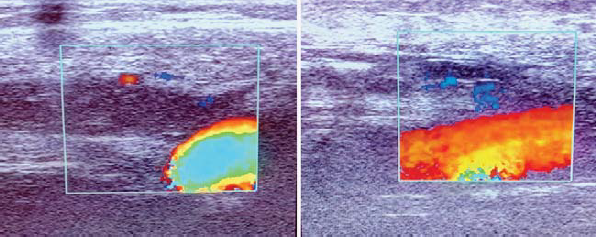
13. ábra. Ultrahang képek a sapheno-femoralis junkcióról, 6 hónappal az endovénás hegesztés után.
A pozitív UH eredmények mellett minden beteg kielégítő kozmetikai eredményt és a KVB klinikai tüneteinek regresszióját mutatta, már a megfigyelés első hónapjaiban (14. ábra).
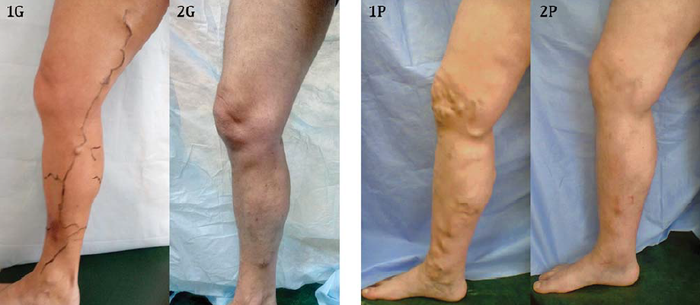
14. ábra. Az endovénás hegesztés alkalmazásának eredményei:
1 ? G. beteg, a műtét előtt és után 1 hónappal; 2 ? P. beteg a műtét előtt és után 2 hónappal.
Szövődményeket, beleértve az égési sérüléseket, a trombózist és a paresztéziát, egyik esetben sem regisztráltunk. Az első 5? 10 nap során, a kezelt vénás törzsek vetületében subcutan ecchymosis minden betegnél többékevésbé nyilvánvaló volt (15. ábra). A tumescens anaesthesia ezen hatása az antikoaguláns profilaxissal együtt okolható, de ez regrediált és nem befolyásolta sem a posztoperatív fájdalmat, sem a kezelés eredményességét.
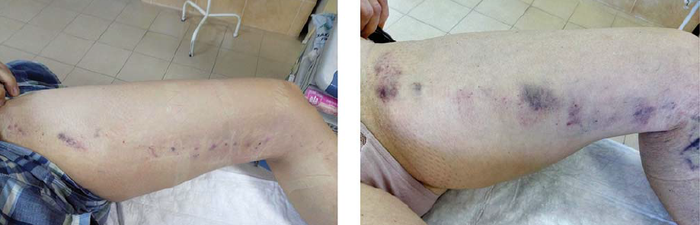
15. ábra. Bőr ecchymosis a v. saphena magna endovénás hegesztése utáni második napon.
Megbeszélés
Az alap-vizsgálatok eredményei azt mutatták, hogy a hegesztő eszköz alkalmas a megfelelően szabályozott nagyfrekvenciás, modulált áram intraluminaris alkalmazására. Hatására a véna spasmus és elzáródás a véna fal szövetek denaturálása miatt következik be.
A véna hegesztés elektromos paramétereinek kontrollált vezérlőalgoritmusa lehetővé teszi a véna fal túlmelegedésének elkerülését és koagulációs nekrózisát. Az extravasalis kompreszszió biztosítja a hegesztő fej és véna fal optimális érintkezését. A kezelés a denaturálás bekövetkeztének pillanatában leáll, ezért nem kíséri a szöveteknek a műszer munkafelületéhez tapadása. Ezeket az eredményeket az alapvizsgálatok minden esetében észleltük, a vénák átmérőjétől, a maradék vér jelenlététől és a véna fal vastagságától függetlenül.
A termometriás és pathomorfológiai vizsgálatok eredményei megállapították, hogy a hegesztést összehasonlítva a termikus abláció más módszereivel, sokkal kissebb a hőhatás és a paravasalis szövetekben sincs elváltozás. Számos kísérleti tanulmány szerint a 80?100 J/cm lineáris energiasűrűségű lézer ablációnál a véna lumenében a hőmérséklet 95 és 300 °C között lehet (10); és a véna felszínén ? 90 -120 °C-os, ami a vénaszövet termikus károsodásához vezethet a véna fal koagulációjának és karbonizálásának alapján (12,14).
A megadott hőmérsékletértékek több mint 2-szer magasabbak, mint az általunk kapott értékek. A véna fal hegesztési területén történő melegítése lehetőleg ne haladhatja meg a fehérje denaturálásának hőmérsékletét. A véna fal és a fali zsírszövet hőmérsékleti csúcsának emelkedése kezelés alatt 0,02?0,6 másodperc volt. Ezek a számok nem haladják meg az ilyen típusú erek termikus relaxációs idejének értékeit, amit J. Bergan (9) mutatott ki. Ezenkívül a műszer munkarészéből származó enyhe hőeloszlás gyakorlatilag kiküszöböli a paravasalis szövetek károsodásának kockázatát.
A hegesztés után kapott patomorfológiai vizsgálatok eredményeinek és a lézer-műtét hasonló adatainak összehasonlítása, a véna falban nyert eltérő jelleget és mélységet jelzik. A lézer-műtét után az ajánlott paraméterek mellett a morfológiai változások a teljes véna falat érintik, az endothel, subendothel, izom és adventicia rétegek koagulációja formájában, míg véna spasmus csak minimális mértékben figyelhető meg (10,14). Ugyanakkor a hegesztés után látható változások hasonlóak az RFA alkalmazása után leírtakkal: elsősorban a véna fal belső és középső rétegeinek megfelelően, továbbá a spasmus nyilvánvaló jeleivel, valamint az izomréteg és az adventitia szétválásának formájával (3).
Véleményünk szerint a hegesztés alkalmazásával kapcsolatos első tapasztalatok biztató eredményeket mutattak. A VSM és a VSP fibrózisának UH jelei 3-6 hónap alatt tanúskodnak a hegesztési-módszer nagy hatékony - ságáról, beleértve a nagy átmérőjű vénákat is. A szövetek viszonylag alacsony hevítése a kezelés során, lehetővé teszi a véna fal koagulációs nekrózisának elkerülését, és minimálisra csökkenti az olyan speciális szövődmények kialakulásának kockázatát, mint a paravasalis égési sérülések és a paresztézia. Ezenkívül a független kutatások során kapott eredmények arra utalnak, hogy az energia - hatások paramétereinek automatikus generálási és ellenőrzési módja lehetővé teszi, hogy egységesítsük a pozitív ablációs eredményeket, a különböző klinikákon.
Tekintettel azonban a megfigyelések kis számára és a viszonylag rövid időre, a tapasztalatok további gyűjtésére van szükség.
Következtetések
- A hegesztés lehetővé teszi a szubkután vénák szabályozott elektrotermikus ablációját a véna fal összetevőinek denaturálása révén.
- Az endovénás hegesztés klinikai alkalmazásának első eredményei biztatóak: a VSM és a VSP fibrózisa a 6 hónapos megfigyelési időszak alatt jól észlelhetően bekövetkezett, a kozmetikai eredmény a betegek 100% - ánál jó volt.
- A kezelés automatikus vezérlési módja segítségével a vénákban és a paravazális szövetekben hatásos, viszonylag alacsony hőmérsékletű melegítést végez, az automatizmus kiküszöböli a szubjektív tényezők hatását az ablációs eredményekre, ami lehetővé teszi az endovénás hegesztést nagy átmérőjű vénák esetén is.
Irodalom
- Chernukha LM, Horbovets VS, Vlaykov GG, Savoliuk SI, Khodos VA, Diadyk OO [ta in]. Mozhlyvosti zastosuvannia zvariuvalnoi tekhnologii v likuvanni varykoznoi khvoroby nyzhnikh kintsivok [Possibilities of application of welding technology in the treatment of varicose disease of the lower extremities]. Klinichna Flebologiia. 2019;(11)1:43-4.
- Horbovets VS, Kunkin DD, Kosakovskyi AL, Krestianov MYu, Liubchenko AS. Prystrii dlya endovenoznoi obliteracii [Device for endovenous obliteration] Patent Ukrayiny ą 120462. 2017 Lyst. 10.
- Horbovets VS, Savoliuk SI, Diadyk OO, Gvozdiak MM, Gerashchenko RA. Rozrobka ta pershyi dosvid zastosuvannia avtomatychnogo rezhymu endovenoznogo elektrozvariuvannia v likuvanni varykoznoi khvoroby nyzhnikh kintsivok [Development and first experience of automatic mode of endovenous electric welding in the treatment of varicose disease of the lower extremities]. Art of medicine. 2018;8(4):35-43.
- Palamarchuk VI, Horbovets VS, Khodos VA, Balatsky RO, Bondarenko YuI, vynakhidnyk; NMAPO imeni Shupyka PL, patentovlasnyk. Sposib obliteracii velykoi pidshkirnoi veny [A method of obliteration of the great saphenous vein] Patent Ukrayiny ą 113093. 2016 Grud 12.
- Paton BE, Ivanova ON, redaktory. Tkanesokhraniaiushchaia vysokochastotnaia elektrosvarochnaia khirurgia [Tissue-preserving high-frequency electric welding surgery]. Kiev: NANU, 2009. 200 s.
- Paton BE. Svarka ł rodstvennie tekhnologii v medicyne [Welding and related technologies in medicine]. Avtomat. Svarka. 2008;11:13-24.
- Savelev VS, Gologorskyi VA, Kyryenko AI. Flebologiia [Phlebology]. Moskva: Medicyna, 2001. 664 s.
- Savoliuk SI, Horbovets VS, Gvozdiak MM, Kunkin DD, Krestianov MYu. Teoretychni, eksperymentalni ta klinichni aspekty zastosuvannia endovenoznogo elektrozvariuvannia u likuvanni varykoznoi khvoroby [Theoretical, experimental and clinical aspects of the use of endovenous electric welding in the treatment of varicose disease]. Endovaskuliarna neirorentgenokhirurgiia. 2017;19(1):49-65.
- Bergan JJ, editor. The Vein Book. Philadelphia: Elsevier, Inc; 2007. 608 p.
- Disselhoff BC, Rem AI, Verdaasdonk RM, der Kinderen DJ, Moll FL. Endovenous laser ablation: an experimental study on the mechanism of action. Phlebology. 2008;23(2):69-76. Available from: DOI: 10.1258/phleb.2007.007038.
- Rosai J, editor. Rosai and Ackerman?s Surgical Pathology Seven edition. Vol. 1, Ch. 2,3. Philadelphia: Elsevier, Inc.; 2011. 2750 đ.
- Shahid KR, Dellon AL, Amrami KK, Spinner RS. Sciatic and peroneal nerve injuries after endovascular ablation of lower extremity varicosities: case reports and review of the literature. Ann Plast Surg. 2015;74(1):64-8. Available from: DOI: 10.1097/ SAP.00 0000 0000000193.
- Kelleher D, Lane TR, Franklin IJ, Davies AH. Socioeconomic impact of endovenous thermal ablation techniques. Lasers Med Sci. 2014;29(2):493-9. Available from: DOI: 10.1007/s101 03-013-1453-8.
- Proebstle TM, M, D, J [et al.]. Thermal damage of the inner vein wall during endovenous laser treatment: key role of energy absorption by intravascular blood. Dermatol Surg. 2002;(28)7:596-600.
Chernukha L M,
Dept Vasc Surg, National Institute of Surgery
and Transplantology named after A.A. Shalimov.
03680 m. Kyiv, Heroes of Sevastopol street 30, Ukraine
Érbetegségek: 2020/1. - 13-22. oldal


