Az elmúlt évtizedekben a szén-dioxid-fürdő kezelés az érbetegek komplex terápiájában tudományosan bizonyítottá vált, és széles körben alkalmazzák az érbeteg-rehabilitációban. A vizsgálat elsődleges célja a szénsavködfürdő vegetatív idegrendszerre kifejtett hatásának, a szimpatikus értónus csökkentésének bizonyítása, másodlagos cél a kezelés idejének optimalizálása volt. A vizsgálatba a beválasztási kritériumok alapján 30 krónikus perifériás verőérbeteg került a kezelt-, és 10 a kontrollcsoportba. A kezelt betegeket tovább bontottuk diabéteszben szenvedő (12 fő) és nem szenvedő (18 fő) alcsoportba. A vizsgált paramétereket a járástávolság (DT), a boka-kar nyomás index (ABI), a szisztolés vérnyomás, a pulzusszám, valamint a bőr hidrózisa mindkét alsóvégtagon (standard apicalis bőrterület saját fejlesztésű eszközzel mért értékeiből számítva) a nulladik, az első, a második és harmadik héten, majd 3 és 6 hónap múlva rögzítettük. A kezelt csoportokban a kezelés előre haladásával együtt növekedett az ABI és a járástávolság értéke. A járástávolság a kezelés után is emelkedett a 3 hónapos vizsgálat időpontjában, azonban a féléves követés idejében már kisebb volt az adott idő alatt megtett út, mint 3 hónappal ezelőtt, viszont még mindig több volt, mint a kezelés megkezdése előtt. A diabéteszes csoportban nagyobb mértékben csökkent a járás - távolság, mint a nem diabéteszes kezelt csoportban. Az ABI értéke az első kontroll (3 hó) alkalmával a nem diabéteszes csoportban nagyobb volt a kezelés végénél tapasztaltnál, a diabéteszes csoportban azonban kisebb. A 6 hónapos vizsgálaton mindkét csoportban csökkent az ABI a megelőző értékhez képest, azonban kedvezőbb volt a kiindulási állapotnál. A pulzus és a szisztolés vérnyomás változása nem volt számottevő, és eltérés a kezelt- és kontrollcsoportok között se volt tapasztalható. A vízveszteség csökkenése mind a bal mind a jobb oldalon a kezelt nemdiabéteszes csoportnál az első kontroll vizitig figyelhető meg, majd a féléves vizsgálatnál emelkedett, de nem érte el a kezelés előtti értéket. A diabéteszes betegek esetében a csökkenés csak a második kezelés után, a harmadik vizit időpontjában jelentkezett, és folytatódott a kezelés után a 3 hónapos kontrollvizsgálat adatai szerint, majd ehhez képest enyhén emelkedett a 6 hónapos vizsgálat során. A szénsavködkezelés során bekövetkező bőrhidróziscsökkenés bizonyította a kezelés sympaticolyticus hatását, mely eltérő a diabéteszes és a nem diabéteszes csoportban, hasonlóan a járástávolság, és az ABI növekedéséhez. Az optimális kezelés így egyénre szabottan növelhető a diabéteszes betegeknél a kívánt tartós effektus eléréséhez, de félévente a kezelést minden esetben ajánlatos ismételni.
Érbetegségek: 2016/3. - 55-63. oldal
KULCSSZAVAK
szénsavködfürdő, sympaticolysis, járástávolság, boka-kar index, bőrhidrózis
Bevezetés
Az elmúlt évtizedekben a szén-dioxid-fürdő kezelés az érbetegek komplex terápiájában tudományosan bizonyítottá vált és széles körben alkalmazzák az érbeteg-rehabilitációban (1, 2, 3, 4, 5). Hazánkban kevésbé elterjedt, de a természetes CO2 gázforrásokkal rendelkező országokban nagy hagyománya van a CO2 gázfürdőnek, melynek lényege, hogy a gáz alakú CO2-t vízfürdővel való egybekapcsolás nélkül használják fel és a fej kivételével a beteg egész teste vagy kezelendő testrésze szén-dioxiddal telt gáztérbe kerül (6, 7, 8, 9). Hediger és Winterschnitz kísérletileg igazolták, hogy az epidermis a CO2 számára a diffúzió törvényei szerint átjárható, ebből adódóan 90% feletti CO2 koncentrációnál 60% feletti relatív páratartalomnál,10-30 ml/perc/testfelületm2 CO2 szívódik fel. A felszívódó gáznak lokális és általános kemospecifikus élettani hatásai vannak (10, 11, 12, 13). A vizes fürdővel szemben a gázfürdő előnyei közé tartozik, hogy magas CO2 koncentráció érhető el, a hidromechanikai terhelés nem érvényesül és bőrkímélő, hámhiány esetén is igénybe vehető. A jelenlegi alkalmazási gyakorlat (napi 20 perc 3 héten keresztül) tapasztalati úton alakult ki (3, 6). A 20 perces időtartamot az észlelt bőrkipirosodás, a három hetet a hatás tartóssága indokolta. A 2007-ben elkezdett több ezer beteget érintő utánkövetéses felmérés bizonyította, hogy az egyformán adagolt kezelés a beteg állapotától függően eltérő 3 hónaptól egy évig tartó hatást biztosít. Ettől függően a kezelést a gyógyszerek szedése mellett időnként ismételni kell. A CO2 élettani hatásai közül ismert közvetlenül az érrendszerre kifejtett, a prekapilláris ellenállást csökkentő, a mikrocirkuláció autoregulációjában való részvétele. Az autoregulációban részt vevő CO2 a prekapilláris ellenállás csökkentése révén csökkenti a perifériás érellenállást, preformált kapillárisok nyílnak meg, a mikrocirkuláció javul (14, 15, 16, 17). A CO2-fürdő hatását növeli, hogy a magasabb CO2-szint az oxihaemoglobin disszociációját növeli (Bohr effektus), aminek következtében az oxigén parciális nyomása nő, a szövetek oxigén utilizációja javul. A CO2-fürdő fenti hatásai gyorsan jelentkeznek és a kezelés ideje alatt végig tartanak, de nem magyarázzák a fürdő hosszú távú kedvező gyógyhatását. Feltételezzük, hogy a fenti, közvetlen perifériás érreakció, vazodilatációs effektusa mellett a CO2-fürdőnek az autonóm idegrendszerre kifejtett hatása is van, ami magyarázza a hosszú távú kedvező eredményt. Vizsgálatunk céljai a szénsavas ködfürdő autonóm (vegetatív) idegrendszerre kifejtett hatásának, a szimpatikus értónus csökkenésének bizonyítása (elsődleges cél), ill. másodlagosan a kezelés idejének optimalizálása voltak.
Anyag és módszer
A vizsgálatba, a beválasztási kritériumok alapján 30 krónikus perifériás verőérbeteg került a kezelt-, és 10 a kontrollcsoportba. A kezelt betegeket tovább bontottuk diabéteszben szenvedő (12 fő) és nem szenvedő (18 fő) alcsoportokra. Két kezelt beteg esetében a járástávolság nem került értékelésre, mert a mérés alatt tartós lábikragörcs lépett fel.
Beválogatási kritériumok: krónikus perifériás verőérbetegség (peripheral arterial disease, PAD) Fontaine II. stadium, 40 év feletti életkor, stabil, minimum két hónapja fennálló 50-400 méteres járástávolság, írásbeli beleegyező nyilatkozat.
Kizárási kritériumok: Akut artériás trombózis, szívelégtelenség fulladással, a lábszárak duzzanatával, súlyos szívritmuszavar, gyakori mellkasi szorító jellegű fájdalom, heveny szívinfarktus és az azt követő 3 hónap, magasvérnyomás 200/100 Hgmm feletti értékkel, súlyos vese- és szemfenéki elváltozásokkal, szemműtét utáni 3 hónap, a vénák heveny gyulladása, trombózisa, súlyos légzőszervi megbetegedés fulladással, nagyfokú vérszegénység, pajzsmirigy fokozott működése (kezeletlenül), heveny gyulladásos betegségek, malignus megbetegedések bármely stádiumában, gyakori eszméletvesztéssel járó betegségek, végtagok kiterjedt fekélye, elhalása, súlyos alvadási zavarok, ismert gyógyszer-, drog-, ill. alkoholfüggőség. Olyan betegek akik nem kívánnak részt venni a tanulmányban vagy együttműködésük nem várható. Cselekvőképesség korlátozottsága vagy egyéb körülmények, amelyek miatt a páciens nem képes megérteni a tanulmány lényegét, jelentőségét.
A kezelt betegek standard szénsavas ködfürdő terápiája és vizsgálata a kapuvári Lumniczer Sándor Kórház Belgyógyászati (Angiológiai) és Mozgásszervi Rehabilitációs Osztályán történtek, a kontroll betegek a soproni Erzsébet Kórház páciensei voltak. A vizsgálat alatt a betegek életmódot nem változtattak, a perifériás verőérbetegség standard gyógyszeres kezelése (acetil - szalicilsav és statin) beállított volt (min. 3 hónap), a vizsgálat alatt egyéb keringésjavító kezelésben nem részesültek, valamint a korábban beállított egyéb gyógyszereiket szedték, a vegetatív idegrendszert befolyásoló gyógyszereken nem változtathattak.
A Regionális Kutatásetikai Bizottság a tanulmányt és a vizsgálati protokollt jóváhagyta. A tanulmány lefolytatása a Helsinki Egyezmény irányelveivel összhangban, a ?Good Clinical Practice? irányelveinek megfelelően történt.
Szénsavköd fürdő, standard terápia. A szénsavas ködfürdőhöz az alapanyagot, a ?79 °C-os szilárd szénsav - havat, a közeli Répcelakról (Linde Rt.) naponta szállítják a kórházba, ahol a felhasználásig hőszigetelt tartályokban tárolják. A szénsavköd előállításánál a szénsavhó azon fizikai tulajdonságából indulunk ki, hogy forráspontja alacsonyabb hőmérsékleten ?78,9 °C-on van, mint olvadáspontja, ami ?56,6 °C, így megolvadás nélkül elforr, azaz gáz formájában elpárolog. Ez a folyamat a szénsavhóra engedett 70 °C meleg vízzel explozív módon felgyorsítható, a víz és a CO2 egyesüléséből pár másodperc alatt tejfehér szénsavköd képződik. 2 kg szénsavhóból 5 l 70 °C-os víz hozzáadásával 1 m3-es kezelőtérben 92 vol%-os CO2 koncentráció és 90%-os relatív páratartalom, valamint 30 °C-os indifferens hőmérséklet érhető el. Ez azért lényeges, mert a bőrön keresztül a diffúzió törvényei szerint felszívódó CO2 mennyisége függ a fürdő CO2 koncentrációjától, páratartalmától, hőmérsékletétől, és a kezelés időtartamától. A fenti paraméterekkel maximális felszívódás érhető el. A 30 °C hőmérsékletű tejfehér szénsavköd másfélszer nehezebb a levegőnél, így alulról felfelé hömpölyögve megtölti a kezelőteret. Az így kialakult hőmérséklet és páratartalom együttesen járul hozzá a bőr pórusainak fellazításához, és ezáltal az emberi testbe a CO2 könnyebben és hatékonyabban hatol be. A fehér szénsavköd magassága vizuálisan is ellenőrizhető és forró víz adagolásával szabályozható. A kezelés időtartama 19 nap, napi 20 perc (standard terápia). A fenti paraméterekkel maximális felszívódás érhető el.
Vizsgált beteg-paraméterek: járástávolság (DT: computeri zált elektromos járószalagon, emelkedés 10%, sebesség 3,6 km/h), a boka-kar nyomás index (ABI: CW Dopplerkészülékkel mérve mindkét oldalon), szisztolés vérnyomás, pulzusszám, valamint a bőr hidrózisa mindkét alsó végtagon (standard apicalis bőrterület saját fejlesztésű eszközzel mért értékeiből számítva).

1. kép.
Saját fejlesztésű bőrhidrózismérő eszköz.
Bőrhidrózis mint az autonóm (vegetatív) idegrendszer működésének indikátora. Az apicalis bőrterületek szelektív szimpatikus beidegzése, myogen tónus nélkül, a perfúziós nyomás változásának bizonyos határán belül, egyszerű mérési lehetőséget kínál, a szimpatikus hatás csökkenésének vizsgálatára, standard körülmények között, a bőrterület hidrózisának mérésével. Egy olyan saját fejlesztésű bőrhidrózismérő eszközt fejlesztettünk és használtunk (1. kép), mellyel nagyon nagy pontossággal (1,8% RH) lehet meghatározni a transzepidermális vízveszteséget (TEWL). A mérőműszerbe egy SHT25 típusú pára- és hőmérséklet-érzékelő (továbbiakban: szenzor) került beépítésre, mellyel a bőr, víz-gát (water barrier) funkciójának legfontosabb paraméterét mérni lehet. A műszerben elhelyezett szenzor, a műszerben kiképzett kamrában, a víz elpárolgását, (a szenzor relatív páratartalmat és hőmérsékletet mérő képessége folytán) gyakorlatilag indirekt módon méri. Az említett kamra nyitott eljárású, azaz a kamra alsó és felső fele nyitott. A kamra alsó fele a bőrhöz szorosan érintkezik; a kamra alsó szélétől 10 mm-re található maga a szenzor, mely a mért értékeket, egy a műszerbe épített bluetooth adó segítségével, a párosított adat analizáló számítógépbe közvetíti. Nyitott kamra módszerünk előnye, hogy a bőr párolgása így folyamatosan mérhető. A szűk kamraméret (0.0002525663706 m2) pedig kiküszöböli a mérést negatívan befolyásoló esetleges légörvényeket.
Mért paraméterek. Hőmérséklet és relatív páratartalom került rögzítésre páciensenként 10 perces időintervallum alatt (ez több mint 100 mintavételt jelent). Ezen idő alatt a résztvevő páciensek TEWL értékeinek meghatározása mindkét lábon egyszerre történt. Az analizáló számítógép a fenti adatokból, illetve a mérés előtt meghatározott konstansok segítségével határozta meg a TEWL értékeket mindkét lábon az alább leírt számítási képletek alapján.

A betegek bevonása 2015. 02. 12 és 2015. 04. 03. között történt. A protokoll szerint vizsgált paramétereket belépéskor (0 hét), majd 1 hét, 2 hét, 3 hét, 3 és 6 hónap után rögzítettük. Az adatok a 6. havi vizsgálatokig álltak rendelkezésünkre.
A statisztikai vizsgálatokat az SPSSv17.0 programmal végeztük. A leíró statisztikai vizsgálat, az egyes vizsgálati időpontokban mért paraméterek átlagát, mediánját, minimum és maximum értékét, szórását, normalitás vizsgálatát, csoportonként tartalmazta. Az értékek normális eloszlását akkor fogadtuk el, ha a ferdeség és csúcsosság abszolút értéke kisebb volt 1-nél. Amely változóknál nem teljesült a normális eloszlás, logtranszformációt végeztünk. Az egyes paraméterek változását az egyes csoportokban, az öt vizsgálati időpont között vizuálisan és statisztikailag is elemeztük. A változások szemléltetése vonal diagrammal történt, amelyen az egyes paraméterek átlagait, az egyes vizsgálati időpontokban, csoportonként ábrázoltuk. A változások statisztikai elemzése a kezelt csoportnál történt, amelynek során a belépési értékhez viszonyítottuk a további vizitek értékeit, továbbá a kezelés utáni állapotváltozásokat is értékeltük. A normális eloszlású változóknál (akár logaritmikus transzformáció után) páros t-próbát, máskülönben a nem paraméteres Wilcoxon-próbát használtuk.
A kontroll- és kezeltcsoport, illetve a diabéteszes és nem diabéteszes alcsoport paraméterváltozásainak össze - hasonlítására a 4. (kezelés vége), az 5. (3 hónapos), 6. (6 hónapos) vizitek és 1. (belépési) vizitek közötti különbségi változókat képeztünk. A különbség statisztikai elemzésére a normalitás hiányában, a nem paraméteres Mann-Whitney és Kolmogorov-Smirnov tesztet végeztük el.
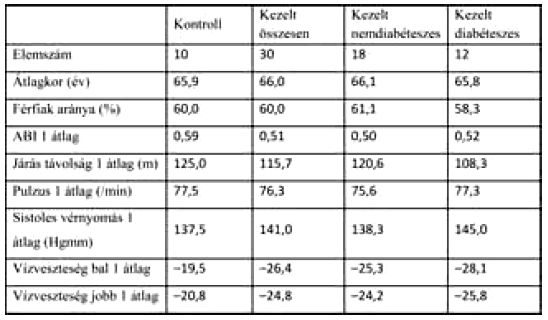
1. táblázat
A betegcsoportok belépési mutatói
Eredmények
A kezelés időszaka a kontrollcsoportban átlagosan 21 nap (min. 21 nap, max. 21 nap), a kezelt csoportban átlagosan 19,17 nap (min. 14 nap, max. 20 nap) volt. A kezelés kezdetétől számított 3 hónapos vizsgálat a kontrollcsoportban átlagosan 84 nap (min. 84 nap, max. 84 nap), a 6 hónapos vizsgálat átlagosan 160,5 nap (min. 160 nap, max. 161 nap) múlva történt, a kezelt csoportban 113,34 nap (min. 99 nap, max. 120 nap), illetve 200,36 nap (min. 152 nap, max. 242 nap) volt az átlagos követési idő. A betegek leíró mutatóit a vizsgálatba belépéskor az 1. táblázat mutatja.
A trendek vizuális vizsgálata során a következőket állapíthatjuk meg. A kezelt csoportokban a kezelés előrehaladásával együtt növekedett az ABI és a járás távolság értéke. A járástávolság a kezelés után is emelkedett a 3 hónapos vizsgálat időpontjában, azonban a féléves követés idejében már kisebb volt az adott idő alatt megtett út, mint 3 hónappal ezelőtt, viszont még mindig több volt mint a kezelés megkezdése előtt. A diabéteszes csoportban nagyobb mértékben csökkent a járástávolság, mint a nem diabéteszes kezelt csoportban. Az ABI értéke az első kontroll alkalmával a nem diabéteszes csoportban nagyobb volt a kezelés végénél tapasztaltnál, a diabéteszes csoportban azonban kisebb. A 6 hónapos vizsgálaton mindkét csoportban csökkent az ABI a megelőző értékhez képest, azonban kedvezőbb volt a kiindulási állapotnál. A pulzus és a szisztolés vérnyomás változása nem volt számottevő, és eltérés se volt tapasztalható a kezelt- és kontroll csoportok között. A vízveszteség csökkenése mind a bal, mind a jobb oldalon a kezelt nem diabéteszes csoportnál az első kontroll vizitig figyelhető meg, majd a féléves vizsgálatnál emelkedett, de nem érte el a kezelés előtti értéket. A diabéteszes betegek esetében a csökkenés csak a második kezelés után, a 3. vizit időpontjában jelentkezett, folytatódott a kezelés után a 3 hónapos kontroll-vizsgálat adatai szerint, majd ehhez képest enyhén emelkedett a 6 hónapos vizsgálat során. (1. ábra)
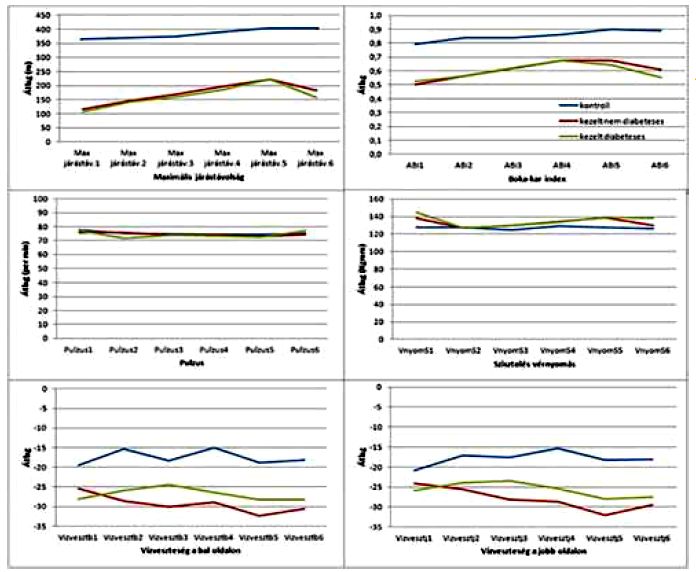
1. ábra.
A vizsgált paraméterek változása az egyes csoportokban.
A változások statisztikai értékelése azt mutatta, hogy szignifikánsan javult a boka-kar index értéke a kezelés során az egyes viziteken, a kiindulóállapothoz viszonyítva, mind a kezelt csoportban, mind pedig a két alcsoportjában, a nem diabéteszes és diabéteszes csoportban is. A javulás a 3 és 6 hónapos kontroll vizsgálaton is megmaradt a kezdeti állapothoz viszonyítva. A féléves vizsgálat alkalmával viszont szignifikánsan csökkent az értéke az előző kontrollhoz képest. Szintén szignifikánsan nőtt a maximális járástávolság mértéke mind három csoportban, minden vizit alkalmával a kiindulási állapothoz képest, és a kedvező változás a kezelés után is folytatódott a 3 hónapos viziten. Azonban a 6. hónapban végzett vizsgálaton szignifikáns csökkenés mutatkozott az előző állapothoz viszonyítva.
A pulzus esetében statisztikailag szignifikáns változás nem volt bizonyítható. Annak ellenére, hogy a terápia 2. hete után emelkedett a szisztolés vérnyomás, a bemeneti értékhez képest statisztikailag szignifikánsan csökkent értéke a kezelt csoportban, a kezelés ideje alatt és a féléves kontrollvizsgálaton is. A láb vízvesztésének a kezelés előtti állapothoz képest, statisztikailag szignifikáns mértékű csökkenése a 3 és 6 hónapos vizsgálaton volt kimutatható, mindkét oldalon. A jobb oldalon a vízveszteség-csökkenés a kezelés után is statisztikailag bizonyítható módon folytatódott az első kontroll vizsgálaton (2. táblázat).
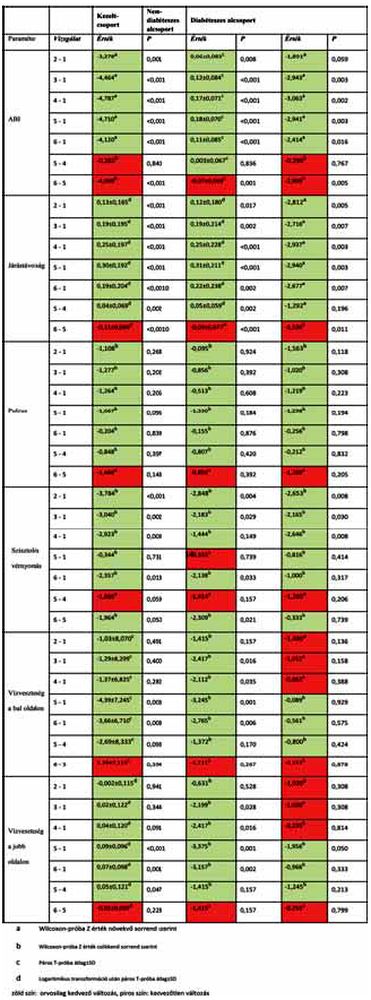
2. táblázat
Az egyes csoportokban mért változások statisztikai eredménye.
A kontroll- és kezelt csoportban mért változások összehasonlítása alkalmával szignifikáns különbség mutat kozott a járástávolság javulásában a 4. és 5. viziten, a kezdeti állapothoz képest, a kezeltcsoport előnyére. A boka-kar index pozitív változása statisztikailag bizonyítható módon nagyobb volt a kezelés után a szénsav terápiát kapott csoportban. A pulzus és a szisztolés vér nyomás változása a két csoportban statisztikailag nem tért el egymástól. A vízveszteség csökkenése szignifikánsan nagyobb volt a kezelt csoportban mindkét oldalon és minden vizsgált viziten, kivétel a bal oldalon a 3 hónapos viziten (3. táblázat).
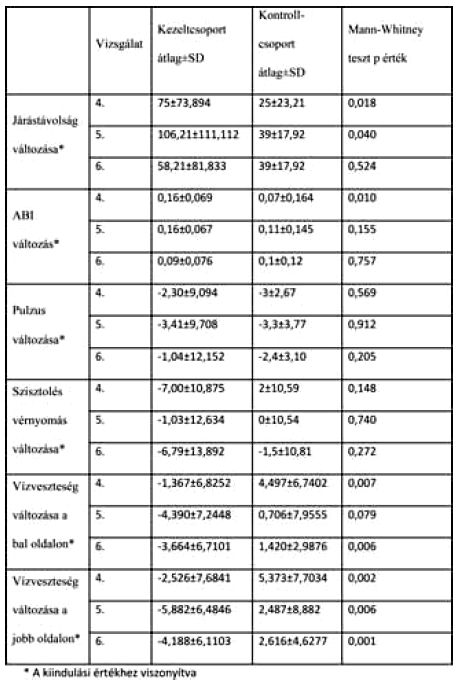
3. táblázat
A kontroll- és kezelt csoportban mért értékek változásának összehasonlítása.
A nem diabéteszes és diabéteszes kezelt al - csoportban mért értékek változásának összevetése során szignifikáns különbség csak a 3 hónapos víz - veszteség-változásnál volt kimutatható (4. táblázat).
Megbeszélés
Az elmúlt évtizedekben a CO2 gáz, keringési rendszerre történő hatásának makroszkópos effektusát írták le tapasztalati úton: perifériás arteriola dilatáció, kapilláris rezistencia csökkenés, preload-, afterload csökkenés, vérnyomás csökkenés, bradycardia (19, 20, 21, 22, 23). Fabry és munkatársai, Fontaine II. stádiumú betegeknél vizsgálta a rövid és hosszú távú klinikai és haemodinamikai vazodilatációs effektust, amelyet a percután felszívódott természetes CO2 gáz okozott (24). Az abszolút és a fájdalom nélküli járástávolság is nőtt 20 napos kezelés után. A hatás 3-12 hónapig tartott. Kezelésük alatt az ABI 37%-al nőtt, a mikrocirkulációs paraméterek és a szöveti oxigenizáció mértéke is javult. Saját eredményeink megerősítik ezen eredményeket. A dysbásiás távolság, a háromhetes kezelés alatt, az összes kezelt betegünk esetében, a három hónapos kontrollig fokozatosan emelkedett, majd a hat hónapos vizsgálatig fokozatosan csökkent. A diabéteszes csoportban drasztikusabban csökkent a DT a vizsgált utolsó három hónapban. Az ABI fokozatosan növekedett a háromhetes kezelés alatt mindkét csoportban, de a nem diabéteszes csoportban a növekedés a három hónapos kontrollig tartott, utána csökkent, ? a diabéteszeseknél már a három hónapos kontrollon csökkenés volt mérhető.
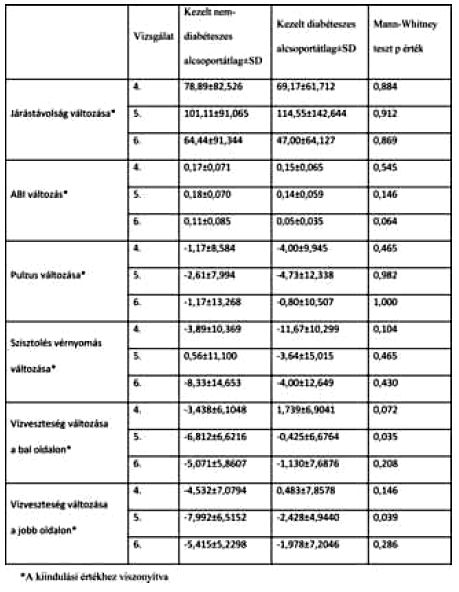
4. táblázat.
A nem diabéteszes és diabéteszes kezelt alcsoportban mért értékek változásának összehasonlítása.
A CO2 élettani hatásai közül ismert, közvetlenül az érrendszerre kifejtett, a prekapilláris ellenállást csökkentő, a mikrocirkuláció autoregulációjában való részvétele. Az Ohm-törvény értelmében valamely érterület/szerv vér áramlása a perfúziós nyomással arányos. Az egyes szervekben azonban az áramlás viszonylag független a perfúziós nyomástól. Egy adott nyomástartományban a perfúziós nyomás emelkedése a prekapilláris ellenállás növekedését, a nyomás csökkenése a prekapilláris ellenállás csökkenését váltja ki, létrehozva az anyagcserétől függő áramlási autóregulációt. Az autóreguláció következménye, hogy a nagyvérköri artériás nyomás változását nem követi automatikusan a kapillárisok nyomásának változása, ezért a kapilláris filtráció független az artériás középnyomás változásaitól. Az autoreguláció egyrészt a vascularis simaizomzat intrinsic tulajdonsága, másrészt a helyileg felszabaduló anyagcsere közti ? vagy végtermékeinek mint pl. a CO2 eredménye (25, 26). A miogén tónus változásai képezik az alapját az elsődlegesen fontos helyi keringésszabályozásnak, az áramlási autoregulációnak és az anyagcserétől függő szabályozásoknak (funkcionális és reaktív hyperaemia.) Feltételezzük, hogy a fenti közvetlen perifériás érreakció, a vazodilatációs effektus mellett a CO2 fürdőnek, az autonóm idegrendszerre kifejtett hatása is fellép, amely a hosszú távú kedvező gyógytényezőt magyarázza.
Mint ismert, egy szerv vagy testrész vérellátását az adott artériák perfúziós nyomása, az erek szimpatikus tónusa és a mikrocirkuláció autoregulációja határozza meg. A nagyvérköri értónus (teljes perifériás ellenállás) idegi szabályozásában kizárólag a szimpatikus ingerületek frekvenciájának változása szerepel. A teljes perifériás érellenállást a folyamatos szimpatikus idegrendszeri érszűkítő aktivitás tartja fent és változtatja szükség szerint. Alapszintű szimpatikus aktivitás minden körülmények között van. Az egyes érszakaszok szimpatikus beidegzésének sűrűsége rendkívül különböző. A legnagyobb beidegzési sűrűség az arteriolák szakaszán található, míg az aortában és a nagy artériákban a szimpatikus beidegzés szerényen reprezentált (26, 27, 28).
A myogen és a szimpatikus vasoconstrictor tónus mértéke az egyes szervekben jelentősen különbözik. Az apicalis bőrterületek ereinek nincs myogen tónusa, viszont a szimpatikus vasoconstrictor tónusa nagy, így a szimpatikus beidegzés megszüntetésével az apicalis bőr vérellátása sokszorosára javul. A bőr kipirul, hőmérséklete nő, verejték elválasztása csökken, meleg, száraz tapintatúvá válik. A perifériás vazodilatáció a megnövekedett paraszimpatikus és csökkent szimpatikus aktivitás következménye (Toriyama és Sato) (29, 30). Az apicalis bőrterületek szelektív szimpatikus beidegzése myogen tónus nélkül a perfúziós nyomás változásának bizonyos határán belül egyszerű mérési lehetőséget kínál a szimpatikus hatás csökkenésének vizsgálatára, standard körülmények között a bőrterület hidrózisának mérésével. A bőrhidrózist használtuk, mint indikátort, a simpaticolyticus hatás igazolására. A háromhetes szén-dioxid-ködfürdő kezelés alatt mindkét csoportban fokozatosan csökkent a hidrózismérővel kimutatott apikális vízveszteség, a kontroll csoporthoz képest, ahol gyakorlatilag konstans értékeket mértünk. Az acrális vízveszteség-csökkenés a kezelés simpaticolytikus hatásának tudható be. A vízveszteség-csökkenés a nem diabéteszes csoportban a három hónapos kontrollig figyelhető meg, majd enyhén emelkedett a féléves kontrollig. A diabéteszes betegeknél csak a kezelés harmadik hetében következett be hidróziscsökkenés, ez folytatódott a harmadik hónapig, majd enyhén emelkedett. Feltételezhetően a diabéteszes, következményes neuropathia miatt a szénsavködkezelés simpaticolytikus hatása csak később, hosszantartó kezelés hatására jelentkezett. Vizsgálataink alapján a diabéteszes érbetegek szénsavködfürdő terápiáját érdemes lenne meg - hosszabbítani, illetve három és hat hónap között a járástávolság-csökkenéssel korrelálva egyénre szabottan ismételni.
Következtetés
A szénsavas ködfürdőt a perifériás obliteratív verőérbetegek kezelésére, a komplex rehabilitáció részeként, évtizedek óta alkalmazzuk (31, 32, 33). A szénsavködfürdő direkt vasodilatációs effektusa jól tanulmányozott, széles körben ismert (34, 35). A perifériás verőérbetegek járástávolsága lényegesen nő, végtag - fájdalmaik mérséklődnek vagy megszűnnek, a trophicus elváltozások gyógyuló tendenciát mutatnak (3, 29).
Fizikai teljesítőképességük fokozódik, kevesebb gyógyszert fogyasztanak, kevesebb a kórházi kezelések száma, a betegek életminősége javul. A szénsavködfürdő kedvező hatásai hosszú távúak, átlagosan fél évig tartanak. A szénsavhókezelés során bekövetkező bőrhidróziscsökkenés bizonyította a kezelés simpaticolyticus hatását, melynek mértéke eltérő a diabéteszes és a nemdiabéteszes csoportban, hasonlón a járástávolság, és az ABI növekedéséhez. Az optimális kezelés így, egyénre szabottan növelhető a diabéteszes betegeknél, a kívánt tartós effektus eléréséhez, de félévente a kezelést ajánlatos minden esetben ismételni.
Irodalom
- Meskó É. (szerk.): Vascularis medicina. Therapia Kiadó, Budapest, 2004
- Ernst E. (1989): Peripheral vascular disease. Physical treatments may help. BMJ 299:873
- Ballagi F.: A szénsavgázfürdő jelentősége a perifériás érbetegek rehabilitációjában. Érbetegségek, 1995/3: 21?27
- Krüger H.: Vergleichende Untersuchung des therapeutischen Effectes von CO2 ? Gasbadern und krankengymnastischer Übungsbehandlung bei der Claudicatio intermittens. Dissertation, Berlin, 1979
- Schnizer W., Erdl R., Schops P., Seichert N. (1985): The effects of external CO2 application on human skin microcirculation investigated by laser Doppler flowmetry. Int J Microcirc Clin Exp, 4:343?350
- Ballagi F., Horváth I., Kerekes I.: Perifériás érbetegek rehabilitációjában elért eredményeink. Rehabilitáció, II/4:33?36 (1992).
- Okos B.: Érrendszeri megbetegedésben szenvedők rehabilitációja, In: Szív- és érbetegek rehabilitációja, szerk.: Böszörményi E., Endresz F., Hoffmann A., Balatonfüred?Budapest, 277?86. 372?91. (1983).
- Málnási G.: A csíki- és háromszéki gázfürdők a XVI?XIX. században. In: Hargita megye természetes gyógytényezői, szerk.: Jakab K., Hargita Megye Néptanácsa Egészségügyi Igazgatóság, Csíkszereda, 411? 426. (1974).
- Schwartz P., Zsirai K.: Érbetegségek kezelése a mihályi-i CO2 gázzal. Gyógyfürdőügy, 8/1: 1421. (1974).
- Duling B. R.: Changes in microvascular diameter and oxygen tension induced by carbon dioxide. Circulat Res, 23: 370. (1973).
- Frommherz E.: Experimentelle Untersuchungen über Durchblutungsanderungen der Haut und den Gasaustausch in Kohlensaurebadern. Dissertation, Freiburg, 1973
- Hartmann B., Bassenge E.: Steigerung der lokalen Hautdurchblutung durch CO2 Fussbader bei Normalpersonen und Gefasspatienten. Eine Untersuchung mit der Laser-Doppler-Flussmessung. Z Phys Med, 18:57. (1989).
- Hartmann B., Dreuws B., Bassenge E.: CO2-induzierte Zunahme der akralen Durchblutung und des Sauerstoffpartialdruckes bei arterieller Verschlusskrankheit. Dtsch Med Wschr, 116: 1617?21. (1991).
- May E.: Klinisch-experimentelle Untersuchungen über den therapeutischen Wert des Segment-Kohlensauregasbades im Vergleich zum konventionellen Gasbad. Dissertation, Berlin (Ost), 1980
- Schnizer W., Erdl R., Schops P., et al: The effects of external CO2 application in humán skin microcirculation investigated by laser Doppler flowmeter. Int J Microcirc, 4: 343. (1985)
- Hartmann B.: Results of the consensus-finding conference on carbon dioxide balneotherapy. Z Phys Med, 19. suppl. 1:11. (1990).
- Akamin Komoto Y., Nakao T., Sunakawa M., Yorozu H. (1988): Elevation of tissue PO2 with improvement of tissue perfusion by topically applied CO2. Adv Exp Med Biol 222:637?645
- Ballagi F.: A szénsavgázfürdőről. Balneo, Gyógyf., Gyógyindegenf., 1997. XVIII/3?4; 16?30.
- A szén-dioxid-gázfürdő. Körlevél. Országos Gyógy für dő - ügyi Igazgatóság. Gyógyfürdőügy, 5/2:10?102. (1971).
- Farkas K., Irányi J., Kérdő I.: A szén-dioxid-gáz physiotherápiás alkalmazása. Rheum. Balneol Allerg, XII/1:1?12. (1971).
- Duling B. R.: Changes in microvascular diameter and oxygen tension induced by carbon dioxide. Circulat Res, 23:370. (1973)
- Diji A. (1959): Local vasodilator action of carbon dioxide on blood vessels of the hand. J Appl Physiol 14(3):414?416
- Dorrance S., McClellan W.S. (1940): Effect of natural carbonated baths on rate and amplitude of pulse and blood pressure. Arch Phys Ther, 21:133?140
- Fabry R., Monnet P., Schmidt J. et al (2009): Clinical and microcirculatory effects of transcutaneous CO2 therapy in intermittent claudication. Randomized double-blind clinical trial with a parallel design. Vasa 38(3):213?224
- Johnson J.M., Proppe D.W. (1996): Cardiovascular adjustments to heat stress. In: Am Physiol Soc (ed), Handbook of Physiology. Environmental Physiology, Bethesda, MD, 215?243
- Kelogg DL (2006): In vivo mechanisms of cutaneous vasodilation and vasoconstriction in humans during thermoregulatory challenges. J. Appl. Physiol. 100:1708?19
- Fukuda S., Matchimoto M., Nishimura N. et al (1990): Endothelial modulation of nor-epinephrine-induced constriction of rat aorta at normal and high CO2 tensions. Am J Physiol 258: H1049?H1054
- Hashimoto M., Yamamoto N. (2004): Decrease in heart rates by artificial CO2 hot spring bathing is inhibited by â1-adrenoreceptor blockade in anesthetized rats. J Appl Physiol 96:226?232
- Toriyama T., Kumada Y., Matsubara T. et al (2002): Effect of artificial carbon dioxide foot bathing on critical limb ischemia (Fontaine IV) in peripheral arterial disease patients. Int Angiol 21:367?373
- Sato M., Kanikowska D., Iwase S. et al (2009): Effects of immersion in water containing high concentrations of CO2 (CO2-water) at thermoneutral on thermo - regulation and heart rate variability in humans. Int J Biometeorol, 53:25?39
- Hartmann B.R., Bassenge E., Hartmann M. (1997a): Effects of serial percutaneous application of carbon dioxide in intermittent claudication: results of a controlled trial. Angiology 48(11):957?963
- Hartmann B.R., Bassenge E., Pitler M. (1997): Effect of carbon dioxide ? enriched water and fresh water on the cutaneous microcirculation and oxygen tension in the skin of the foot. Angiology 48:337?343
- Hartmann B., Pittler M., Drews B. (2009): CO2 Balneotherapy for arterial occlusion diseases: Physiology and Clinical Practise. http://www.co2bath.com/academic-e.htm. Accessed 20 September 2009
- Savin E., Balliart O., Bonnin P. et al (1995): Vasomotor effects of transcutaneous CO2 in stage II peripheral occlusive arterial disease. Angiology 46:785?791
- Schmidt K.L. (2009): Carbon dioxide bath (Carbon dioxide spring). http://www.nutecint.com/Docs/Carbon%20Dioxide%20 Bath.pdf. Accessed 20 September 2009.
Dr. Galambos Barnabás Phd.
Soproni Gyógyközpont
Ez az e-mail-cím a szpemrobotok elleni védelem alatt áll. Megtekintéséhez engedélyeznie kell a JavaScript használatát.
Érbetegségek: 2016/3. - 55-63. oldal


