A krónikus vénás keringési elégtelenség kialakulásának pontos patomechanizmusa a mai napig nem is-mert. Azonban az utóbbi évek kutatási eredményei egyre inkább arra utalnak, hogy a folyamatban egy gyulladásos komponens is szerepet játszik. Ennek azért van nagy jelentősége, mert ez indokolja, hogy a bázisterápiának szánótó kompressziós kezelés mellett alkalmazzuk a gyulladásos komponensre is ható, egyéb hatásmechaniznmsaik miatt már eddig is jól bevált, adjuváns gyógyszeres kezelési lehetőségeket, a jól ismert flavonoidokat és a nemrégiben hazánkban is forgalomba került, eszcint tartalmazó készítményt.
Érbetegségek: 2005/2. 63-65. oldal
KULCSSZAVAK
Krónikus vénás elégtelenség, gyulludás, gyógyszerek
A krónikus vénás keringési elégtelenség gyakori megbetegedés, a vénás nyomás tartós emelkedését jelenti. Előfordulási gyakorisága Európában mintegy 2%. Kialakulásának legmagasabb incidenciája nőknél a 40-49 éves, míg férfiaknál a 70-79 éves korban van. Az alsó végtagi vénákban a vénabillentyűk záródási zavara és a következményes reflux, illetve a vénás rendszer okklúziója miatt pangás alakul ki. A pangás miatt megnövekedett vénás nyomás áttevődik a kapilláris rendszerre, ami a mikrocirkuláció szintjén akadályozza a keringést. A lassult keringés több módon is kihat a szövetek vér- és oxigénellátására. A pangás miatt nő a kapilláris-permeabilitás, ami ödémaképződéssel jár. Ennek következtében az extravazális térben fehéijedús, többek között fibrinogént tartalmazó folyadék halmozódik fel. Ha az in¬tersticiális vagy perikapilláris térbe fibrinogen kerül, az fibrinpolimerré alakul. Így perikapilláris fibrinmandzsetta képződik, ami diffúziós barriert jelent az oxigén számára. A folyadékkilépés következtében az intravazális hematokrit és ezzel együtt a vér viszkozitása is növekszik, ami természetesen szintén rontja a szövetek oxigenizációját.
 A kapillárisokban lelassult áramlás kedvez a fehérvér-sejt-csapda jelenség kialakulásának, amit nagyon szellemes kísérlettel igazoltak. Egészséges egyéneket és krónikus vénás keringési elégtelenségben szenvedőket ültettek egy órán keresztül, lógó alsó végtagokkal. A vizsgálat kezdetén és azt követően negyedóránként vért vettek a vena saphena magnájukból, amiben a fehérvérsejtszámot vizsgálták. Azt találták, hogy míg egészséges vénás keringésű egyéneknél a fehérvérsejtszám a vizsgálat végére a kiindulási értékhez képest mintegy 5%-kal csökkent, addig a krónikus vénás keringési elégtelenségben szenvedőknél a fehérvérsejtszámcsökkenés megközelítette a 30%-ot.
A kapillárisokban lelassult áramlás kedvez a fehérvér-sejt-csapda jelenség kialakulásának, amit nagyon szellemes kísérlettel igazoltak. Egészséges egyéneket és krónikus vénás keringési elégtelenségben szenvedőket ültettek egy órán keresztül, lógó alsó végtagokkal. A vizsgálat kezdetén és azt követően negyedóránként vért vettek a vena saphena magnájukból, amiben a fehérvérsejtszámot vizsgálták. Azt találták, hogy míg egészséges vénás keringésű egyéneknél a fehérvérsejtszám a vizsgálat végére a kiindulási értékhez képest mintegy 5%-kal csökkent, addig a krónikus vénás keringési elégtelenségben szenvedőknél a fehérvérsejtszámcsökkenés megközelítette a 30%-ot.
Önmagában a keringésben rekedő, a kapillárisok átmérőjéhez közeli méretű fehérvérsejtek mechanikus keringési akadályt képezve is képesek a mögöttes területeken hipoxiát okozni. Másrészt azonban a mikrocirkulációban rekedt leukociták és az érfalat borító endothelsejtek szoros kapcsolatba is lépnek egymással. Ehhez az endothelsejtek felszínén lévő, úgynevezett sejtadhéziós molekulákra (Cell Adhesion Molecule - CAM) van szükség. A fehérvérsejtek a posztkapilláris venulák területén tapadnak ki az endothelsejtekhez. Ezzel egy folyamat indul meg, a leukociták már nem sodródnak a keringéssel, hanem lassan gördülni kezdenek az érfal belfelszínén. Ezután lelapulnak az endothelhez, és végül az endothelsejtek között átbújnak a szövetekbe. Eközben a leukociták aktiválódnak. Lizoszómáikból aktív proteolitikus enzimek, szabadgyökök szabadulnak ki, és ezek károsítják a kapilláris bazálmembránját. A szintén szabaddá váló kemotaktikus faktorok további granulocitákat vonzanak az adott területre. Ez tovább fokozza a plazmaproteinek és a fibrinogén környező szövetekbe történő kiáramlását. Mindezek a folyamatok összességében hipoxiához, a szövetekben kialakuló steril gyulladáshoz és szövetroncsolódáshoz vezetnek. A gyulladásos kaszkádban az aktivált endotheliumon és leukocitákon kívül hízósejtek, makrofágok és fibroblasztok is részt vesznek, amelyek nagy mennyiségű gyulladásos mediátor és metabolit, sejtadhéziós molekulák, növekedési faktorok és kemotaktikus anyagok előállításával elsősorban az extracelluláris mátrix és parenchimasejtek ellen fordulnak. Ez a gyulladásos elmélet kiegészíti a vénás eredetű ulcus cruris kialakulásának trophicus szemléletét.
A vénás nyomás emelkedésében jelentős szerepet játszik a vénabillentyűk komplett záródási képességének elvesztése. A vénabillentyű inszufficiencia két mechanizmussal jöhet létre. Az egyik, hogy a billentyűk egyik vagy mindkét vitorlája megrövidül, esetleg perforálhat is. A másik lehetséges mechanizmus a vénafal tágulása, ebben az esetben az egymástól eltávolodó, egészséges billentyűk nem képesek megfelelően lezárni a véna lumenét.
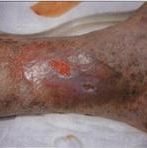
Vannak arra utaló bizonyítékok, hogy a fenti gyulladásos reakciók nemcsak a teljesen kifejlődött krónikus vénás keringési elégtelenségben vannak jelen, hanem a primer vénás diszfunkció kialakulásában is szerepet játszhatnak, és trigger-mechanizmusként szerepelnek a vénabillentyű-destrukció létrejöttében is. Ezt bizonyítja az is, hogy a vena saphena magna inszufficiens billentyűiben monocita infiltrációt mutattak ki. Ez azt is jelentheti, hogy a vénás betegségek egy részében a kiváltó ok az ismertetett aszeptikus gyulladásos reakció is lehet. A gyulladásos reakció bizonyítéka a krónikus vénás keringési elégtelenség késői stádiumában kialakuló lipodermatosclerosis is (1. ábra). Az érintett bőrterületen szövettanilag a dermis papilláris plexusainak perivasculáris infiltrációja mutatható ki.
A mikrocirkulációban bekövetkező elváltozások ismertetése kapcsán azt sem szabad elfelejtenünk, hogy ezen a szinten károsodik az artériás és a nyirokkeringés is.
A vénás keringési zavarok bázisterápiája jelenleg is a kompressziós kezelés és lehetőség esetén a műtéti beavatkozás. Emellett nagyon sok beteg kap valamilyen adjuváns gyógyszeres terápiát is. Főként azért, mert melegben a kompressziós harisnyák vagy rugalmas pólyák viselése a betegek számára elviselhetetlen, néha a beteg nem kívánja a műtétet vagy az operáció elvégzésének az esetleges kísérő-betegségek miatt nagy a kockázata. Az erre a célra alkalmazott szerek többsége valamilyen növényi eredetű hatóanyag-keveréket tartalmaz. Ezeket, a gyógyszercsoportokat ipari méretekben főként a hatvanas-hetvenes években kezdték előállítani és forgalmazni.
A hazánkban eddig forgalomban lévő és jól ismert, természetes, illetve félszintetikus flavonoid-származékokat tartalmazó gyógyszerek (Detralex, Venoruton, Endotelon) mellé felsorakozott a kémiailag más jellegű, triterpén szaponinokat (főként eszcint) tartalmazó vadgesztenyemag-kivonat, a Venastat is.
A flavonoidok rendkívül elterjedtek a növényvilágban és bőségesen kerülnek az emberi táplálékokba is. Több ezer származékuk ismert, kutatásuk hosszú múltra tekint vissza. Hatásmechanizmusukra általában jellemző, hogy fokozzák a vénás tónust és a nyirokáramlást. Csökkentik az erek hiperpermeabilitását és növelik a kapilláris-rezisztenciát. Befolyásolják a leukociták és az endothelsejtek közti kapcsolatot. Gátolják a fehérvérsejtek adhézióját és migrációját, a gyulladásos mediátorok felszabadulását és hatását, ezáltal anti-inflammatorikus hatásuk is van.
A vadgesztenyemag-kivonatok hatásában, azaz a krónikus vénás keringési elégtelenség objektív és szubjektív tüneteinek enyhítésében a központi szerepet triterpén típusú szaponinglikozid tartalomnak, ezen belül is az eszcinnek tulajdonítják. A hazánkban is forgalomba került Venastat retard kapszulában lévő szárított vadgesztenyemag-kivonat tömege 240,0-290,0 mg, amely 50 mg eszcinnek felel meg. Az eszein kémiailag maga sem egységes, hanem nagyon hasonló szerkezetű vegyületek keverékéből áll. Jóllehet a vadgesztenyemag-kivonatok klinikai javallatai már évtizedekkel ezelőtt kialakultak, a hatásmechanizmus preklinikai magyarázatára és a hatékonyság klinikai igazolására egészen napjainkig folytak és folynak vizsgálatok.
Már az 1950-es évek végétől vizsgálni kezdték a venotonizáló hatást, amelyet állatkísérletekben, in vitro és humán vizsgálatokban is kimutattak. Emellett megállapították érpermeabilitást csökkentő, kapilláris filtrációt, gátló hatását, amelyeknek köze lehet a bizonyított gyulladáscsökkentő, valamint szabadgyök-reakciókat és a szabadgyökök által okozott károsodásokat gátló hatásához is. Gátolja továbbá az elasztáz- és hialuronidáz-aktivitást, melyek az endothelium és az extracelluláris mátrix szerkezetét károsítják.
Legújabban, 2002-ben a vadgesztenyemag-kivonatokról megjelent egy Cochrane Áttekintés. A Cochrane áttekintések a bizonyítékokra alapozott orvoslás legjelentősebb dokumentumai közé tartoznak, amelyeket az adott terület kiemelkedő szakértői állítanak össze, előre meghatározott értékelési szempontok szerint, és alapos irodalmazást követően. Az értékelő munka során csak a megfelelő minőségű klinikai vizsgálatok adatait és eredményeit használják fel. Az értékelők szerint általában véve a placebo-kontrollos klinikai vizsgálatok adatai azt mutatják, hogy a vadgesztenyemag-kivonatok javítják a krónikus vénás keringési elégtelenség tüneteit. Hat placebo-kontrollos klinikai vizsgálat értékelte a lábfájdalmat, és ezekben a vadgesztenyemag-kivonat a placebóhoz képest szignifikáns mértékű enyhülést idézett elő. A Cochrane Áttekintés megjegyzi továbbá, hogy az esetleges mellékhatások, mint például a hányinger, a gyomorpanaszok és a bőrviszketés rendszerint enyhék és ritkák. A végkövetkeztetés szerint az eddig rendelkezésre álló bizonyítékok alapján a vadgesztenyemag-kivonat hatékony és biztonságos rövidtávú kezelést jelent. Ugyanakkor a szak-irodalomban - vélhetően a különböző, egymással nem bio-ekvivalens készítmények alkalmazása miatt - számos ellent-mondás is található, így további jól tervezett, randomizált klinikai vizsgálatok is szükségesek e terápiás lehetőség hatékonyságának értékelésére. Fontos megjegyezni, hogy a vadgesztenyemag-kivonat az előny/kockázat gondos mérlegelése után terhességben is javasolható. Ezidáig humán embriotoxikus/teratogén hatást nem észleltek.
A fentiek ismeretében elmondható, hogy a vadgesztenye magjából kivont, eszcint tartalmazó, recept nélkül kapható készítménnyel a kompressziós kezelést nem vagy nem megfelelően alkalmazó, rossz compliance-ű betegeknél, valamint funkcionális panaszok (vénás betegségre utaló tünetek megléte mellett nincs jelentős vénabillentyű-elégtelenség) esetén kúraszerű alkalmazás mellett a szubjektív panaszok javulása érhető el. A gyógyszer jól tolerálható, az elvégzett klinikai vizsgálatok során nem tapasztaltak súlyos mellékhatást.
Irodalom
- Kökény Z.: A visszérbetegség mint fokozatosan kifejlődő kór-kép, amely a legkorábbi stádiumtól kezdve a lábszárfekély esetén is gyógyszeresen is kezelendő. Érbetegségek, XI. évf., 2004/3.: 46.
- Kökény Z.: A krónikus vénás elégtelenség és a lábszárfekély gyógyszeres kezelése. Érbetegség, IX. évf.., 2002/4.: 42.
- Pécsvárady Zs.: Vénás betegségek: felületes thrombophlebitis, mélyvénás thrombosis, krónikus vénás elégtelenség. In: Vascularis medicina, Therapia Kiadó, 2004., szerk. Meskó Éva.
- Steins, A., Jünger, M., Zuder, D., Rassner, G.: Microcirculation in venous leg ulcers during healing: prognostic impact. Wounds, 11(1): 6-12., 1999.
- Greenwood, J. E., Edwards, A. T., McCollum, C. N.: The possible role of ischemia reperfusion in the pathogenesis of chronic venous ulceration. Wounds, 7(6): 211-19., 1995.
- Stücker, M., Schöbe, M. C., Hoffmann, K., Schultz-Ehrenburg, U.: Cutaneous microcirculation in skin lesions associated with chronic venous insufficiency. Dermatol. Surg., 21: 877-882., 1995.
- Bauersachs, J., Fleming, 1., Busse, R.: Pathophysiology of chronic venous insufficiency. Phlebology, II: 16-22., 1996.
- Ono, T., Bergan, J. J., Schmid-Schönbein, G. W.: Monocyte infiltration into venous valves. J. Vase. Surg., 27: 158-66., 1998.
- Pittler, M. H., Ernst, E.: Horse-chestnut seed extract for chronic venous insufficiency. Arch. Dermatol., 134: 1356-60., 1998.
- Maessen-Visch, M. B., Sommer, A., De Paepe, J. A., Neumann, H. A. M.: Changes in microcirculation in patients with atrophie blanche visualized by laser Doppler perfusion imaging and transcutaneous oxygen measurements. Phlebology, 13: 45-49., 1998.
- Bogs, U., Bremer, D.: Ober Rosskastaniensamen und daraus hergestellte Auszüge. Pharmacie, 26(7): 410., 1971.
- Hippocastani semen (Rosskastaniensamen) Trockenextrakt (DAB) aus Rosskastaniensamen. Banz., Nr. 71., Vol. 15., 4.,1994.
- Venastat retard kapszula alkalmazási előírás. OGYI-eng. száma: 19992/40/2002.
- Bisler, H., Pfeifer, R., Klüken, N., Pauschinger, P.: Wirkung von Rosskastaniensamenextrakt auf die transkapillüre Filtration bei chronischer venöser lnsuffizienz. Dtsch. Med. Wschr., 111: 1321., 1986.
- Rudolfsky, G., Neiss, A., Otto, K., Seibel, K.: Ödemprotektive Wirkung und klinische Wirksamkeit von Rosskastanienextrakt im Doppelblindversuch. Phlebol. Protokol., 15: 47., 1986.
- Hitzenberger, G.: Die therapeutische Wirksamkeit des Rosskastanienextraktes. Wien. Med. Wochenschr., 17: 385., 1989.
Érbetegségek: 2005/2. 63-65. oldal


