A szerző saját kutatási eredményeik alapján foglalja össze az artériás stiffness meghatározásával kapcsolatos megfigyeléseit. A szisztémás autoimmun betegségekben, a vesetranszplantáció során, a perifériás érbetegek diagnosztikájában illetve longitudinális jelleggel a primer antifoszfolipid szindrómában vizsgálták meg az oszcillometriás módszerrel mért pulzushullám terjedési sebesség és augmentációs index értékeket. A stiffness paramétereket előzetesen összevetették az endothel dependens vazodilatáció és az artéria carotis intima-media vastagság vaszkuláris paraméterekkel. Elvégezték az osz cillometriás módszer és az EKG kapuzott carotisfemoralis pulzushullám terjedési sebesség korrelációs vizsgálatát. A szerző felveti azt a kérdést, hogy e módszer, a számos pozitív vizsgálati eredmény ellenére miért nem nyerte még el az ajánlás szintű bevezetést a vaszkuláris betegek diagnosztikájába.
Érbetegségek: 2024/1. 15-18. oldal
Bevezetés
Az artériás stiffness mérést 2005-ben vezettük be tanszékünkön. A carotis-femoralis EKG kapuzott ultrahang módszer (foot-to-foot) mellett elérhetővé vált oszcillometriás módszerrel mérhető aorta pulzushullám terjedési sebesség és augmetációs index meghatározás. Első lépésként az volt a célunk, hogy a kutatásokban rutinszerűen használt endotheldependens úgynevezett flow-mediált vazodilatációt, és az artéria carotis intima-media vastagságot, mint angiológiai paramétereket korreláltassuk az artériás stiffness értékekkel (1. és 2. ábra).
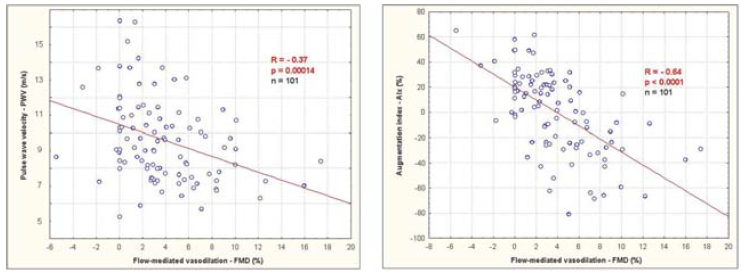
1. ábra.
Angiológiai módszerek adatainak összevetése I.
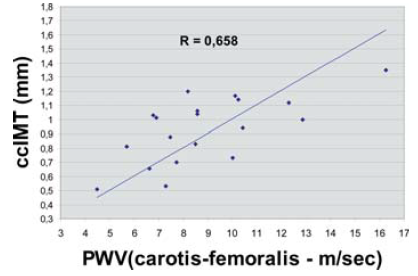
2. ábra.
Angiológiai módszerek adatainak összevetése II.
101 beteg adatait feldolgozva jó korrelációt találtunk a pulzushullám terjedési sebesség és a flow-mediált vazodilatáció között, valamint kiváló összefüggést kaptunk az augmentációs index és a flow-mediált vazodilatáció között is. Természetesen összehasonlítottuk a carotis-femoralis EKG kapuzott ultrahangos módszerrel mért aorta pulzushullám terjedési sebességeket és az oszcillometriás módszerrel kapott eredményeket is, ahol szintén jó összefüggést találtunk, melyet a 3. ábrán mutatunk be (1).
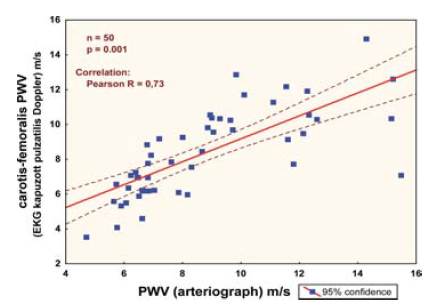
3. ábra.
Arteriograph és EKG - kapuzott ultrahangos mérőmódszerek összehasonlítása a pulzushullám terjedési sebesség mérésében.
A fenti eredmények feljogosítottak arra, hogy a vizsgálatokat nagyobb számú esetre kiterjesszük. Első lépésként 277 autoimmun beteg vizsgálatát végeztük el. A betegcsoportok a következők voltak: szisztémás lupus erythematosus, rheumatoid arthritis, Sjögren-szindróma, primer antifoszfolipid szindróma, progresszív szisztémás szklerózis, kevert kötőszöveti betegség és nem differenciált kollagenózis. A mérési eredményeket korban, nemben és Framingham-i rizikótényezőkre nézve azonos kontroll csoporttal hasonlítottuk össze. A meghatározott angiológiai paraméterek tehát a következők voltak: flow-mediált vazodilatáció, nitrát-mediált vazodilatáció, artéria carotis intima-media vastagság, aorta pulzushullám terjedési sebesség és augmentációs index. Az eredményeket az 1. táblázatban foglaljuk össze. Betegcsoportok közül a primer antifoszfolipid szindróma és a progresszív szisztémás szklerózis megbetegedések emelhetők ki abból a szem - pontból, hogy itt találtuk legrosszabbnak az endothel funkciót és a megnövekedett artériás stiffness paramétereket. Mindkét betegcsoportot további analízisnek vetettük alá (2).
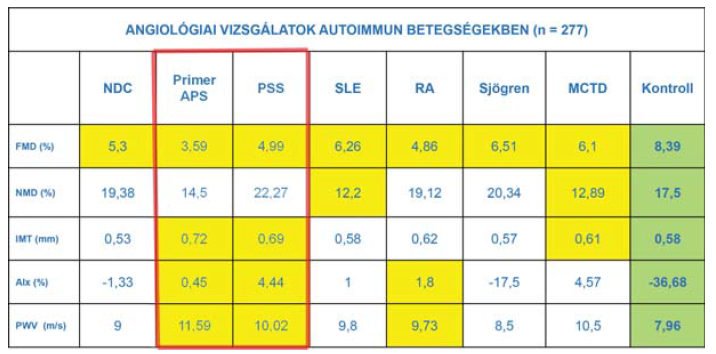
1. táblázat.
Szisztémás autoimmun betegek angiológiai vizsgálati eredményei.
Primer antifoszfolipid szindrómában az angiológiai eltéréseket összevetettük immuno-inflammatórikus eltérésekkel, mely utóbbiakat a perifériás vérből határoztunk meg. A pulzushullám terjedési sebesség és az augmentációs index pozitívan korrelált az Interleukin-4 szint emelkedéssel. Intracelluláris citokin expressziós vizsgálatokat végezve a pulzushullám terjedési sebesség javuló tendenciát mutatott az IL-10 pozitív, CD 8 pozitív sejtek arányával, valamint ezzel ellentétben rosszabbodást mutatott a CD 8 populáció IL-10 negatív alcsoportjával (3). A progresszív szisztémás szklerózis egy fokozott fibrózissal járó megbetegedés, amelynek kardiális és vaszkuláris manifesztációja is van. Az erek fibrotikus folyamatát jellemző fokozott artériás merevséget jól lehet detektálni a megnövekedett aorta pulzushullám terjedési sebességgel és a korai szisztolés reflexhullám augmentációjával. Az eredményeket a 4. ábrán tüntettük fel (4). 16 Érbetegségek,
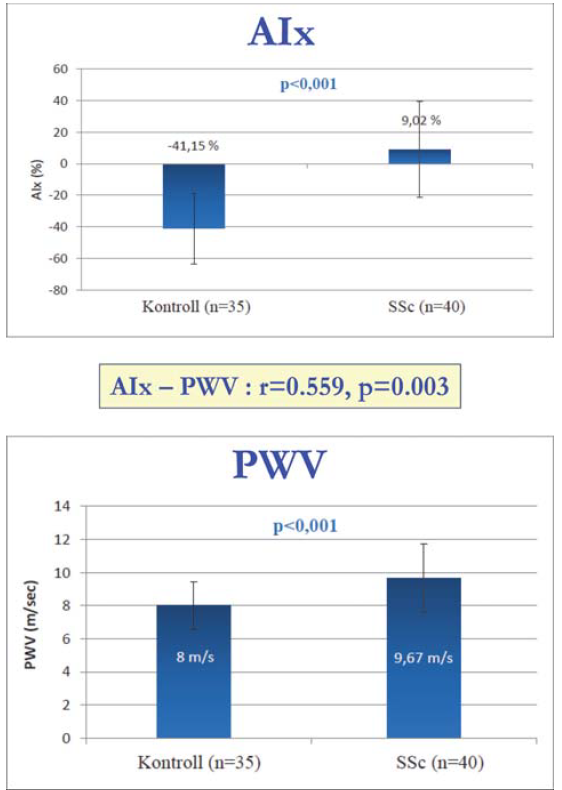
4. ábra.
Stiffness paraméterek progresszív szisztémás szklerózisban.
A rheumatoid arthritis egy kiváló lehetőség volt arra, hogy a biológiai terápiák angiológiai paraméterekre kifejtett hatását megfigyeljük. A számos vizsgálat közül kiemelhető, hogy a 24 hetes adalimumab kezelés szignifikánsan javította az aorta pulzushullám terjedési sebességet, miközben az artéria carotis intima-media vastagság nem változott (5. ábra) (5).
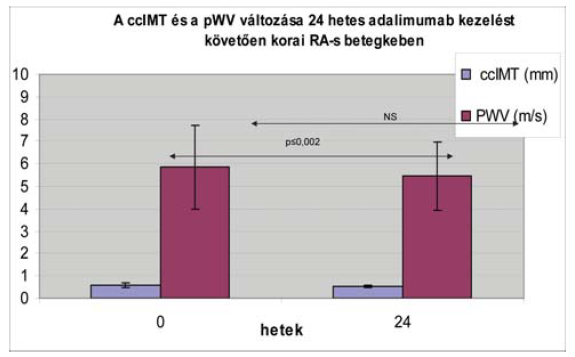
5. ábra.
Biológiai terápia hatása a pulzushullám terjedési sebességre rheumatoid arthritisben.
A végstádiumú vesebetegség kardiovaszkuláris hatásai közismertek a megnövekedett morbiditási és mortalitási adatok alapján. Joggal merül fel a kérdés, hogy pozitív hatást hoz-e az artériás stiffness paraméterek vonatkozásában a sikeres vesetranszplantáció. Jelenleg ezzel egy rövid távú követéses vizsgálatot folytatunk, amely mind az aorta pulzushullám sebesség, mind az augmentációs index egyértelmű javulását igazolta a postoperatív időszakban (6. ábra) (6).
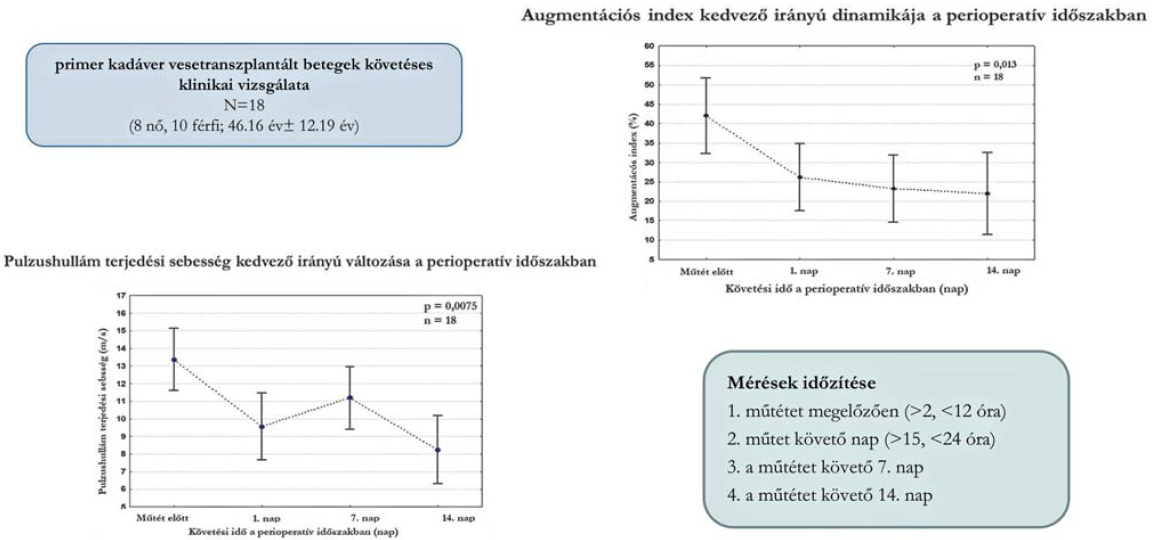
6. ábra.
Stiffness paraméterek változása vesetranszplantáció után.
A fenti vizsgálatok keresztmetszeti vagy rövidtávú vizsgálatok voltak. 2005-ben elindítottunk egy longitudinális követéses vizsgálatot primer antifoszfolipid szindrómában, azzal a céllal, hogy: 1. hogyan változnak az angiológiai paraméterek és az antitest profil a követés során, 2. a kiinduláskor mért angiológia paraméterek jeleznek-e, bírnak-e prediktív értékkel egy későbbi thromboemboliás esemény bekövetkezését illetően. Összesen 26 beteget volt alkalmunk követni oly módon, hogy 10 év elteltével újra tudtuk mérni az angiológiai paramétereket és a követett 10 év klinikumának ismeretében összefüggést kereshettünk a kiindulási angiológiai paraméterek és a bekövetkezett thromboemboliás események között. 16 betegnél thrombotikus esemény nem zajlott le, míg 10 betegnél volt thromboemboliás szövődmény a vizsgált 10 év alatt. Természetesen a betegek a követés során adekvát antithrombotikus kezelésben részesültek. Nem találtunk szignifikáns összefüggést a kiindulási angiológiai para - méterek károsodása és a bekövetkezett thromboemboliás események között. A 10 év alatt a thrombotikus eseményre nézve pozitív betegek között egyedül az artéria carotis intima-media vastagság szignifikáns növekedését észleltük (7. ábra)(7).
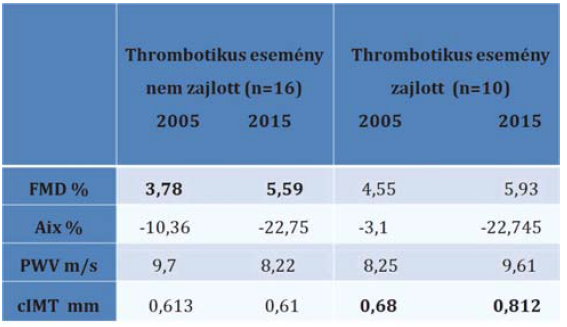
7. ábra.
Angiológiai paraméterek változása a trombo - emboliás klinikum tükrében. 10 éves követéses vizsgálat.
A neurológia klinikával közös angiológiai vizsgálati és gondozási rendszert alakítottunk ki, ahol a cerebro - vaszkuláris gondozás és a perifériás érbeteg kivizsgálás valamint gondozás egyidejűleg megtörtént. Abból a célból fejlesztettük ki ezt a modellt, hogy egyfelől felhívjuk a figyelmet ezen betegcsoportokban a komplex vaszkuláris kivizsgálás szükségességére, valamint leteszteljük az artériás stiffness paraméterek viselkedését az egyes izolált, valamint komplex érbeteg csoportokban. Ezen úgynevezett Auguszta Vascularis Program az alsó végtagi perifériás artériás érbetegség domináló hatását igazolta a károsodott artériás stiffness paraméterekre. A csak kardiovaszkuláris rizikóbetegségben szenvedők esetében normálisnak mértük a stiffness paramétereket, izolált cerebrovaszkuláris betegség esetén egy mérsékelt augmentációs index növekedést tapasztaltunk, egyértelműen kóros pulzushullám terjedési sebesség és augmentációs index csak perifériás érbetegség jelenléte esetén volt tetten érhető, ezekben a beteg - csoportban (8. ábra) (1).
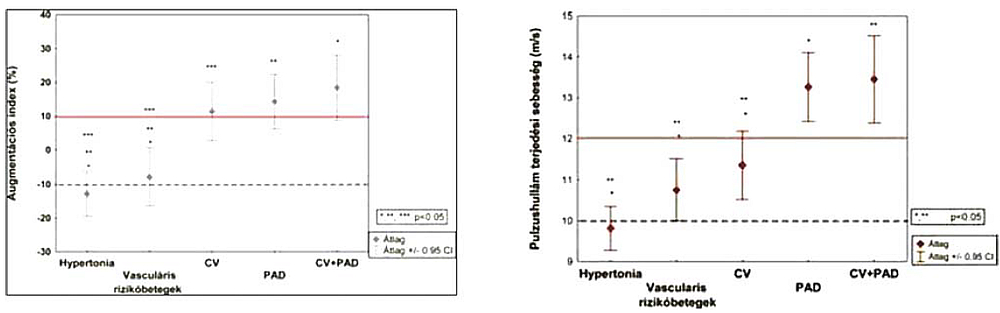
8. ábra.
Kardiovaszkuláris manifesztációk és az artériás stiffness kapcsolata (Auguszta Vascularis program).
A fenti eredmények összegzik azokat a sikereket, amiket elértünk az artériás stiffness vizsgálatokkal. A módszert alkalmasnak találtuk bizonyos autoimmun patomechanizmusú vasculopathiák detektálására, valamint ígéretes eredmények mutatkoztak a vesetranszplantáció pozitív hatásának követésére is. Figyelmet érdemlő a károsodott artériás stiffness és az alsó végtagi perifériás érbetegség kapcsolata is. Ha ez így van, mi magyarázza a címben szereplő csalódásokat az artériás stiffnessnek a klinikai diagnosztikában való használhatóságát illetően? A kérdés jogosságát fokozza az a tény, hogy a nemzetközi irodalom is magas impakt faktorú közleményekben fogad el kísérletes eredményeket ezzel kapcsolatban. Ennek ellenére jelenleg nem tudunk olyan nemzetközi ajánlást idézni, amely megadná azt a kardiovaszkuláris klinikai indikációs pontot, ahol javasolja az artériás stiffness meghatározását akár diagnosztikus, akár terápiás célból. Átmenetileg ugyan bekerült az Európai Hypertonia ajánlásba, mint célszervkárosodást jelző paraméter, de később kikerült az ajánlásból. Igazság szerint nem is olyan könnyű megmondani, hogy a háziorvosi, kardiológiai vagy az angiológiai betegellátási gyakorlatban mi az a pont, ahol diagnosztikus, vagy a terápia meghatározása céljából javasolnánk, hogy történjen meg egy aorta pulzushullám terjedési sebesség vagy például egy augmentációs index meghatározás. Mindezek alapján úgy érzem, hogy ez egy olyan nyitott kérdés a kardiovaszkuláris diagnosztikában és ellátásban, amely további vizsgálatokat indokol. Tekintettel arra, hogy bőségében vagyunk keresztmetszeti klinikai vizsgálatoknak, az igazi továbblépést a longitudinális prospektív vizsgálatok jelentenék, azaz annak meg - határozása, hogy egyes klinikai szituációkban milyen prediktív értékkel bír az artériás stiffness mérése. Ezek alapján meghatározható lenne, hogy a mindennapi gyakorlatban mikor érdemes a mérést elvégezni és fel lehetne tenni a kérdést a tisztázandó terápiás konzek - venciákra is.
Irodalom
- Laczik R. és mtsai. Perifériás érbetegek és stroke-ot elszenvedett betegek komplex angiológiai vizsgálata és gondozási folyamata. Érbetegségek / Hungarian Journal of Vascular Diseases (1218-3636) 2012; 19(2), 31:38.
- Soltész P. et al.A comparative study of arterial stiffness, flow-mediated vasodilation of brachial artery, and the thickness of the carotid artery intima-media in patients with systemic autoimmune diseases. Clin. Rheum. 2009; 28(6) 655:662.
- Dér H. et al. Rheumatol.(Oxford) 2008; 47(11) 1628:1634.
- Timár O. et al. Increased arterial stiffness as the marker of vascular involvement in systemic sclerosis. J. Rheumatol. 2008; 35(7):1329:1333.
- Kerekes Gy. et al. Effects of biologics on vascular function and atherosclerosis associated with rheumatoid arthritis. Ann. N. Y. Acad. Sci. 2009; 1173, 814:821.
- Kovács D. et al. Transplant. Proc. 2011; 43(4)1252:253.
- Veres K. et al. .Lupus. 2010; 19(13)1520:1526.
Írta: Soltész Pál
Debreceni Egyetem, Klinikai Központ
II. Belgyógyászati Klinika,
Angiológiai részleg,
Ez az e-mail-cím a szpemrobotok elleni védelem alatt áll. Megtekintéséhez engedélyeznie kell a JavaScript használatát.
Érbetegségek: 2024/1. 15-18. oldal


