A szerzők micro- és macroangiopathiás diabetes mellitusban szenvedő betegek echocardiographiás vizsgálattal nyert haemodinamikai paramétereinek összehasonlító vizsgálatát végzik el. Ennek során a diabeteses szövődmények hatásain túl a tartósan alkalmazott inzulin, illetve sulfonylurea therapia haemodinamikai hatását is értékelik. Mieroangiopathias szövődmények fennállása esetén a perifériás ellenállás (ESMWS) csökkenésével összefüggésben szignifikáns módon növekszik a frakcionálja roströvidülés (FS) és a circum-ferentialis roströvidülés (CRS) értéke. Maeroangiopathiában a változások ellentétes irányúak. A perifériás ellenállást (ESMWS) és a balkamrai ejectiós időt (LVET) az inzulin, illetve a sulfonylurea kezelés ellentétesen befolyásolja. Az izovolumiás relaxációs időt mind a szövődmények, műid az antidiabetikus kezelés rontja. Szövődmények fennállásakor a szénhidrát anyagcsere rendezése során a hosszú távra tervezett kezelés haemodinamikai hatására is figyelemmel kell lennünk.
Érbetegségek: 1996/4. - 5-11. oldal
KULCSSZAVAK
diabetes mellitus, echocardiográfia, haemodinamika, mikroangiopátia
A diabetes mellitusban (DM) szenvedő betegek micro- és macrovascularis szövődményei mind a morbiditásban, mind a mortalitásban jelentős szerepet játszanak. A Joslin Klinika felmérése szerint az inzulin felfedezése előtti periódusban a cardiovascularis szövődmények a halálozások csupán 20%- áért feleltek (1). Mivel az inzulin-therapia bevezetése radikálisan csökkentette az acut ketoacidotikus halálozási arányt, így már az 1960-as évekre kikristályosodott, hogy a cardiovascularis halálozás milyen nagy számban fordul elő DM betegek körében (1, 2, 3). Szinte a mai napig érvényes az a megfigyelés, mely szerint a diabeteses halálozás mintegy 75%-ának hátterében cardiovascularis szövődmény áll. Ez vezetett arra, hogy a 60-as, 70-es évektől kezdődően keresik az összefüggéseket a diabetes mellitus és szövődményei, a micro-, illetve macrovascularis érintettség között, kutatják a klinikai, illetve szövettani megjelenést (1, 2, 4), a patomechanizmust, az utóbbi években pedig a biokémiai, élettani összefüggéseket is (5). Szervi lokalizációt tekintve mind a nucroangiopathia, mind az angiosclerosis vonatkozásában a szív és a perifériás keringés is érintett lehet. Az ezt vizsgáló klinikai tanulmányok alapján beszélünk ma a diabeteses cardiomyopathia fogalmáról (4), illetve arról a tényről, hogy az atherosclerosis és a coronariasclerosis ac- celerált, súlyosabb és kiterjedtebb formában van jelen diabeteses betegek szervezetében (3, 7). A kóros szénhidrát anyagcsere, mint önálló rizikófaktor hátrányos haemodina- mikai hatásai noninvasív vizsgálatokkal - EKG. mechano, terhelés, echo, izotóp - jól követhetők (8, 9, 10, 11, 12). Újabban az alkalmazott inzulin, illetve sulfonylurea (SU) therapia haemodinamikai hatását is felvetik (33, 34, 35, 36).
Vizsgálatunk célja
Célunk DM micro-, valamint micro- és macroangiopathiával rendelkező betegcsoport direkt mért noninvasív és számított haemodinamikai paramétereinek összehasonlító vizsgálata volt. Azt is értékelni kívántuk, hogy a krónikusan alkalmazott orális sulfonylurea vagy inzulin therapia lehet-e hatással a vizsgált haemodinamikai paraméterekre.
Betegek
Vizsgálatunkba 43 beteget vontunk be, akik közül 29 nő, 14 férfi volt. 18 kontroll személy paramétereit értékeltük (részben egészséges, részben csökkent glucose tolarenciával bíró, de érszövődménnyel nem rendelkező). A betegek közül 12 csak diabeteses microangiopathiában szenvedett (retinopathia és/vagy nephropathia és/vagy neuropathia), 13 fő a microangiopathia mellett macroangiopathiában szenvedett még (coronariabetegség és/vagy carotis betegség és/vagy hypertonia és/vagy obliteratív perifériás érbetegség és microangiopathia). A kontroll betegek átlag életkora 36+/-12 év, inzulinnal kezelt betegeké 37+/-13 év, sulfonylureaval kezelt betegeké 48+/-6 év volt.
Módszer
A microangiopathia jelenlétét rutin klinikai - fundus kép, microalbuminuria, illetve organikus és autonóm neuropathia - vizsgálatokkal igazoltuk. Macroangiopathia bizonyítására terheléses ergometriás vizsgálatot, perifériás erek doppler vizsgálatát, carotis doppler vizsgálatot végeztünk.
Hitachi EUB echocardiographon 5 perces ágynyugalmat követően, típusos (csúcsi, négyüregi, parasternalis) pozícióból, EKG rögzítéssel párhuzamosan végeztük méréseinket. Ennek során vizsgáltuk a végdiastoles és végsystoles átmérőt (EDD, ESD) a hátsófal (HF) és septum (IVS) vastagságát, a frakcionalis roströvidülést (FS) és circumferencialis roströvidülést (CRS), perctérfogatot (cardiac output = CO), a szívindexet (cardiac indexet = Cl), ejekciós frakciót (EF), a balkamrai lassú és gyors telődés arányát (A/E), a balkamrai nyomásfeleződési időt (PHT), systolera és diastolera jellemző időintervallumokat: preejekciós periódust (PEP), frekvenciára korrigált preejekciós időt (PEPi), ejekciós időt (LVET, PEP/LVET), isovolumiás relaxációs időt (IVRT). A rendelkezésünkre álló adatokból számítottuk a perifériás ellenállásból származó, fali stresszre utaló paramétert (ESMWS), valamint a halkamra tömegét (LV mass), a szívfrekvenciát (fr), valamint az EKG görbe alapján a szum- mációs R hullámot (R) (1. táblázat).

1. táblázat.
Vizsgált paraméterek.
Statisztikai analízis
Az értékelést egy, illetve két tényezős variancia analízis- 2 sel, chi teszttel végeztük.
Eredmények
Értékelésünket - a fenti statisztikai módszerek felhasználásával - először a diabeteses érszövődményekkel való összefüggésben, majd a therápiás hatásokra való figyelemmel végeztük el.
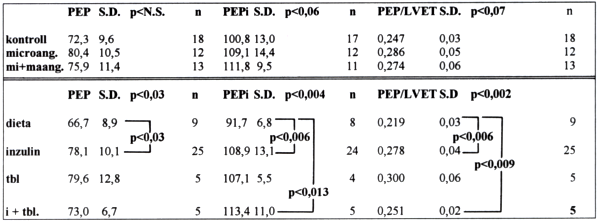
2. táblázat.
Preejekciós intervallumok szövődmény és therapia szerinti megoszlása. Rövidítések: microang. = microangiopathia, mi + maang. = micro- és macroangiopathia, tbl. = orális antidiabtikummal kezelt betegek csoportja, i + tbl. = egyidejűleg alkalmazott inzulin és orális antidiabetikum.
Eredményeinket a 2-4. táblázatokban foglaljuk össze. A bal kamra tömege a macroangiopathiás csoportban (LV mass=28,3 S.D. 3,9 n=13) szignifikánsan magasabb volt mind a kontroll (LV mass=23,98 S.D. 3,1 n=18 p<0,05), mind a microangiopathiás (LV mass=24,l S.D.3,4 n=12 pp<0,02) csoporthoz képest, ebbe a csoportba lényegesen több hypertomas beteg tartozott. Ugyanakkor a balkamrai volumenre utaló summatiós R hullám a microangiopathiás csoportban (R=18,4 mm S.D.3,5 n=ll) bizonyult nagyobbnak a kontrollhoz képest. Bár ez az érték nem mutat szignifikáns különbséget sem a kontroll (R=16,6 mm S.D. 16,1 n=16, pp<N.S.), sem az egyidejűleg macroangiopathiás szövődménnyel is bíró (R=16,5mm S.D.3,7 n=13, pp<N.S.) csoporthoz képest, mindenképpen utal a microangiopathiás csoportban fennálló hyperkinezissel kapcsolatos balkamrai volumenterhelésre. A microangiopathiás csoportban észlelt magasabb nyugalmi frekvenciaérték (fr) megközelíti a szignifikancia határát, melyben szerepe van az ebben a csoportban nagy számban eló'forduló neuropathiás szövődménynek is, ez utóbbi azonban jelenleg nem képezte külön vizsgálatunk tárgyát. A systoles funkció változása ellentétes irányú az eltérő szövődménnyel érintett csoportokban. Microangiopathiában az ejectiós frakció (EF=67,6% S.D.7,69 n=12) értéke növekszik, míg a macroangiopathiával érintett csoportban a microangiopathia jelenlététől függetlenül csökken (EF=56,4% S.D.10,4 n=13). Ha a macroangiopathiás csoportot a csupán microangiopathiában szenvedő csoporthoz hasonlítjuk, akkor különösen szembeötlő a különbség (- 11,1% pp<0,005), mely a macroangiopathiás csoportban megnövekedett perifériás ellenállás (ESMWS=111,4 dyn/cm ) következményének tulajdonítható. A hátsófal végsystoles átmérőhöz viszonyított vastagsága microangiopathiás csoportban (HF/ESD=0,47% S.D. 0,12 n=12) a kontrollhoz képest (HF/ESD=0,34% S.D.0,67 n=17) szignifikáns módon nagyobb (pp<0,002), azonban ez macroangiopathia jelenlétében nem érvényesült (HF/ESD=0,39 S.D. 0,07 n=13 pp<N.S.) (3/b. táblázat).
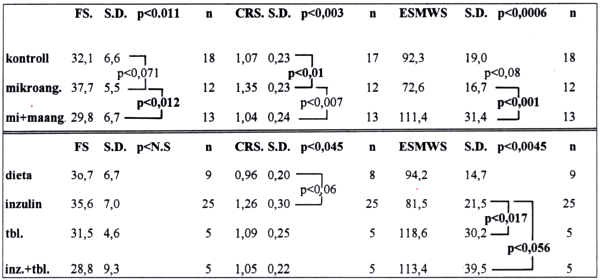
3/a. táblázat.
Systoles paraméterek a szövődmények és a therapia összefüggésében.
Rövidítések: microang. = microangiopathia, mi + maang. = micro- és macroangiopathia,
tbl. = orális antidiabtikummal kezelt betegek csoportja,
i + tbl. = egyidejűleg alkalmazott inzulin és orális antidiabetikum.
A microangiopathiás csoportban a frakcionális roströvidülésben (FS=37,7% S.D.5,5 n=12, p<0,011), illetve a circumferencialis roströvidülésben (CRS=1,35 m/s S.D. 0,23 n=12, <0,01), a várt romlás helyett a kontroll csoport értékeit (FS=32,1 S.D. 6,6 n=18) (CRS=1,07 m/s S.D. 0,23 n=17) meghaladó jó eredményeket kaptunk (p<0,011 p<0,01), melynek oka, hogy - más szerzők által leírtakhoz hasonlóan - ebben a vizsgált csoportban is előfordult 4 db jelentős hyperkinezissel, illetve csökkent perifériás ellenállással bíró fiatal, inzulinnal kezelt beteg. Természetesen ezen betegek paraméterei nem adnak teljes keresztmetszetet az I. típusú DM-ről. A macroangiopathiás szövődménnyel is rendelkező betegeknél a vártnak megfelelően mindkét paraméter (FS=29,9% S.D. 67, n=13, p<N.S. CRS=1,04 m/s S.D. 0,24 n= 13, p<N.S.) értékében a kontrollhoz képest csökkenést észleltünk, azonban a különbség csak a microan-giopathiás csoportban mért paraméterekhez hasonlítva volt szignifikáns (p<0,012, p<0,007) (3/a. táblázat).
A sytoles funkciót jellemző más paraméterekben (PEP, PEPi, PEP/LVET), a szövődményekkel összefüggésben nem találtunk szignifikáns eltérést. Ez utóbbi paraméterek az alkalmazott therapia függvényében bizonyulnak érzékenyebbnek (inzulin PEP/LVET=0,28 S.D. 0,05 n=25 p<0,006, tbl PEP/LVET=0,30 S.D. 0,06 n=5 p<0,009). Szignifikáns eltérés a kontrollhoz képest a PEPi értékben láttunk mind az inzulin, mind pedig a tbl-val folytatott the-rapia esetében is (p<0,006 p<0,013) (2. táblázat). A perifériás ellenállásra, illetve a szívizom terhelésre utaló stresszre (EWMWS), ezzel kapcsolatosan a balkamra hátsó fali kontractióra (HF/ESD) az eltérő módon kezelt csoportok ellentétes módon reagálnak. (3/a. és 3/b. táblázat).
Az inzulinnal kezelt csoportban a perifériás ellenállás a diétával kezelt csoporthoz (ESMWS=94,2 dyn/cm2) képest csökken (81,5 dyn/cm2), míg a sulfonylureaval kezelt csoportban megnövekszik (ESMWS=118,6 dyn/cm2. Bár az analízis a vizsgált csoportok között statisztikailag értékelhető eltérést mutat, ez csupán az eltérő módon kezelt csoportok értékeit egymáshoz hasonlítva látszik szignifikánsnak (inz./tbl p<0,017, mz./inz.+tbl. p<0,056), ezzel is megerősítve az orális sulfonylurea, valamint az inzulin therapia keringésdinamikai hatását.
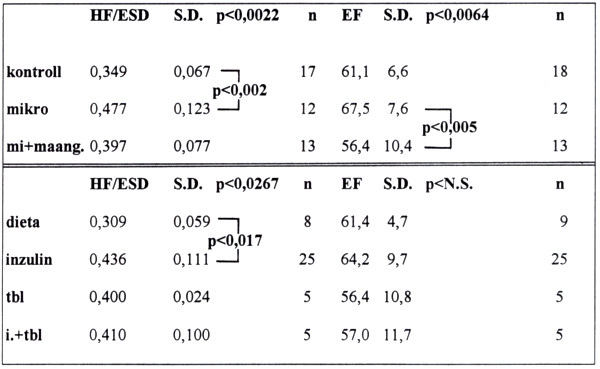
3/b. táblázat.
Systoles paraméterek és szövődmények a therapia függvényében.
Rövidítések: microang. = microangiopathia, mi + maang. = micro- és macroangiopathia
Az isovolumiás relaxációs idő (IVRT), valamint a bal-kamrai kóros diastoles functióra utaló PHT és A/E érték mind a microangiopathias csoportban (IVRT=91,5 msec S.D. 16,1 n=12, PHT=93,9 msec S.D. 25,6 n=10, A/E=0,72 S.D, 0,12 n=9), mind a macroangiopathiaval is érintett csoportban (IVRT=87,8 msec S.D.12,2 n=13, PHT=90,1 msec S.D.15,8 n=ll, A/E=0,65 n=13) megnyúlt. A kontrolitól való eltérés azonban nehezen értékelhető, mivel a kontroll csoport angiológiai szövődménnyel nem bíró, de csökkent glucose tolarenciával rendelkező egyéneket is magában foglalt. Az adatok alapján azonban egyértelmű a kóros CH anyagcsere diastoles funkciót károsító hatása (4. táblázat). Ha az aktuálisan alkalmazott antidiabetikus therapiát vizsgálva értékeljük a relaxációs, illetve diastoles paramétereket, akkor azt tapasztaljuk, hogy a kontroll csoporthoz képest (IVRT=69,6 S.D.9,46 n=9) mind az inzulinnal kezelt csoportban (IVRT=88,9 msec S.D. 14,7 n=25), mind a sul- fonylureaval kezelt csoportban (IVRT=90,5 msec S.D. 7,16 n=5) az isovolumiás relaxációs idő jelentősen, azonos irány-ban változik, szignifikáns módon megnyúlik (p<0,004 p<0,043). A pitvari kontrakció mértékére utaló A/E hánya-dos is hasonlóképpen változik. A kontroll csoporthoz (A/E=0,54 S.D.0,11 n=9) képest az inzulinnal kezelt cso-portban is (A/E=0,72 S.D.0,10 n=22) és a sulfonylureával kezelt csoportban is (A/E=0,75 S.D.0,18 n=5) növekszik. Mindkét esetben a változás mértéke a kontrollhoz képest szignifikánsnak mondható (p<0,002 p<0.012). A balkamrai nyomásfelezési időben a vizsgált csoportok között szignifikáns eltérés nem mutatkozott (4. táblázat).
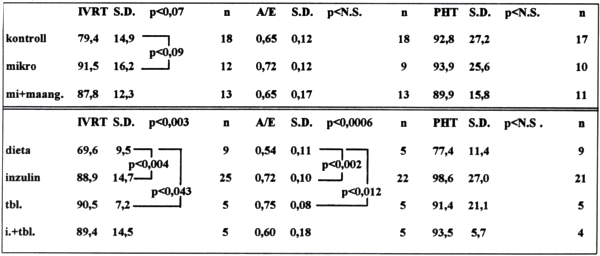
4. táblázat.
Diastoles paraméterek a szövődmények és a therapia függvényében.
Rövidítések: microang. = microangiopathia, mi + maang. = micro- és macroangiopathia,
tbl. = orális antidiabtikummal kezelt betegek csoportja,
i + tbl. = egyidejűleg alkalmazott inzulin és orális antidiabetikum.
Eredményeink összefoglalásaként azt mondhatjuk, hogy korábbi vizsgálatok eredményeivel egyezően a diabeteses micro-, illetve macroangiopathia jelenléte észlelhető mind a systoles, mind a diastoles paraméterekben. Míg a microangiopathiás csoportban szignifikáns módon növekedett a FS, CRS, és csökkent az ESMWS értéke, addig macroangiopathiában ugyancsak szignifikáns módon csökkent a FS, CRS, és növekedett az ESMWS értéke. A perifériás stresszre utaló ESMWS értéket és a balkamrai ejectiós időt (LVET) az inzulin, illetve az orális antidiabetikus therapia ellentétes irányban befolyásolja. Az ejekciós frakció (EF), illetve a HF/ESD tekintetében a microangíopathiás hatás érzékelhetőbb, mindkét paraméter értéke növekszik. Preejectiós paraméterek tekintetében szövődmények hatása statisztikailag nem volt értékelhető. A PEP, PEPi értékek az inzulin therá- piával, míg a legérzékenyebb paraméter, a PEP/LVET érték a sulfonylurea kezeléssel is szoros korrelációt mutat. Mindkét típusú szövődmény fennállásakor azonos irányban változik, növekszik az izovolumiás relaxációs idő (IVRT). A relaxációs paraméterre mindkét therapiának szignifikáns hatása van, hatásuk azonos módon, a paraméter értékét növelve érvényesül. A lassú és gyors telődés arányát vizsgálva hatásuk ugyancsak szignifikánsnak és hasonló irányúnak tekinthető (A/E).
Következtetések, megbeszélés
Mintegy másfél évtizede ismert a balkamra funkció károsodása diabetes mellitusban (18, 19, 20). Az eddigi tanulmányok egy része az I. típusú diabetessel foglalkozik és a balkamra diastoles funkció károsodását a microangiopathiás elváltozás következményének tulajdonítja (13, 14). Más szerzők szerint ezen betegcsoport mintegy egyharmadánál a balkamrai diszfunkció nem hozható összefüggésbe a microangiopathiás szövődménnyel (11, 15, 17, 23). Borrow még a specifikus diabeteses szívizombetegséget mint létező entitást is kétségbe vonta. Diastoles szívizomkárosodással azonban a II. típusú diabetes mellitusban is számolnunk kell (20, 26, 27). A funkciókárosodás hátterében a hyperglikaemiás állapot következtében károsodott myocardialis Ca2+ATP- ase activítast (29, 30), illetve a kimutatható hyperinzulinae- miat (31, 32, 33), valamint a diabetes fennállásának idó'tar- tamát vélték döntő tényezőnek (19, 19). Leírták az inzulin-nal történt anyagcsere rendezés haemodinamikailag is ked-vező hatását (15), mely szerint a II. típusú DM-ban a rossz anyagcsereállapotban észlelt diastoles/systoles funkciózavar reverzibilissé tehető átmeneti inzulinkezeléssel (16, 28). Más szerzők azonban anyagcsere rendezés esetén nem észleltek javulást a károsodott diastoles funkcióban (22.) II. típusú DM esetén, még tartósan kielégítő anyagcsere kontroll esetén is gyorsabb a vascularis status romlása (23, 27). Innen indult el az az elképzelés, hogy a diabetes lefolyásán, időtartamán, illetve a közvetlen anyagcsere hatáson túl az alkalmazott antidiabetikus therapiának is lehetnek haemodi- namikai, noninvasív mérésekkel követhető hatásai. Utóbbi években kísérletes élettani munkák számolnak be a sulfony- lurea készítmények, mint specifikus ATP-dependens K+ csatorna blokkolók extrapancreatogen hatásáról, mely a fiziológiás vasoregulatióban is jelentősséggel bírhat (34). Az inzulinnak korábban leírták már adenyl-cyclase inhibitor tulajdonságát, mely magyarázhatja a perifériás rezisztencia csökkentést. Ismeretes azonban az izomsejtekre kifejtett proliferatív hatása is (32, 33).
Szerzők fenti klinikai vizsgálatukban, noninvasív módon nyert haemodinamikai parameterek statisztikai összehasonlító vizsgálatával bizonyítottnak vélik, hogy a microangio- pathia jelenléte a szívizomban noninvasív módon mérhető, az echocardiographiás vizsgálattal a későbbiekben követhető. Az alkalmazott antidiabetikus therapia haemodinamikai hatásai is követéses vizsgálatokkal észlelhetővé, értékelhetővé válnak. A kóros szénhidrát anyagcsere, illetve az alkalmazott antidiabetikus therapia a szívcikluson belül más és más paramétereket befolyásolnak. Mindezek a SU-k szívben és a perifériás érrendszerben nagy számban jelenlévő, a vasoregulatióban fontos szereppel bíró ATP-dependens K+ csatornákra gyakorolt hatásával, illetve az inzulinnak korábban leírt adenyl-cyclase inhibitor szerepével, izomsejtre gyakorolt proliferatív hatásával magyarázhatók. Ily módon az antidiabetikus therapia hatása a fennálló szövődmény ke-ringésdinamikai hatásához hozzáadódhat, melynek mértéke, esetleges előnye vagy kedvezőtlen korrekciója további kutatások tárgyát képezheti. így a micro-, illetve macroangipathiás szövődményben szenvedő diabetes betegeknél a CH anyagcsere rendezése során, az alkalmazott therapia esetleges haemodinamikai hatását is figyelembe kell vennünk a hosszú távra szóló antidiabetikus kezelés megválasztásakor.
Irodalom
- Garcia, M. J. és mtsai.: Morbidity and mortality in diabetics in the Framingham population. Diabetes 1974. 23. 105-111.
- Kannel, W. B. és mtsai.: Role of diabetes in congestive heart fa- ilure: The Framingham Study. Am. J. Cardiol. 34. 29-24.
- Pogátsa G.: A cukorbetegségben kialakuló szívelváltozások vizsgálatának újabb eredményei. Orvostudomány 4. 1994.
- Factor, S. M.: Capillary microaneurysm in the diabetic heart. New Engl. J. Med. 1980. 302. 384-88.
- Brownlee, M.: Advance glocosylation end products in tissue and the biochemical basis of diabetic complications. N. Engl. J. Med. 1988. 318. 1315-21.
- Vered, A. és mtsai.: Exercise induced left ventricular dysfuncti- on in young men with asymptomatic diabetes mellitus (diabetic cardiomyopathy). Am. J. Cardiol. 1984. 54. 633-37.
- Fein, F. S.: Diabetic Cardiomyopathy. Diabetes Care. 1990. Vol. 13. No. 11. Suppl. 4. 1169-1179.
- Uusitpa M. és mtsai.: Impairment of diastolic function in midd- le-aged type I. and type II. diabetic patients free of cardiovas- cular disease. Diabetológia 1988. 31. 783-791.
- Jermendy és mtsai.: Systolic time intervals in type I. diabetes mellitus during exercise. Diabetológia. 1983. 532-34.
- Khan, J. K.: Radionuclid assessement of left ventricular diastolic filling in diabetes mellitus with and without cardiac autonóm neuropathy. J. Am. Coll. Cardiol. 1986. 7. 1303-06.
- Rokey, R. és mtsai.: Determination of parameters of left ventricular diastolic filling with pulsed echocardiography: compa- rison with cineangiography. Circulation 1985. 71. No. 3. 543- 550.
- Zarich. S. W.: Diabetic cardiomyopathy. Am. Heart. J. 1989. 118. 1000-1112.
- Fraser. G. E. és mtsai.: Comparison of Echocardiographic Va- riables Between Type I. Diabetics and Normál Controls. Am. J. Cardiol. 1995. 75. 141-145.
- Ruddy. T. D. és mtsai.: The Relationship of Cardiac Diastolic Dysfunction to Concurrent Hormonal and Metabolic Status in Type I. Diabetes Mellitus. J. Clin. Endocrinol. Metab. 1988. 113. 113-118.
- Fein, F. S.: Diabetic cardiomyopathy. Diabetes Care, 1990. Vol. 13. No. 11. Suppl. 4. 1169-79.
- Hiramatsu. J. és mtsai.: Left ventricular filling abnormalities in non-insulin-dependent diabetes mellitus and improvement by short-term glycemic control. Am. J. Cardiol. 1992. 70. 1185- 1189.
- Paillole, C. és mtsai.: Prevalence and Significance of Left Ventricular Filling Abnormalities Determined by Doppler Echocardiography in Young Type I. (Insulin-Dependent) Diabetic Patients. Am. J. Cardiol. 1989. 64: 1010-1016.
- Raev, D. C.: Which Left Ventricular Function Is Impaired Ear- lier in the Evolution of Diabetic Cardiomyopathy? Diabetes Care, 1994. Vol. 17. No. 7. 633-639.
- Mustonen, J. N. és mtsai.: Left Ventricular Systolic Function in Middle-Aged Patients with Diabetes Mellitus. Am. J. Cardiol. 1994. 73.: 1202-1208.
- Uusitupa, M. és mtsai.: Impaírement of diastolic function in middle-aged type 1 (insulin-dependent) and type 2 (non-insu- lin-dependent) diabetic patienLs free of cardiovascular disease. Diabetología, 1988. 31. 783-791.
- Mildenberger, R. R.: Clinically unrecognized ventricular dysfunction in young diabetic patients. J. Am. Moll. Cardiol. 1984. 54. 633-637.
- Bélijc, T. és mtsai.: Improved metabolic control does not rever- se left ventricular filling abnormalities in newly diagnosed non-insulin-dependent diabetes patients. Acta Diabetol. 1994. 31. 147-150.
- Shapiro, L M. és mtsai.: Left ventricular function in diabetes mellitus I.: Methodology and prevalence end spectrum of ab-normalities. Br. Heart J. 1981. 45. 122-128.
- Airaksinen, J. és mtsai.: Impaired Left Ventricular Filling in Young Female Diabetics. A. Med. Scand. 1984. 216. 509-616.
- Airaksdinen. K. E.: Augmentation of atrial contribution to left ventricular filling in IDDM subjects as assesed by doppler echocardiography. Diabetes Care. 1989. 12. 159-161.
- Ferraro, S. és mtsai.: Comparison of left ventricular function in insulin- and non-insulin-dependent diabetes mellitus. Am. J. Cardiol. 1993. 71. 409-414.
- Di Bonito, P. és mtsai: Diastolic dysfunction in Patients with Non-insulin-dependent Diabetes Mellitus of Short Duration. Diabetic Medicine 1996. 13. 321-324.
- Hiramatsu, J. és mtsai.: Left ventricular filling abnormalities in non-insulin-dependent diabetes mellitus and improvement by short-term glycemic control. Am. J. Car. 1992. 70. 1185-1189.
- Pengargkul, S. és mtsai.: Depressed cardiac sarcoplasmic reti- cular function from diabetic rats. J. Mol. Cell. Cardiol. 1981. 13. 303-309.
- Ganguly, P. K. és mtsai.: Defectiv sarcoplasmic reticular cal- cium transport in diabetic cardiomyopathy. Am. J. Physiol. 1983. 144. E528-535.
- Sasson, Z. és mtsai.: Insulin resistance is an important determi- nant of left ventricular mass in obes. Circulation. 1993. 88. 1431-1436.
- Breitweser, J. A. és mtsai.: Cardiac septal hyperthrophy in hyperinsulinemic infants. J. Pediatr. 1980. 96. 535-539.
- Ito, H. és mtsai.: Insulin-like growth factor I induces hyperthrophy with enhanced expression of muscle-gene in cultured rat cardiomyocytes. Circulation 1993. 87. 1715-1721.
- Chi, L. és mtsai.: Actions of pinacidil at a reduced potassium concentration: a direct effect possibly involving the ATP-de- pendent potassium channel. J. Cardiovasc. Pharmacol. 1993. 21. 179-90.
- Hofmcmn. D. és mts.: Potassium channel blockade and acut myocardial infarction: implication for management of the non- insulin requiring diabetic patient. E. Heart J. 1993. 14. 1585- 1589
Dr. Nieszner Éva
HIETE Belgyógyászati és Kardiovascularis Centrum
II. Belgyógyászati Klinika
1135 Budapest, Szabolcs u. 35.
Érbetegségek: 1996/4. - 5-11. oldal


