Bevezetés: Az iliofemoralis szintű obstrukció műtéti megoldásának egyik gyakran alkalmazott módszere a Vollmar által bevezetett (1969) félig zárt ringstripper dezobliteráció. A módszer hátránya a leválasztott intima- media henger vakon történő proximális levágása, amely reziduális stenosis vagy lebegő intimaszél miatt korai reocclusióhoz vezethet. A műtéttel kombinált intervenció során az intraoperatív DSA képerősítő segítségével lehetőség van a szem ellenőrzése mellett végzett proximális levágására, a reziduális stenosis, illetve a disztális lebegő intimaszél stenttel történő fixálására.
Beteganyag és módszer: Fenti kombinált műtétet 49 esetben végeztük el. Az a. iliaca externa és a. femoralis communisra kiterjedő elváltozások 11 esetben TransAtlantic Inter-Society Consensus (TASC) B, 16 alkalommal TASC C, 22 betegnél TASC D csoportba tartoztak. A műtét során a ringstripper dezobliterációt a megelőzően az aortába vezetett intervenciós vezetődróton "over-the-wire" technikával végeztük, a proximális intimaperem ellátása stent beültetéssel történt.
Eredmények: A beavatkozások minden esetben sikeresek voltak. Intraoperatív szövődmény, illetve korai reocclusio nem fordult elő. Reoperációra 2 betegnél femoralis utóvérzés, egy esetben szeptikus szövődmény, egy alkalommal disztális bypass okklúzió miatt kényszerültünk. 16 hónapos átlagos utánkövetés mellett 2 resztenózis alakult ki.
Megbeszélés: Kezdeti eredményeink alapján a Vollmar dezobliteráció intervenciós kiterjesztésével "minimal invaziv" módon a teljes iliofemoralis rekonstrukció biztonsággal elvégezhető. A proximális intimavég stenttel történő fixálása, illetve az esetleges reziduális iliaca stenosis intervenciója kiküszöböli a hagyományos módszer hátrányait. E műtét alkalmazásával műér implantáció, illetve egy kiterjesztett műtéti megterhelés elkerülhető. A hosszú távú eredmények további utánkövetést igényelnek.
Érbetegségek: 2007/3. 107-116. oldal
KULCSSZAVAK
iliofemoralis rekonstrukció, Vollmar, dezobliteráció, intervenció, hibrid
Bevezetés
A radiológiai intervenció széles körű megjelenésével az iliofemoralis obstruktív elváltozások helyreállításának hagyományos taktikája kétségtelenül jelentős változáson ment keresztül. A technika elterjedésével a korábban kiterjesztett érsebészeti beavatkozást igénylő esetek kerülnek percután "helyreállításra". A TransAtlantic Inter-Society Consensus (TASC) (1) négy csoportba sorolja az iliofemoralis szakasz morfológiai elváltozásait (I. táblázat), ennek alapján tesz javaslatot a választandó eljárásra. Az ajánlások alapján az "A" kategória esetén intervenció, a "D" kategóriában sebészeti beavatkozás javasolt. Mindazonáltal a "B" és "C" kategória vonatkozásában az eredmények ellentmondásosak. Utánkövetés alapján az 5 éves nyitvamaradás szignifikánsan jobb a sebészi csoportban (64% vs. 86%) (2). Az a. iliaca externán (AIE) végzett intervenció statisztikailag szignifikáns módon rosszabb hosszú távú eredményt mutat az a. iliaca communis (AIC) hasonló beavatkozásainál, más szóval igazolt a jól ismert tény, hogy az AIE nem "hálás" terület az intervenció számára (3, 4, 5).

I. táblázat.
A TransAtlantic Inter-Society Consensus (TASC) morfológiai klasszifikációja.
A radiológia kihívásának megfelelően az érsebészeti gyakorlatban is tetten érhető a csökkentett vagy minimal invazív beavatkozásra való törekvés. Az unilateralis iliofemoralis régióra vonatkozóan ennek a követelménynek messze megfelel a Vollmar által (1969) bevezetett, izolált femoralis feltárásból végzett félig zárt retrográd thrombendarterectomia (TEA) (6). Az eredeti műtét eredményeit azonban jelentősen rontja a desobliterátum vakon végzett proximális levágása, amelynek következtében proximális residuális stenosis, lebegő intimaszél maradhat vissza korai restenosishoz, occlusióhoz vezetve (7, 8, 9).
A két módszer kombinációjával az előnyök összeadódnak, a hátrányok kiküszöbölhetők. Az intraoperatív DSA készülék segítségével láthatóvá tehető a proximális iliaca szegment, szükség esetén intervenciós beavatkozással kombinálva a műtétet.
Vizsgálatunk célja, hogy a döntően AIE - a. femoralis communis (AFC) régióra lokalizálódó, TASC B-C-D csoportba sorolható esetek általunk bevezetett hibrid (TEA+intervenció) műtétjének rövid- és középtávú eredményeit áttekintsük.
Hibrid iliofemoralis TEA (HIFTEA) műtétet indikáltunk az angiográfia alapján AIE stenosis és/vagy occlusio esetén. Azonos oldali AIC stenosis, femoropoplitealis stenosis és/vagy occlusio nem jelentett kontraindikációt. A HIFTEA ellenjavallt az iliofemoralis szintű aneurizmatikus elváltozás vagy az iliaca externa 5 mm átmérőnél kisebb fibrotikus degenerációja esetén. Az AIC hosszú szakaszú, aorta bifurkációig érő occlusiója szintén kontraindikációt jelentett. Az aorta stenosisa vagy bilaterális iliaca betegség esetén, egyedi mérlegelés és a kísérő betegségek alapján döntöttünk a HIFTEA vagy kiterjesztett abdominalis műtét között.
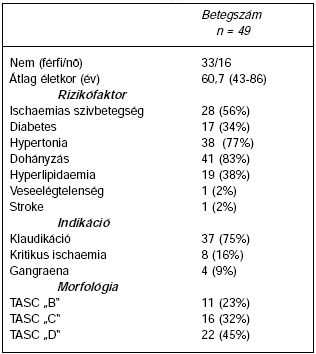
II. táblázat.
A betegek demográfiai adatai, rizikófaktorok, műtéti indikáció és TASC beosztás.
Beteganyag
2004. január 1-jétől 2006. június 30-ig 55 beteget választottunk be a műtétre. 6 esetben később részletezett okból nyitott extraperitonealis konverzióra kényszerültünk, ezért ezeket a vizsgálatból kizártuk. A fennmaradó 49 beteg átlag életkora 60,7 év (43-86 év), 33 férfi, 16 nő. A műtét indikációja 37 betegnél 100 méter alatti claudicatio, 8 esetben gangraena, 4 alkalommal kritikus ischaemia volt. A demográfiai adatok, a rizikófaktorok és TASC klasszifikáció szerinti megoszlás a II. táblázatban látható.
A claudicatiós csoportban konzervatív terápia hatástalansága esetén került sor műtétre. A preoperatív kivizsgálás fizikális vizsgálatból, doppler index mérésből, szükség esetén color-flow duplex vizsgálatból (aneurysma, ectasia gyanúja esetén), illetve angiográfiából állt.
Hibrid iliofemoralis TEA (HIFTEA) műtétet indikáltunk az angiográfia alapján AIE stenosis és/vagy occlusio esetén. Azonos oldali AIC stenosis, femoropoplitealis stenosis és/vagy occlusio nem jelentett kontraindikációt.
A HIFTEA ellenjavallt az iliofemoralis szintű aneurizmatikus elváltozás vagy az iliaca externa 5 mm átmérőnél kisebb fibrotikus degenerációja esetén. Az AIC hosszú szakaszú, aorta bifurkációig érő occlusiója szintén kontraindikációt jelentett. Az aorta stenosisa vagy bilaterális iliaca betegség esetén, egyedi mérlegelés és a kísérő betegségek alapján döntöttünk a HIFTEA vagy kiterjesztett abdominalis műtét között.
Módszer
A beteg előkészítése a standard módon történik, a konszenzus nyilatkozat tartalmazza az esetleges műtéti kiterjesztésre szükséges beleegyezést is. A fektetés és femoralis feltárás hagyományos módon történik. Az iliofemoralis átmenetben a rendszerint mediális és laterális circumflexa oldalágat külön, ezek eredése felett az AFC-t dupla gumihurokra vesszük. Testsúlytól függően 7500-10000 NE NaHeparint adagolunk a betegnek.
Seldinger tűvel punkciót végzünk az AFC középső harmadán, majd intoducert vezetünk be retrográd irányba. Mobil, C-karos DSA készülékkel intraoperatív angiográfiát készítünk az aorta bifurkációtól distalisan a teljes iliaca szakaszról. Road-map technikával a stenosis mértékétől, morfológiájától függően "J" vagy "egyenes" végű, szükség esetén hidrofil bevonatú 0,035˝ diagnosztikus vezetődrótot vezetünk az aortába. Legfontosabb cél a drót proximális végének az aortába juttatása úgy, hogy a proximális nyitott érszakasz területén a drót valódi lumenben legyen. AIE occlusio esetén "egyenes" végű diagnosztikus katéter supportként történő alkalmazásával segíthetjük a drót áthaladását. Sikeres drót felvezetést a drót könnyű, akadálymentes mozgathatósága jelzi. AIE occlusio, vagy nem kielégítő retrográd angiográfiás kép esetén, a dróton diagnosztikus katétert vezetünk az AIC-be, és anterograd képet készítünk. Ezután hosszanti arteriotómiát ejtünk az AFC-n, és hagyományos módon körkörös intimahengert képezünk a lamina elastica externa rétegében. Tompa végű dissecáló spatulával kiterjesztjük a réteg képzést proximális irányba, miközben ügyelünk a drót helyben (aortában) maradására - célszerűen kifogjuk az izolálás fix pontjához. Alkalmas méretű (5-10 mm) Vollmar ringstrippert (Aesculap) fűzünk a drót szabad végén át az átvágott intima hengerre, majd a road-map képen folyamatos átvilágítással követve fokozatos, sodró mozdulattal választjuk le az intimahengert - lehetőség szerint az iliaca interna (AII) eredéséig, ahol általában ez előbbi eredése akadályát képezi a további leválasztásnak. Amennyiben a road-map képen elértük a kívánt magasságot, a gyűrűben lévő vágó drót meghúzásával átvágjuk az intima hengert, amelyet a henger proximális részének megmozdulása, illetve a vágó drót vezető drótra feszülése - megakadása - jelez. Ezután a vezető drótra feszülő strippert a levágott intima hengerrel és a vezetődróttal együtt lassan lefelé húzzuk, amíg a gyűrű megjelenik az arteriotómia nyílásában. Közben fluoroszkópiával folyamatosan figyeljük a vezető drót proximális végét, hogy ne kerüljön a levágás szintje alá. Ez könnyen elkerülhető, ha előzetesen a drótot magasan az aortába vezettük. A levágott intimahenger általában 10-20 cm hosszú, a drót proximális végének ekkora retrográd mozgására kell számítani. A teljes manipuláció során a proximális vérzést a dupla gumihurokkal kontrolláljuk. A vezetődróton keresztül újra bevezetjük az introducert, amelyet szintén a gumihurokkal rögzítünk. Retrográd DSA képet készítünk, amelyen jól látszik a proximális stenosis, intimalépcső, esetleges disszekció, a lebegő intimaszél, reziduális intima. Az előbbiek megoldására megfelelő méretű ballonra épített acél (rövid szegment) vagy öntáguló nitinol (hosszabb szegment) stentet deponálunk. Az eredményt kontroll angiográfiával ellenőrizzük (1. ábra). Kielégítő morfológiai eredmény esetén a drótot, introducert eltávolítjuk, a disztális intima leszegésével, szükség esetén a műtét további disztális kiterjesztésével (profunda TEA, AFS TEA, bypass), az arteriotómia direkt zárásával fejezzük be a beavatkozást.
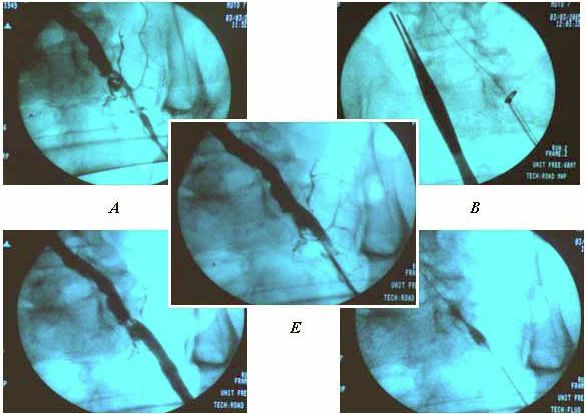
1. ábra.
A: Intraoperatív retrográd angiographia. B: "over-the-wire" ringstripper desobliteratio. C: kontroll angiographia, szignifikáns reziduális stenosis. D: stent implantáció. E: kontroll angiographia, jó morphológiai eredmény.
A posztoperatív hatodik napig preventív dózisú LMWH kezelés mellett folytattuk a korábbi antithrombocyta medikációt (100 mg Aspirin/die, ASA-nonresponder vagy intolerancia esetén 2x75 mg ticlopidin). Egyéb okból szükséges cumarin kezelést folytattunk.
A beteg távozásakor az operált végtag klinikai állapotában bekövetkezett változást az American Heart Association (AHA) (22) beosztása szerint állapítottuk meg (III. táblázat).
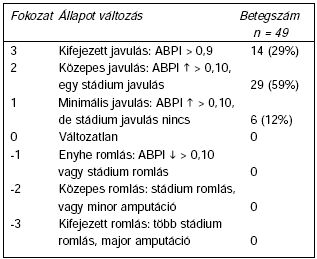
III. táblázat.
Az American Heart Association klasszifikációja a postprocedurális állapot változásról (22), eredményeink ennek alapján.
Az utánkövetés a műtétet követő 6. héten, majd félévente fizikális és doppler nyomás vizsgálatból állt. Restenosis vagy occlusio gyanúja esetén color duplex vizsgálatot végeztünk. Szignifikáns restenosisként értelmeztük a 70%-nál nagyobb szűkületet a desobliterált érszakaszon.
Elsődleges nyitvamaradás: a vizsgált időszakban az átjárható desobliterált érszakaszon egyéb beavatkozás nélkül. Késői restenosis miatt szükséges PTA/stent esetén elsődleges asszisztált nyitvamaradásról, a restenosis vagy occlusio miatt végzett újabb műtét esetén másodlagos nyitva maradásról beszélünk.
Utóbbiak statisztikai analízisét XLSTAT 2006 (Addinsoft) szoftverrel végeztük. A nyitvamaradási értékeket life-table módszerrel számítottuk.
Eredmények
55 beteget készítettünk elő a kombinált beavatkozásra. 6 esetben extraperitonealis nyitott konverzióra kényszerültünk, 5 esetben sikertelen drót felvezetés, illetve eredménytelen hagyományos Vollmar TEA, egy esetben subintimalis stent depozíció miatt (valamennyi konverzió a műtét bevezetésének első 6 hónapjában történt). A fennmaradó 49 beteg eredményeit vizsgáltuk.
3 alkalommal (6%) sikerült a Vollmar eszközt az iliaca interna (AII) eredése fölé az iliaca communisba vezetni. 36 esetben (73%) a proximális intima henger átvágása közvetlen az AII eredés alatt, 10 betegnél (21%) az AIE proximális-középső harmadában történt. A kontroll angiográfia során 4 esetben (8%) az AIE falához tapadó reziduális intimarészletek igazolódtak, amelyek ismételt ringstripper manipulációval kerültek eltávolításra. 50%-nál kisebb reziduális stenosis 26 (53%), ennél nagyobb szignifikáns stenosis 19 (38%) esetben fordult elő. Valamennyi esetben észlelhető volt a proximális intimacsonk "megmozdulása, lebegése", amelyet a hosszabbrövidebb szakaszon jelentkező subintimalis kontrasztanyag telődés ("dissectio") jelzett. A fenti eltérések korrigálására minden esetben stent implantációt végeztünk, 3 betegnél két fémhálót alkalmaztunk az AIC hosszú szakaszú stenosisa miatt (összesen 52 stent).
29 esetben (59%) a. profundára, 10 alkalommal (20%) a. superficialisra, 10 esetben (20%) mindkettőre kiterjesztett lokális TEA-t végeztünk. 5 (11%) esetben distalis kiegészítésként térd feletti poplitea szakaszra vezetett bypasst (3 VSM, 2 dacron) végeztünk. Az AFC tómiáját 33 (67%) esetben direkt varrattal, 11 (23%) esetben folttal, 5 alkalommal a disztális bypass proximális anastomosisával zártuk.
Intraoperatív szövődmény és korai reocclusio nem fordult elő (primer eredményesség 100%).
Az átlagos ápolási idő 8,9 nap (5-16 nap) volt. Ez idő alatt 4 reoperációra kényszerültünk, 2 (4%) esetben femoralis utóvérzés, 1 esetben (2%) sebsuppuratio, 1 (2%) esetben a disztális femoropoplitealis VSM bypass occlusiója miatt.
Az operált végtag klinikai állapotában bekövetkezett változást az American Heart Association (AHA) (22) beosztása szerint állapítottuk meg: 14 (29%) esetben kifejezett, 29 (59%) betegnél közepes, 6 (12%) alkalommal enyhe klinikai javulást értünk el. Változatlan vagy roszszabb állapot nem alakult ki (III. táblázat).
Az átlagos utánkövetés 15,7 (1-35) hónap volt, 4 (8%) betegről nincs információ, működő desobliterált érszakasz mellett 2 exitus (13. hónapban myocardialis infarctus, 25. hónapban malignus betegség) fordult elő.
Szignifikáns restenosist két esetben (postop. 8., illetve 11. hónap) észleltünk. Mindkét alkalommal dysbasiás panaszok fokozódása, egyik esetben acralis minor necrosis kiújulása, gyenge femoralis pulzus, ABPI (ankle-brachial blood pressure index) csökkenése, valamint duplex vizsgálat igazolta a restenosist. Mindkét betegnél a proximális intima csonk az AIE középső harmadában volt, a restenosis az utóbbit lefedő stenten belül (instent restenosis) alakult ki. Elektív extraperitonealis nyitott desobliteraciót végeztünk a stent eltávolításával szövődménymentesen, távozáskor a klinikai javulás mindkét betegnél 3-as fokozatú volt.
Life-table módszerrel végzett számítás alapján az elsődleges nyitvamaradás 12. hónapnál 97,1%, 24. hónapnál 93,6%, 30. hónapnál 93,6% (6. ábra), a másodlagos nyitvamaradás 30. hónapnál 100% volt.
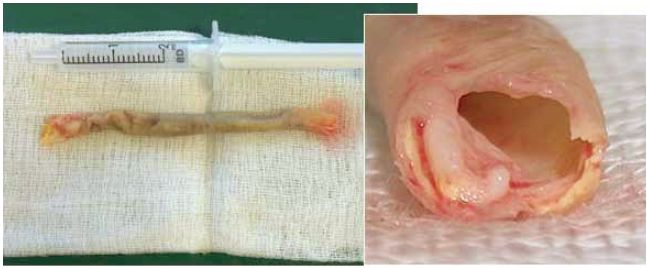
2. ábra.
Eltávolított intimahenger, a proximális csonk területén jelentős reziduális stenosis.
Megbeszélés
Az iliofemoralis régió érsebészeti helyreállító beavatkozásai közül a Vollmar által bevezetett AIE félig zárt TEA előnye:
- A stenoticus pathológiai folyamat szubsztrátumát jelentő intima-media henger eltávolításra kerül (v. ö.: primer AIE stenting, (10) AFC desobliterációval kombinált AIE stenting (11) (2. ábra).
- Heterológ anyag (műanyag bypass) nem kerül beültetésre.
- Megfelel a minimal invazív sebészet törekvésének, izolált femoralis feltárásból a műtét elvégezhető.
Hátrányai azonban jelentősen korlátozzák, illetve rontják a műtét eredményeit:
- Az iliaca interna (AII) eredése a stripper számára "akadályt" képez, így proximális irányban általában a desobliteráció határát képezi.
- Szem ellenőrzés hiányában a desobliterált érfalon, illetve a proximális intimaszél területén visszamaradó lebegő intima, reziduális stenosis korai reocclusio oka lehet (8, 9).
A fenti műtét több módosításon ment keresztül, amelyek célja egyrészt a desobliterált érszakasz hosszának növelése, másrészt a "vakon" végzett beavatkozás "szemmel" történő ellenőrzése.
Előbbire példa MollRing-stripper bevezetése (12), amely az eredeti műszer drótjának funkcióját két, ollószerűen működő gyűrűvel helyettesíti. Smeets közleményében a fenti eszközzel 85%-os 3 éves asszisztált elsődleges nyitva maradást ért el (13), azonban nem teljesen érthető a közleményből az AIC hasonló módon történő desobliterációja.
Utóbbira példa az extraperitonealis feltárásból végzett nyitott, vagy félig nyitott TEA (14, 15), valamint az everziós technikával végzett műtét (16), ezek azonban a nagy műtéti megterhelés miatt nem felelnek meg a minimal invazív törekvésnek.
A desobliterált érszakasz és a proximális intimacsonk műszeres ellenőrzésére a duplex UH vagy nyomásgrádiens mérés intraoperatív használata nehézkes, az angioszkópia (17) a vértelenség igénye miatt nem került széleskörű alkalmazásra. Az intravasculáris ultrahang diagnosztika alkalmas készülék és megfelelő szakember esetén nagy pontossággal detektálja az eltéréseket.
Vogt közleményében 20 műtét során alkalmazták az intraoperatív UH kontrollt (7), ebből 14 esetben sikerült az eszközt az AIC-be felvezetni. 10 esetben (50%!) találtak residuális intimarészt, és 10 esetben reziduális 40-60%-os stenosist.
Az intraoperatív DSA alkalmazása megoldást jelent a félig zárt TEA mindkét hátrányának kiküszöbölésére:
- Segítségével láthatóvá válik a lebegő intima és a reziduális stenosis.
- Az általunk bevezetett kombinált technika révén lehetőség nyílik a rekonstruált érszakasz kiterjesztésére: AIC stenosis, proximális intimacsonk területén visszamaradó reziduális stenosis intervenciós megoldása.
Utóbbi megállapítást két tény magyarázza:
- Az AIE sebészi desobliterációjával az eredeti TASC C-D morfológia A-B formába kerül (AIC területén szegmentális vagy akár hosszabb 3-6 cm-es stenosis), amely az ajánlások alapján (1) már javasolt az intervenciós beavatkozásra.
- A proximális intimacsonk stenttel történő tágításának indikációja 50%-nál nagyobb reziduális stenosis esetén egyértelmű. Ilyen eset anyagunkban 38%-ban, Vogt közleményében 50%-ban (7) fordult elő.
További megfontolást igényel, hogy a proximális intimacsonk területén kialakuló lebegő intimaszegély a késői restenosis kialakulásának döntő tényezője lehet, amelynek stenttel történő lefedése megakadályozhatja a szűkület kialakulását (3. ábra).
Elméleti meggondolás alapján a gyűrűvel leválasztott és a dróttal átvágott intima síkja nem esik azonos vonalba, illetve a dróthurok húzása további lokális proximális diszszekciót hoz létre (4. ábra). Ennek következtében az átvágás után néhány mm-es körkörös, mobilis intimaszél marad vissza.
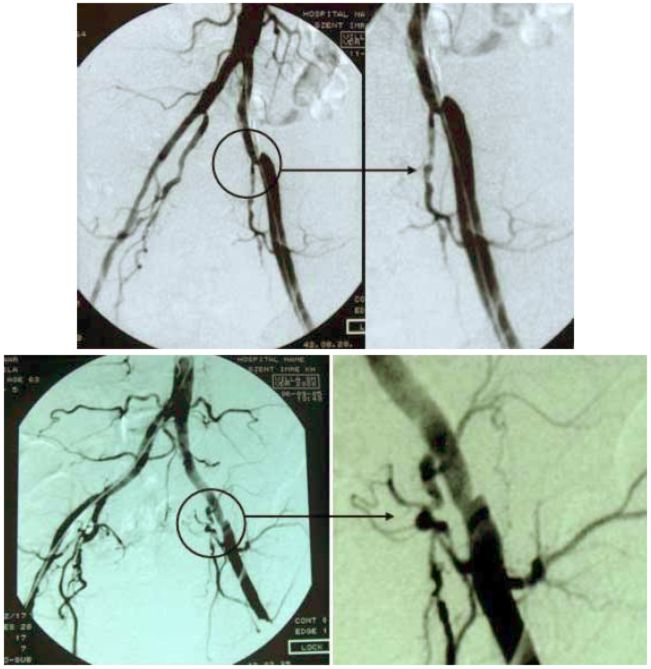
3. ábra.
Hagyományos Vollmar TEA után kialakult proximális stenosis angiographiás képe.
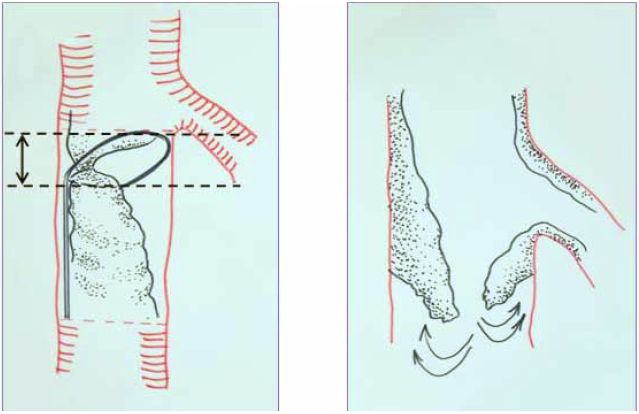
4. ábra.
A proximális lebegő intimaszél kialakulásának mechanizmusa.
A folyadékok áramlását az alábbi két alapvető fizikai összefüggés jellemzi:
- Kontinuitási egyenlet: Egy áramlási cső két különböző keresztmetszetén a folyadék áramlási sebessége fordítottan arányos a keresztmetszetekkel (18). (Abból adódik, hogy az áramlási cső bármely helyén ugyanannyi idő alatt ugyanannyi térfogatú folyadék áramlik át.)
Képlettel:
A1v1 = A2 v2
(A: keresztmetszet, v: sebesség) - Bernoulli-törvény: Súrlódásmentes áramlásban a nyomás nagysága állandó (19).
p + 1/2 q v2 + h q g = állandó
(p: statikai nyomás, q: viszkozitás, v: sebesség, h: vonatkozási magasság, g: nehézségi gyorsulás)
Fentiek alapján a reziduális relatív stenosis (eredeti lumen kisebb átmérőjű) területén a nyomás csökken, azaz "szívóerő" lép fel, amely a körkörös intimaszegélyt a lumen felé fordítja. Feltételezhető még a lebegő szél mögött fellépő turbulens áramlás hasonló irányba ható szerepe is (20, 21). Mindez jól látható a hagyományos Vollmar dezobliteráció után készült angiográfia felvételein (5. ábra).
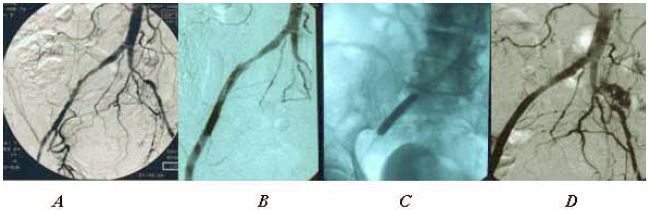
5. ábra.
A: preoperatív morphológia.
B: hagyományos Vollmar TEA kontroll angiographia: részleges proximális dissectio, reziduális stenosis.
C: stent depozíció.
D: jó eredmény.
A proximális intimacsonk stenttel történő lefedése tehát e fizikai hatások kiküszöbölése révén, a hagyományos műtét során természetszerűleg visszamaradó szabad intimaszél következtében kialakuló restenosis megelőzésére szolgálhat (6. ábra).
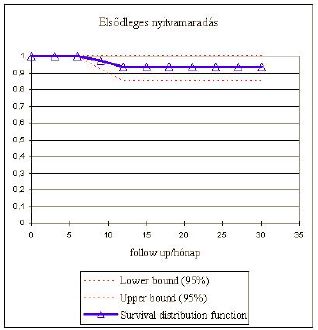
6. ábra.
Life-table analízis: elsődleges nyitvamaradás (XLSTAT2006, Addinsoft).
A sikeres HIFTEA műtét előfeltétele a diagnosztikus vezetődrót aortába juttatása. A manőver sztenotikus AIE esetén nem különösebben nehéz, szegmentális vagy teljes okklúzió esetén azonban nagy gyakorlat mellett is többször sikertelen. Fontos a drót helyzetének pontos megítélése, subintimalis elhelyezkedés esetén a stent depozíciója a műtét extraperitoneális konverzióját igényli, utóbbi anyagunkban egy esetben, a tanulási fázisban fordult elő. Sikertelen drót felvezetés esetén lehetőség van az ellenoldali - amennyiben nyitott - femoralis percutan punkcióján keresztül crossover technikával anterograd drót levezetésre a dezobliteráció után. Utóbbit magunk részben az invazivitás kiterjesztése, részben a postprocedurális nyomókötés kényelmetlensége (ellenoldali friss műtéti seb) miatt csak legvégső esetben alkalmazzuk.
Az intervenciós beavatkozások terjedésének korában sokan megkongatják a vészharangot az érsebészet felett. A fentiekben részletezett beavatkozás jól demonstrálja az érsebészeti beavatkozások változatlan szerepét az arteriosclerosis tüneteinek enyhítésében. A két módszer kombinálásával a hátrányok közömbösíthetők, az előnyök összeadódnak. Az alapvető különbség a sebészi dezobliteráció és az intervenció között az, hogy az előbbi során eltávolításra kerül a stenosishoz vezető patológiai szubsztrátum, az intima-media henger, megszüntetve ezáltal a restenosis kialakulásnak feltételét. Az operált érszakaszban kialakuló reocclusiót általában a be-, illetve kiáramlási pálya eredeti intimájának területén kialakuló progresszió okozza. Mindazonáltal tapasztalatunk alapján az occludált stentek eltávolítása technikailag általában könnyű (post-stent érsebészet). Ennek oka talán a beültetett fém idegen test környezetében kialakuló idegentestreakció, speciális gyulladásos elemekkel, amelyek az érfal rétegeinek markánssá válásához, könnyebb desobliterációhoz vezetnek.
Eredményeink és a fenti megfontolások alapján megállapítható, hogy a minimal invazív iliofemoralis rekonstrukcióra törekvés ígéretes módszere az általunk bevezetett hibrid beavatkozás, amellyel a hagyományos félig zárt Vollmar dezobliteráció "nyitottá, láthatóvá" tehető, stent deponálással a korai restenosist, reocclusiót okozó tényezők (proximális reziduális stenosis, lebegő intima) egy része kiküszöbölhető.
Irodalom
- Dormandy, J. A.: Management of peripheral arterial disease (PAD). TASC Working Group. TransAtlantic Inter-Society Consensus (TASC). J. Vasc. Surg. 31. (suppl), 1-296., (2000)
- Timaran, C. H., Prault, T. L., Stevens, S. L., Freeman, M.B., Goldman, M. H.: Iliac artery stenting versus surgical reconstruction for TASC (TransAtlantic Inter-Society Consensus)type B and type C iliaca lesions. J. Vasc. Surg. 38., 272-278., (2003)
- Johnston, K. W., Rae, M., Hogg-Johnston, S. A., Colapinto, R. F., Walker, P. M., Baird, R. J., Sniderman, K. W., Kalman, P.: Five-year results of a prospective study of percutaneous transluminal angioplasty. Ann. Surg. 206., 403-413., (1987)
- Powell. R. J., Fillinger. M., Walsh. D. B., Zwolak. R., Cronenwett. J. L.: Predicting outcome of angioplasty and selective stenting of multisegment iliac occlusive disease. J. Vasc. Surg. 32., 564-569., (2000)
- Powell, R. J., Bettmann, M., Fillinger, M., Feffrey, R., Langdon, D., Walsh, D. B.: The durability of endovascular treatment of multisegment iliac occlusive disease. J. Vasc. Surg. 31, 1178-1184, (2000)
- Vollmar, J., Laubach, K., Gruss, J. D.: The technique of thrombendarterectomy (spiral ring disobliteration) Bruns Beitr. Klin. Chir. 217., 678-690., (1969)
- Vogt, K. C., Sillesen, H., Schroeder, T. V.: The use of intravascular ultrasound for intraoperative assessment during semiclosed thrombendarterectomy. Ultrasound. Med. Biol. 24., 21- 25., (1998)
- Van den Dungen, J. J. A. M, Boontje, A. H., Kropveld, A.: Unilateral iliofemoral occlusive disease: Long term results of semiclosed endarterectomy with the ringstripper. J. Vasc. Surg.14., 673-677., (1991)
- Van den Heijden, F. H. W. M., Eikelboom, B. C., van Reedt Dortland, R. W. H.: Long term results of semiclosed endarterectomy of the superficial artery and the outcome of failed reconstructions. J. Vasc. Surg. 18., 271-279., (1993)
- Veville, C. D., Kashyap, V. S., Clair, D. G., Bena, J. F., Lyden, S. P., Greenberg, R. K., O'Hara, P. J., Sarac, T. P., Ouriel, K.: Endovascular management of iliac artery occlusions: extending treatment to TransAtlantic Inter-Society Consensus class C and D patients. J. Vasc. Surg. 43., 32-9., (2006)
- Nelson, P. R., Powell. R. J., Schermerhorn. M. L., Fillinger. M. F., Zwolak. R. M., Walsh. D. B., Cronenwett. J. L.: Early results of external artery stenting combined with common femoral artery endarterectomy. J. Vasc. Surg. 35., 1107- 1113., (2002)
- Teijink, J. A., van den Berg, J. C., Moll, F. L.: A minimally invasive technique in occlusive disease of the superficial femoral artery: remote endarterectomy using the MollRing Cutter. Ann. Vasc. Surg. 15., 594-598., (2001)
- Smeets, L., de Borst, G. J., de Vries, J. P., van den Berg, J. C., Ho, G. H., Moll, F. L.: Remote iliac artery endarterectomy: seven-year results of a less invasive technique for iliac artery occlusive disease. J. Vasc. Surg. 38., 1297-1304., (2003)
- Radoux, J. M., Maiza, D., Coffin, O.: Long-term outcome of 121 iliofemoral endarterectomy procedures. Ann. Vasc. Surg. 15., 163-170., (2001)
- Oertli, D., Wigger, P., Landmann, J., Waibel, P.: Long-term results after open and semiclosed thrombendarterectomy for aortoiliac occlusive disease. Eur. J. Vasc. Endovasc. Surg. 11., 432-436., (1996)
- Vitale, G. F., Inahara, T.: Extraperitoneal endarterectomy for iliofemoral occlusive disease. J. Vasc. Surg. 12., 409-413., (1990)
- Neville, R. F., Yasuhara, H., Watanabe, B. I.: Endovascular management of arterial intimal defects: An experimental comparison by arteriography, angioscopy and intravascular ultrasonography. J. Vasc. Surg. 13., 496-502., (1991)
- Tandon, P. N., Rana, U. V., Kawahara, M., Katiyar, V. K.: A model for blood flow through a stenotic tube. Int. J. Biomed. Comput. 32., 61-78., (1993)
- Bálint P.: Orvosi Élettan. Medicina Könyvkiadó, 1. kötet, 151., 167., (1981)
- Imbesi, S. G., Kerber, C. W.: Why do ulcerated atherosclerotic carotid artery plaques embolize? A flow dynamics study. Am. J. Neuroradiol. 19., 761-766., (1998)
- Binns, R. L., Ku, D. N.: Effect of stenosis on wall motion. A possible mechanism of stroke and transient ischemic attack. Arteriosclerosis, 9., 842-847., (1989)
- Pentecost, M. J., Criqui, M. H., Dorros, G., Goldstone, J., Johnston, K. W., Martin, E. C., Ring, E. J., Spies, J. B.: Guidelines for peripheral percutaneous transluminal angioplasty of the abdominal aorta and lower extremity vessels. A statement for health professionals from a special writing group of the councils on Cardiovascular Radiology, Arteriosclerosis, Cardio-Thoracic and Vascular Surgery, Clinical Cardiology, and Epidemiology and Prevention, the American Heart Association Members. J. Vasc. Interv. Radiol .14., S495-S515., (2003)
dr. Simó Gábor
1115 Budapest, Tétényi u. 12-16.
Érbetegségek: 2007/3. 107-116. oldal


