Típusa: Klinikai egészségügyi szakmai irányelv
Azonosító: 001472
Érvényesség időtartama: 2020. 01. 31.
Érbetegségek: 2017/2. 41-62. oldal
I. IRÁNYELVFEJLESZTÉSBEN RÉSZTVEVŐK
Társszerző
Egészségügyi Szakmai Kollégiumi Tagozat(ok):
1. Angiológia és érsebészet Tagozat
Dr. Farkas Katalin
belgyógyász, angiológus, profilvezető főorvos, Szent Imre Egyetemi Oktatókórház, Angiológia Profil, a fejlesztőcsoport kapcsolattartója, társszerző
Dr. Mátyás Lajos
érsebész, részlegvezető főorvos, Borsod-Abaúj-Zemplén Megyei Kórház és Egyetemi Oktató Kórház Ér- és Endovascularis Sebészeti Részleg, társszerző
Dr. Palásthy Zsolt
sebész, érsebész, osztályvezető egyetemi adjunktus, Szegedi Tudományegyetem, Sebészeti Klinika, társszerző
Dr. Landi Anna
belgyógyász, angiológus, főorvos, Belváros-Lipótváros Egészségügyi Szolgálat, Angi - ológia, társszerző
Prof. Dr. Pécsvárady Zsolt
belgyógyász, angiológus, osztályvezető főorvos, Pest Megyei Flór Ferenc Kórház, II. Belgyógyászati Osztály, Angiológia, társszerző
Véleményező
Egészségügyi Szakmai Kollégiumi Tagozat(ok):
1. Belgyógyászat, endokrinológia, diabétesz és anyagcserebetegségek Tagozat
Prof. Dr. Karádi István, tagozatvezető, véleményező
2. Radiológia Tagozat
Dr. Bánsághi Zoltán, radiológus, intevenciós radiológus, a MACIRT elnöke, igazgatóhelyettes, Semmelweis Egyetem Radiológiai Klinika, véleményező
3. Kardiológia Tagozat
Prof. Dr. Merkely Béla, tagozatvezető, véleményező
4. Geriátria és krónikus ellátás Tagozat
Prof. Dr. Bakó Gyula, tagozatvezető, véleményező
5. Sebészet Tagozat
Prof. Dr. Oláh Attila, tagozatvezető, véleményező
6. Háziorvostan Tagozat
Dr. Szabó János, tagozatvezető, véleményező
"Az egészségügyi szakmai irányelv készítése során a szerzői függetlenség nem sérült."
"Az egészségügyi szakmai irányelvben foglaltakkal a fent felsorolt egészségügyi szakmai kollégiumi tagozatok vezetői dokumentáltan egyetértenek."
Az irányelvfejlesztés egyéb szereplői Betegszervezet(ek) tanácskozási joggal:
1. Betegszervezet megnevezése
-
Egyéb szervezet(ek) tanácskozási joggal:
1. Egyéb szervezet megnevezése
-
Szakmai társaság(ok) tanácskozási joggal:
1. Magyar Angiológiai és Érsebészeti Társaság
Prof. Dr. Járai Zoltán, belgyógyász, kardiológus, angiológus, profilvezető főorvos, Szent Imre Egyetemi Oktatókórház, Kardiológia Profil, tanácskozási joggal
2. Kardiológiai Profil, tanácsközási joggal
Dr. Kolossváry Endre, belgyógyász, angiológus, profilvezető helyettes főorvos, Szent Imre Egyetemi Oktatókórház, Angiológia Profil, tanácskozási joggal
3. Angiológiai Profil, tanácskozási joggal
Dr. Jassó István, belgyógyász, angiológus, részlegvezető főorvos, Egyesített Szent István és Szent László Kórház-Rendelőintézet, I. Belgyógyászati Osztály, Angiológiai Részleg, tanácskozási joggal
II. ELŐSZÓ
A bizonyítékokon alapuló egészségügyi szakmai irányelvek az egészségügyi szakemberek és egyéb felhasználók döntéseit segítik meghatározott egészségügyi környezetben. A szisztematikus módszertannal kifejlesztett és alkalmazott egészségügyi szakmai irányelvek, tudományos vizsgálatok által igazoltan, javítják az ellátás minőségét. Az egészségügyi szakmai irányelvben megfogalmazott ajánlások sorozata az elérhető legmagasabb szintű tudományos eredmények, a klinikai tapasztalatok, az ellátottak szempontjai, valamint a magyar egészségügyi ellátórendszer sajátságainak együttes figyelembevételével kerülnek kialakításra. Az irányelv szektorsemleges módon fogalmazza meg az ajánlásokat. Bár az egészségügyi szakmai irányelvek ajánlásai a legjobb gyakorlatot képviselik, amelyek az egészségügyi szakmai irányelv megjelenésekor a legfrissebb bizonyítékokon alapulnak, nem pótolhatják minden esetben az egészségügyi szakember döntését, ezért attól indokolt esetben dokumentáltan el lehet térni.
III. HATÓKÖR
Egészségügyi kérdéskör:
perifériás verőérbetegség ellátása
Ellátási folyamat szakasza(i):
diagnosztika, kezelés, rehabilitáció, gondozás
Érintett ellátottak köre:
perifériás artériás keringési zavarban szenvedő felnőtt
Érintett ellátók köre
Szakterület:
0100 belgyógyászat,
0101 angiológia, phlebológia, lymphológia,
0106 geriátria,
0203 érsebészet,
4000 kardiológia,
5100 röntgendiagnosztika,
5103 angiográfiás diagnosztika,
5108 CT diagnosztika,
5109 MRI diagnosztika,
5203 vaszkuláris intervenciós radiológia,
6301 háziorvosi ellátás,
6303 felnőtt és gyermek (vegyes) háziorvosi ellátás
Egyéb specifikáció:
nincs
IV. MEGHATÁROZÁSOK
1. Fogalmak
A perifériás verőérbetegségek: az aortának és az aorta a koszorúereken kívüli ágainak progresszív szűkületével, elzáródásával, vagy éppen permanens tágulatával (aneurysma) járó kórképek. Szűkebb (és egyben világszerte elfogadott) értelemben a perifériás verőérbetegség alatt az alsó végtag artériáinak obliteratív megbetegedését értjük (perifériás obliteratív verőérbetegség), jelen irányelv ennek ellátására vonatkozik. Az alsóvégtagi érszűkület követ - keztében a keringés nem képes a szöveti oxigénigényt biztosítani. Ez enyhébb esetben claudicatio intermittenshez (Fontaine II stádium) vagy súlyosabb esetben szöveti károsodáshoz, kritikus végtagischaemiához vezet (Fontaine III, IV stádium).
2. Rövidítések
| AAA | hasi aorta aneurysma |
| BKI | boka-kar index |
| CI | claudicatio intermittens |
| CTA | computer tomographiás angiographia |
| DSA | digitális subtractiós angiographia |
| DUS | Duplex Ultrahang vizsgálat |
| KVI | kritikus végtag ischaemia |
| KKVI | krónikus kritikus végtag ischaemia |
| MI | miokardiális infarktus |
| MRA | mágneses rezonanciás angiographia |
| PAD | perifériás verőérbetegség |
| TAG | thrombocyta aggregáció gátló |
3. Bizonyítékok szintje
A bizonyítékok besorolására használt rendszert a fejlesztő csoport az Európai Kardiológus Társaság irányelvéből vette át. [3]
A szövegben a bizonyítékok besorolását a szöveges leírás után tett zárójelben jelöljük, pl.: (Evidencia szint: C).
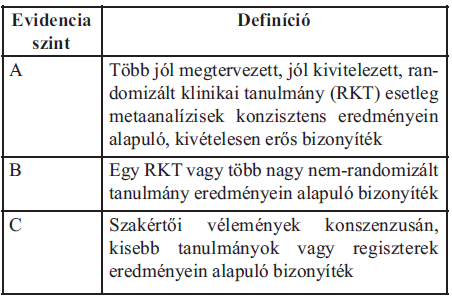
1. táblázat
4. Ajánlások rangsorolása
Az ajánlások besorolása az azokat alátámasztó bizonyítékokon alapul. A fejlesztőcsoport alapvetően az Európai Kardiológus Társaság irányelv ajánlás rangsorolását alkalmazta [3].
Az irányelv szövegében az ajánlások besorolását az ajánlás szövegét követően zárójelben jelöljük (pl. (IIa).

2. táblázat
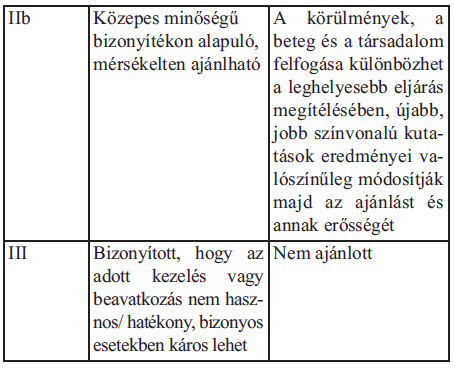
3. táblázat
V. BEVEZETÉS
1. A témakör hazai helyzete, a témaválasztás indoklása
Magyarországon, hasonlóan a világ más fejlett országaihoz, a szív-és érrendszeri betegségek képezik a vezető halálokot. A perifériás verőérbetegség (peripheral arterial disease, PAD), az egész szervezetet érintő, generalizált atherosclerosis egyik megjelenési formája. A PAD prevalenciája a korral nő, nagy populációs vizsgálatok alapján a 30-35 éves korcsoportban kb. 1%, míg 70 év feletti életkorban eléri a 20%-ot. Az érszűkület sokáig semmilyen panaszt nem okoz és sok esetben csak akkor kerül felismerésre, amikor a romló vérellátás következtében a járás erősen korlátozottá válik vagy a lábon nem gyógyuló seb, fekély alakul ki. Ez önmagában is komoly panaszokat, a hétköznapi feladatok ellátásának akadályát jelenti, így jelentős életminőség romlást okoz, súlyos esetben a végtag elvesztéséhez, amputációhoz vezet. Több nagy epidemioló - giai vizsgálat is igazolta, hogy a PAD nagy kardiovasz - kuláris mortalitással jár együtt, mely a claudicatio intermittensben szenvedő ill. a tünetmentes PAD betegekben is, 5 év alatt elérheti a 30 %-ot. Ez a nagy mortalitás a perifériás érbetegek több mint 60 %-ában egyidejűleg fennálló coronaria és carotis elváltozásokkal függ össze. A PAD nemcsak tünetekkel járó esetekben, hanem tünetmentes állapotban is a kardiovaszkuláris ischaemiás események független előrejelzője. Mindezek alapján a PAD felderítése és megfelelő kezelése a kardiovaszkuláris halálozás csökkentésének egyik fontos eszköze.
2. Felhasználói célcsoport
Közvetlen cél az érbetegek ellátásában jelenleg tapasztalható egyenetlenség és szervezetlenség fel számolása, a komplex ellátás folyamatosságának biztosítása minden egyes beteg részére. Az ellátás biztonságát és egyenletesen magasabb színvonalra emelését olyan egységes módszerek alkalmazása/elterjesztése szolgálja, amelyek a gyógyítás eredményessége és költséghatékonysága szempontjából egyaránt megfelelnek a bizonyítékokon alapuló orvoslás (evidence based medicine=EBM) követelményeinek.
Másodlagos cél a jelen ajánlások további alkalmazása más (országos és helyi) eljárásrendek, kapcsolódó folyamatszabályozások (pl.: finanszírozás, belső minőségirányítás, stb.) kidolgozásában.
Az ajánlások hosszabb távú célja a hazai érbeteg ellátás felzárkóztatása, csatlakoztatása az EU-ban (is) kezdeményezett Vaszkuláris Centrumok kialakításával (kritériumai: a multidiszciplínáris diagnosztika, megelőzés, kezelés és követéses gondozás).
3. Kapcsolat a hivatalos hazai és külföldi szakmai irányelvekkel
Egészségügyi szakmai irányelv előzménye:
(Kérjük, a felajánlott lehetőségek közül törölje a nem releváns mondatokat.)
Jelen fejlesztés az alábbi, lejárt érvényességi idejű szakmai irányelv témáját dolgozza fel.
Azonosító: -
Cím: A perifériás obliteratív verőérbetegségek
Nyomtatott verzió: Egészségügyi Közlöny, 2006. évi 5. szám
Elektronikus elérhetőség: https://kollegium.aeek.hu
Kapcsolat külföldi szakmai irányelv(ek)kel:
Jelen irányelv az alábbi külföldi irányelv(ek) ajánlásainak adaptációjával készült.
Szerző(k): Jeffrey L. Anderson, Jonathan L. Halperin, Nancy M. Albert, Biykem Bozkurt, Ralph G. Brindis, Lesley H. Curtis, David DeMets, Robert A. Guyton, Judith S. Hochman, Richard J. Kovacs, E. Magnus Ohman, Susan J. Pressler, Frank W. Sellke, and Win- Kuang Shen
Tudományos szervezet: ACCF/AHA
Cím: Management of Patients With Peripheral Artery Disease (Compilation of 2005 and 2011 Guidelines ACCF/AHA Guideline Recommendations): A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines [1]
Megjelenés adatai: 2013
Elérhetőség: http://circ.ahajournals.org/content/early/ 2013/03/01/CIR.0b013e31828b82aa.citation
Szerző(k): Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG
Tudományos szervezet: TASC II Working Group
Cím: Inter-society consensus for the management of peripheral arterial disease (TASC II) [2]
Megjelenés adatai: J Vasc Surg. 2007; 45(suppl S):S5–S67.
Elérhetőség: http://www.jvascsurg.org/article/S0741-5 214(06)022968/abstract
Szerző(k): European Stroke Organisation, Tendera M, Aboyans V, Bartelink ML, Baumgartner I, Clément D, Collet JP, Cremonesi A, De Carlo M, Erbel R, Fowkes FG, Heras M, Kownator S, Minar E, Ostergren J, Poldermans D, Riambau V, Roffi M, Röther J, Sievert H, van Sambeek M, Zeller T; ESC Committee for Practice Guidelines.
Tudományos szervezet: ESC
Cím: ESC Guidelines on the diagnosis and treatment of peripheral artery diseases [3]
Megjelenés adatai: European Heart Journal (2011) 32, 2851–2906
Elérhetőség: http://eurheartj.oxfordjournals.org/content/ ehj/32/22/2851.full.pdf
Kapcsolat hazai egészségügyi szakmai irányelv(ek)kel:
(Kérjük, a felajánlott lehetőségek közül törölje a nem releváns mondatokat.)
Jelen irányelv nem áll kapcsolatban más hazai egészség ügyi szakmai irányelvvel.
VI. AJÁNLÁSOK SZAKMAI RÉSZLETEZÉSE
1. PAD kórelőzmény és fizikális vizsgálat [3]
Ajánlás 1
A PAD szempontjából veszélyeztetett egyéneket ellenőrizni kell csökkent járástávolság, claudicatio, ischaemiás nyugalmi fájdalom és/vagy nem gyógyuló sebek fennállása szempontjából. (Evidencia szint: C) (I osztályú ajánlás)
A kórelőzmény felvétele során törekedni kell arra, hogy részletesen kikérdezzük a betegek panaszait, tüneteit. Jelen esetben a perifériás artériás betegségre jellemző eltéréseket felfedő, a differenciál diagnózist célzó, az egyéb atheroscleroticus eredetű betegségek esetleges jelenlétére is utaló kérdéseket (angina pectoris, agyi vascularis történés, a bélrendszert ellátó zsigeri artériák szűkülete, vagy elzáródása okozta posztprandiális hasi fájdalom) - kell feltenni. Perifériás obliteratív betegségre van gyanú, ha terhelés közben jelentkezik lábszár, comb, vagy a farpofa izmaiban fájdalom, kellemetlenség, ill. lábzsibbadás. Tisztázandó, hogy a panaszok pihenéssel, álló-, ülő-, fekvő pozícióval, vagy terheléssel függenek össze és a fájdalom pihenésre oldódik-e. Nem gyógyuló, vagy rosszul gyógyuló seb a lábon, lábfejen ugyancsak PAD irányába gyanút keltő tényezőnek számít.
Ajánlás 2
A PAD szempontjából veszélyeztetett egyénekben a láb pulzusok ellenőrzése és a láb megtekintése szükséges. (Evidencia szint: C) (I osztályú ajánlás) A kórelőzmény felvétele után szobahőmérsékletű, jól világított vizsgálóban, a beteget fekvő helyzetben, a végtagokat ruhától mentesen kell vizsgálni. Az inspectio során detektálni kell, hogy egyforma-e a körfogatuk, a szőrzet kornak, nemnek megfelelő-e, nincs-e színeltérés (lividitás, bőrvörösség, sápadság), a körmök nem töredezettek-e, interdigitális mikózis jele látható-e, van-e bármely bőrlézió, seb (gangréna, fekély) a lábakon, vagy lábfejeken. Súlyos PAD-ra utal, ha a szőrzet hiányzik, trofikus bőrelváltozások és hypertrofiás körmök láthatóak.
Az artériák - brachialis, radialis, ulnaris, femoralis, poplitea, dorsalis pedis, tibialis posterior –, valamint a hasi aorta (pulzációja, megnövekedett átmérője) tapintása meg kell, hogy történjen minden esetben. Felső végtagi perfúziós panaszok esetén az Allen teszt elvégzése is szükséges. A tapintott pulzusok intenzitásuk szerint számmal jelölt módon regisztrálandóak; 0=teljesen hiányzik, 1= gyengén tapintható, 2= normális, 3= kemény, peckelő
Ajánlás 3
50 év feletti egyéneknél rá kell kérdezni, hogy elsőfokú rokonaiban előfordult-e hasi aorta aneurysma (AAA). (Evidencia szint: C) (I osztályú ajánlás)
Meg kell kérdezni, hogy aorta aneurysma előfordult-e az első fokú rokonok között.
2. Tünetmentes perifériás érbetegség [4-35]
Ajánlás 4
A csökkent járástávolság, claudicatio, ischaemiás nyugalmi fájdalom és/vagy nem gyógyuló sebek jelenlétének tisztázása szükséges minden 50 év feletti, atherosclerotikus rizikó tényezővel rendelkező egyénnél, ill. minden 65 éves vagy idősebb felnőttnél. (Evidencia szint: C) (I osztályú ajánlás)
A PAD-ra vonatkozó anamnesztikus adatok felvétele, vagy a lábakon lévő sebek tisztázása szükséges azon 50 év feletti személyeknél, akiknél az érelmeszesedésre vonatkozó kockázati tényezők megtalálhatóak, ill. minden 65 éves, vagy attól idősebb felnőtt esetén.
Tünetmentes lehet az a személy, akinek egyáltalán nincs panasza, vagy hiányoznak a klasszikus claudicatio inter - mittenst (CI) jellemző panaszok, de jelentős a végtag funkció romlása és fokozott az egyéb ischemiás események rizikója. Megtévesztő lehet, ha más okból alakul ki fájdalom (pl.:lumbalis discopathia, spinalis stenosis), ill. egyéb alsó végtagokat érintő kórkép (izombetegség, neuropathiavagy compartment szindroma) áll fenn.
Epidemiológiai felmérések során claudicatio intermittens regisztrálására korábban a WHO Rose féle kérdőívet, majd annak Edinburgh-i (1.táblázat),ill. azt követően San Diego-i módosított formáját használták. A kérdőív a szűrővizsgálat első lépcsője, azt mindig kell követnie további vizsgálatoknak.
Ajánlás 5
A tünetmentes perifériás verőérbetegséget a bokakar index (BKI) meghatározásával kell igazolni, hogy a betegeknek felajánlhassák azokat a terápiás lehetőségeket, amelyek csökkentik a megnövekedett miokardiális infarktus (MI), stroke és halál rizikóját. (Evidencia szint: B) (I osztályú ajánlás)
Californiában végzett vizsgálatból az derült ki, hogy a férfiak 2,2%-ában, a nők 1,7%-ában volt típusos CI, míg a PAD előfordulása 11,7%-nak bizonyult. A bizonyított PAD betegek kb. 10%-ának volt típusos panasza, további vizsgálat nélkül 91%-uk felderítetlen maradt volna. Ugyanezen tanulmányban megvizsgálták a pedál pulzusok eltérő tapintásának validitását. Azt találták, hogy férfiak 20,3%-ában, nők 22,1%-ában mutatkozott abnormális pulzus. A palpatio felül értékelte a prevalenciát. A Rotterdam tanulmányban 7715 55 évnél idősebb személy vizsgálatakor a CI előfordulása 1,6% volt, a 0,9 alatti boka/kar indexűek 19,1%-nak bizonyultak. Ezen esetben még a 10%-t sem érte el a típusos panaszosok aránya. A nem típusos láb- panaszok jelentőségére hívta fel a figyelmet a PARTNERS tanulmány; a korábban diag - nosztizált PAD betegek 26%-ban teljesen panaszmentesek voltak, 62%-ban volt atípusos a panasz és csak 13%-ban mutatkozott típusos CI. Az újólag diagnosztizált csoportban 48% bizonyult panaszmentesnek, az atípusos panasz 46% volt és csak 6%-ban mutatkozott típusos CI.
McDermott és munkatársai azt is bebizonyították, hogy a tünetmentes csoport 63%-ában még terheléssel sem volt kiváltható CI, ugyanakkor az alsó végtagok egyéb funkció romlását (csökkent járássebesség, mérsékeltebb egyen - súlyozási képesség) konstatálták. A Cardiovascular Health Study eredményei ugyancsak a tünetmentesek alsó végtagi teljesítőképességűk csökkenéséről számoltak be. Hazánkban is történt 21 892 50-75 éves hypertoniás személy szűrése tünetmentes perifériás artériás betegségre, akik közül 14,4% bizonyult PAD betegnek. Az adatok arra utalnak, hogy gyakori a tünetmentesség, ill. az atípusos panaszok előfordulása, ezért a kérdőíves és fizikális vizsgálatokat objektív vizsgáló eljárással ki kell egészíteni mindazon 50 év feletti személyeknél, akiknél az érelmeszesedésre vonatkozó kockázati tényezők megtalálhatóak, ill. minden 65 éves, vagy attól idősebb felnőtt esetén.
Nagyon lényeges, hogy minél hamarább detektáljuk a PAD jelenlétét boka/kar index meghatározással - amely egyszerű, olcsó és megbízható nem invaziv vizsgáló eljárás - hogy azonnal meg lehessen kezdeni a kockázati tényezők kezelését, ezzel esélyt adva a hosszabb túlélésnek és a jobb életminőséghez való hozzájutásnak. A beteget a diagnózis felállításakor részletesen tájékoztatni kell a kórlefolyásról, a várható vascularis eseményekről, az életkilátásról, az érintett végtag bekövetkezhető ischemiás állapotáról. Keresni szükséges az egyéb atheroscleroticus eredetű kórképek, úgymint ISZB, carotis szűkület jeleit és fel kell ajánlani a rizikó elimináció lehetséges módozatait.
Ajánlás 6
Tünetmentes PAD betegeknek ajánlott a dohányzás abbahagyása, lipid csökkentő kezelés, a magyar irányelveknek megfelelő diabetes és hypertonia kezelés. (Evidencia szint: B) (I osztályú ajánlás)
A PAD az atherosclerosis egyik manifesztációjának tekinthető. Kockázati tényezői, úgymint a dohányzás, diabetes mellitus, dyslipidemia, hypertonia, elősegítik a kórképnek, valamint az egyéb atheroscleroticus eredetű betegségeknek a kialakulását és progresszióját.
A tünetmentes PAD személyek prognózisa nem nevezhető benignusnak, mivel a jelen lévő atherosclerosis kockázati tényezők lényegében a tünetes egyénekével megegyező. Többnyire nagy prevalenciájú a diabetes, a dohányzás, a hypertonia és hypercholesterinemia és jelzetten több a cardiovascularis események rátája is.
A dohányzás igen erőteljes etiológiai rizikó faktora az alsó végtagi obliterativ artériás betegségnek, 2-3x nagyobb valószínűséggel hat e kórkép kialakulása irányában, mint a corocariasclerosis létrejöttére. Dohányosok esetén 3-10x nagyobb mértékben alakul ki a claudicatio intermittens a nem dohányzókhoz képest. A PAD betegek több, mint 80%-a leszokott, vagy aktív dohányos. A dohányzás intenzitása dózis-dependens – napi cigaretta szám és időtartam - módon növeli a PAD rizikóját.
A hazai V.Kardiovaszkuláris Konszenzus Konferencia kimondta: A dohányzás abbahagyásához történő segítségnyújtás az egészségügyi ellátás része. A betegellátásban résztvevő minden orvosnak el kell sajátítania a leszokást segítő, bizonyítottan hatásos módszerek alkalmazását, beleértve a farmakoterápia és a magatartás terápia módszereit. Minden beteg-orvos találkozás alkalmával tisztázni kell, hogy a beteg dohányzik-e és a dohányzó betegnek határozottan és egyértelműen javasolni kell a dohányzás abba hagyását és ehhez segítséget kell felajánlani.
Diabetes mellitusos egyéneken nagy nemzetközi felmérések szerint 2-4x nagyobb előfordulású a PAD a nem diabetesesekhez képest, a Framingham Study eredményei 3,5-8,6-szoros értéket mutatnak. A diabetes súlyossága és fennállásának ideje befolyásolja a kórkép kialakulását, annak progresszióját, valamint az is bebizonyosodott, hogy sokkal több a kritikus végtag ischemia megjelenése a diabeteses betegek között és 7-15x nagyobb arányú az alsó végtagi major amputació. A hazai VI.Kardiovaszkuláris Konszenzus Konferencia meghatározta diabetes mellitus esetén a célértékeket, melyek a következők: éhomi vércukor:<6,0mmol/l, postprandiális vércukor:< ,5mmol/l, HbA1c: 6-8,0%.
A zsír anyagcsere eltérései közül az emelkedett össz-, LDL-koleszterin, a csökkent HDL-koleszterin és hyper - triglyceridemia kockázati tényezőt képez a PAD kialakulásában és előrehaladásában. Az összkoleszterin 10mg/dl emelkedése 5-10 %-kal emeli meg a PAD kialakulását. Számos epidemiológiai tanulmány szerint a PAD betegek összkoleszterin szintje jelentősen magasabb azon egyénekéhez képest, akiknek nincs perifériás érbetegségük. A hazai VI.Kardiovaszkuláris Konszenzus Konferencia a PAD betegeket a nagy vagy igen nagy rizikójú csoportba sorolta, a javasolt célértékek nagy rizikó esetén: összcholesterin:<4,5mmol/l, LDL-cholesterin: <2,5mmol/l, triglicerid:<1,7mmol/l, HDL-cholesterin: >1,0mmol/l (férfi),>1,3mmol/l (nő)
A hypertonia a Framingham Study adatai szerint 2,5-4x növeli a claudicatio intermittens kialakulását és a hypertonia súlyosságával arányos a kockázat.
A Magyar Hypertonia Társaság ajánlása szerint a PAD betegek vérnyomása Fontaine II.stádiumban 140/90 Hgmm alatt tartandó.
A hypertonia a Framingham Study adatai szerint 2,5-4x növeli a claudicatio intermittens kialakulását és a hypertonia súlyosságával arányos a kockázat. A Magyar Hypertonia Társaság ajánlása szerint a PAD betegek vérnyomása Fontaine II.stádiumban 140/90 Hgmm alatt tartandó.A hypertonia a Framingham Study adatai szerint 2,5-4x növeli a claudicatio intermittens kialakulását és a hypertonia súlyosságával arányos a kockázat. A Magyar Hypertonia Társaság ajánlása szerint a PAD betegek vérnyomása Fontaine II.stádiumban 140/90 Hgmm alatt tartandó.
Ajánlás 7
Terheléses boka-kar index (BKI) mérés hasznos lehet az alsóvégtagi PAD megállapításában, azokban a betegekben, akiknek a BKI értéke normális (0.91 - 1.30), nincsen klasszikus klaudikációs tünetük és nincs más ismert atherosclerotikus betegségük. (Evidencia szint: C) (IIa osztályú ajánlás)
Terhelést követően reaktiv hyperemia jön létre a normál érrendszerben, amely mind a felső, mind az alsó végtagban fokozza az áramlást. Ily módon ép érrendszerű egyéneken közvetlenül a terhelés után végzett BKI értéke nem változik. Alsó végtagi artériás stenosis esetén – amikor a nyugalmi érték normális, vagy határértékű - a szisztémás nyomás megnövekszik, de a boka-nyomás változatlanul marad, következésképpen a BKI csökkenni fog. Főleg jól kompenzált, nagy artériák szegmentális occlusiója adja ezt az eltérést.
Ajánlás 8
Az ujj-kar index mérés hasznos lehet az alsóvégtagi PAD megállapításában, azokban a betegekben, akiknek a BKI értéke nagyobb, mint 1.30 és nincs más ismert atherosclerotikus betegségük. (Evidencia szint: C) (IIa osztályú ajánlás)
Krónikus vesebetegség, diabetes mellitus hosszan tartó fennállása és idős kor esetén az artériák falában media - sclerosis alakulhat ki, amely lehetetlenné teszi a BKI kivitelezését. Nem, vagy csak nagy nyomással komprimálhatóak a cruralis erek, ezért az a. dorsalis pedis, vagy/és az a.tibialis posterior nyomásértéke magas, így az index 1,3 feletti lesz. Ilyen esetben öregujj/karindex értéke a mérvadó; a halluxon, vagy a II. lábujjon lehet erre alkalmas mandzsettátval nyomást mérni, melyet osztunk a karon mért szisztolés értékkel. A 0,6 alatti szint utal PAD-ra.
Ajánlás 9
Tünetmentes PAD betegeknek ajánlott a thrombo - cyta aggregáció gátló kezelés a kardiovaszkuláris események megelőzése céljából. (Evidencia szint: C) (IIa osztályú ajánlás)
Az Antithrombotic Trialists’ Collaboration 135 000 magas rizikójú személynél vizsgálta meg az aspirin cardiovascularis eseményeket befolyásoló hatását. Azt találták, hogy 22%-ban csökkentette az adverz cardiovascularis eseményeket és a vascularis halálozást. A vizsgálat részét képező 9716 PAD személy esetében ez a csökkenés 23% volt. Metaanalízis során összevetették több aspirin adag hatását. A napi 75-150mg dózis hozta a legmagasabb – 35% - vascularis esemény csökkenést. Kisebb aspirin adag lényegesen kisebb hatású volt (13%), a nagyobb dózisoknál növekedett a vérzéses mellékhatás. A CAPRI tanulmányban öszehasonlították az aspirin és a clopidogrel hatását 19 185 atheroscleroticus betegségben szenvedő egyénen; a clopidogrel 8,7%-kal jobban csökkentette a cardio - vascularis eseményeket az egész vizsgált populációban, a PAD betegek esetében a csökkentés 23,8%-kal nagyobb mérvű volt, mint az aspirin hatása. A perifériás artériás érocclusiot az aspirin nem mérsékelte.
A fenti tanulmányok nagy számú adata alapján kell határozottan ajánlani kimutatott kórkép esetén - akár tünetes, akár tünetmentes - a napi 75-150mg aspirint, vagy 75mg clopidogrelt alternativ thrombocyta aggregáció gátlóként.
3. Claudicatio intermittens [3, 35-39]
Ajánlás 10
Claudicatio intermittens (CI) esetén vaszkuláris fizikális vizsgálat szükséges, beleértve a BKI mérését. (Evidencia szint: B) (I osztályú ajánlás)
A claudicatio intermittens alapja a terheléssel létre hozott ischemia egy adott izomcsoportban, mely fáradságot, diszkomfort érzést, fájdalmat eredményez. Nyugalomban a vérellátás helyre áll, a panaszok oldódnak. Az elzáródás helyének megfelelően típusos tünetek jelentkeznek; az iliaca artériák szűkülete, vagy elzáródása a csípőben, a far izomzatban és a combban, esetleg a lábszár izom zatban okoz fájdalmat, a femoralis és poplitea artériák occlusioja többnyire a lábszár izomzat fájdalmát generálja. A tibialis artériák elzáródása ugyancsak a lábszár izomzat vérellátási zavarához, következésképpen itt jelentkező fájdalomhoz vezet, ill. jelentkezhet fájdalom és zsibbadás a lábfejben. Az ischemia súlyosságát Fontaine és Rutherford kategorizálta (2. táblázat).
A láb fájdalmat számos egyéb kórkép, alteráció is létrehozhatja. A differenciál diagnózist a 3. táblázat adatai segíthetik.
Claudicatio intermittens esetén meg kell történnie a kórtörténet precíz felvételének, melynek tartalmaznia szükséges a panaszok kezdetét, dinamikáját, a családi angiológiai anamnézist, a rizikó tényezők – dohányzás, hypertonia, diabetes, dyslipidemia – regisztrálását, a fizikális vizsgálatot, a látható eltérések leírását, az összes tapintható artéria pulzusának minősítését és az artériás zörejek észlelését. A fizikális vizsgálatot minden esetben a boka/kar index meghatározása követi.
Ajánlás 11
CI esetén a BKI mérést terhelést követően is el kell végezni, amennyiben a nyugalmi index normális. (Evidencia szint: B) (I osztályú ajánlás)
Amennyiben meglévő claudicatio intermittens ellenére a BKI normál értéket mutat, akkor felmerül pseudo CI lehetősége, melyet terhelést követő BKI meghatározással lehet kizárni, ha normalizálódik az index, akkor PAD kizárható. Az artéria iliakak, femoralisok szegmentális, jól kompenzált elzáródása járhat normális nyugalmi BKI-szel, de terhelést követően kóros értéket kapunk.
Ajánlás 12
Revaszkularizáció a CI azon eseteiben mérlegelendő, amikor szignifikáns funkció csökkenés áll fenn és jó esélye van a tünetek javulásának, valamint nem áll fenn egyéb, a fizikai aktivitást gátló betegség (pl. angina, szívelégtelenség, idült légzőszervi betegség, vagy orthopediai elváltozás). (Evidencia szint: C) (I osztályú ajánlás)
A claudicatio intermittens mértéke, foka nagyban meghatározza a PAD betegek életminőségét. Alacsony járás távolság esetén felmerül a revascularisatio lehetősége, át kell tekinteni a további teendőket. Ilyen esetben keresni kell az atheroscleroticus társbetegségeket –ISZB, szívelégtelenség, arteria renalis szűkűlet, vese elégtelenség, carotis stenosis okozta cerebrovascularis elégtelenség – gerinc betegségeket, izületi eltéréseket, hiszen e betegségek jelenléte jelentős mozgáskészség csökkenéssel járhat és a beavatkozás nem hoz eredményt [36]. Azt is figyelembe kell venni, hogy a PAD a végtagok vitalitását illetően egy relatíve benignus kórkép, a kritikus láb ischemia kialakulása, láb amputáció kis arányban fordul elő, tehát minden invazív beavatkozás alaposan mérlegelendő [37, 38].
Ajánlás 13
Azok az IC-ban szevedő betegek, akiknek feljánlják az endovasculáris vagy sebészi kezelést:
(a) kellő információt kell kapjanak a kontrollált tréning terápiáról és a gyógyszeres kezelésről;
(b) átfogó rizikócsökkentő és thrombocyta gátló kezelést kell kapjanak;
(c) olyan szignifikáns járás csökkenéssel kell rendelkezzenek, amely a normális munkavégzést, életvitelt vagy más, a beteg számára fontos tevékenységet; és (d) olyan kell legyen a PAD lézió anatómiája, amelyben a revaszkularizációs beavatkozás kockázata alacsony és nagy a valószínűsége a kezdeti és hosszú távú sikernek. (Evidencia szint: C) (I osztályú ajánlás)
Amennyiben a fizikai tréning program, az életmódi változtatások nem hoztak lényeges javulást és a fentiek átgondolása megtörtént, valamint a tervezett beavatkozás feltételei adottak, akkor lehet tervezni a revascularisatiót.
a. Minden beavatkozás előtt ismernie kell a betegnek az életmód változtatás várható eredményeit, a farmakoterápiás lehetőségeket és a fizikai tréning javító hatását.
b. A beavatkozás időpontja akkorra tehető, amikor a vérnyomás elfogadható értéken van, a diabetes kompenzáltsága detektálható, a lipidek célértéken vannak, a dohányzásról való leszokás folyik, vagy a tervek között szerepel.
c. Akkor kell a beavatkozás tervezésével foglalkozni, ha a csökkent járásképesség a személyt gátolja a munkájában, társadalmi kapcsolatainak vitelében, egyéb feladatainak végzésében. A biológiai életkort kell alapul venni. Nem végzendő beavatkozás olyan személyekben, akik számára a kisebb járás távolság is megfelelő (pl. idős egyén, aki lakásban mozog csupán), a mozgáskészség javulása nem jelentene az életvitelében változást.
d. A kivizsgálást, ha beavatkozás szükségessége merül fel, úgy kell kibővíteni, hogy egyértelműen tisztázható legyen a szűkület, vagy elzáródás anatómiai elhelyez - kedése. Meg kell határozni, hogy rekonstrukciós beavat - kozásként percutan angioplasztika, vagy érsebészeti eljárás az első választandó beavatkozás. A lehetőségekről, a várható becsült közeli és távolabbi eredményről a beteget tájékoztatni szükséges.
4. Kritikus végtag ischaemia [1-3]
Ajánlás 14
Kritikus végtag ischaemiában (KVI) szenvedő betegekben gyorsított módon kell értékelni és kezelni azokat a tényezőket, amelyek növelik az amputáció rizikóját. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 15
KVI- ban szenvedő betegekben, amennyiben nyitott sebészi beavatkozás várható, szükséges a kardiovasz kuláris rizikó értékelése. (Evidencia szint: B)
Ajánlás 16
A korábban KVI-án átesett betegek esetében évente legalább 2 alkalommal szakorvosi ellenőrzés szükséges, tekintettel a kiújulás relatíve nagy incidenciájára. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 17
A KVI szempontjából veszélyeztetett betegekben (BKI <0.4 diabeteses betegben, ill. diabetes és ismert PAD fennállása) a lábak rendszeres ellenőrzése szükséges a KVI objektív tüneteinek felismerése céljából. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 18
KVI sikeres kezelését követően a láb rendszeres direkt (cipő és zokni nélküli) ellenőrzés szükséges. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 19
KVI és atheroembolizáció gyanuja esetén ki kell zárni az aneurysmatikus elváltozásokat (pl. hasi aorta, poplitea, vagy femoralis aneurysmák). (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 20
KVI, bőr fekély és nyilvánvaló végtag infekció esetén azonnal szisztémás antibiotikus kezelést kell kezdeni. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 21
KVI és bőrnekrózis esetén a beteget sebkezelésben jártas szakemberhez kell irányítani. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 22
A KVI szempontjából veszélyeztetett betegek esetében az akut végtag panaszok jelentkezése potenciális vaszkuláris sürgősségi állapotot jelezhet, ezért az ilyen betegek esetében azonnali szakorvosi vizsgálat ill. kezelés szükséges. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 23
A KVI szempontjából veszélyeztetett vagy azon már átesett betegek oktatásban kell részesüljenek az önellenőrzésről, a kiújulás lehetősége miatt. (Evidencia szint: C)
(I osztályú ajánlás)
5. Akut kritikus végtag ischaemia [2,3]
Ajánlás 24
Akut végtag ischaemia és menthető állapotú végtag esetén a beteg sürgős vizsgálata javasolt az elzáródás szintjének megállapítására az azonnali endovaszkuláris vagy sebészi revaszkularizáció céljából. (Evidencia szint: B) (I osztályú ajánlás)
6. Korábbi végtagi artériás revaszkularizáció [2,3]
Ajánlás 25
Az infrainguinális bypass graft hosszútávú átjárhatóságát gondozási program keretében kell ellenőrizni, mely magában foglalja az időszakos érpanaszok kikérdezését, nyugalmi BKI mérést, ill. szükség esetén a Duplex Ultrahang vizsgálat (DUS) végzését, amennyiben véna graft került felhasználásra. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 26
Az infrainguinális bypass graft hosszú távú átjár - hatóságának ellenőrzésére megfontolható egy gondozási program, mely rendszeres időközökben terheléses BKI mérést és más artériás képalkotó vizsgálatokat tartalmazhat. (Evidencia szint: B) (IIa osztályú ajánlás)
Ajánlás 27
Az endovaszkuláris beavatkozás helyének hosszú távú átjárhatóságának ellenőrzésére megfontolható egy gondozási program, mely rendszeres időközökben terheléses BKI mérést és más artériás képalkotó vizsgálatokat tartalmazhat. (Evidencia szint: B) (IIa osztályú ajánlás)
7. Diagnosztikus módszerek [1, 40-55]
7.1. Boka-kar index és ujj-kar index
Ajánlás 28
Nyugalmi BKI mérés ajánlott alsóvégtagi PAD gyanúja esetén a következő esetekben: terhelésre jelentkező alsóvégtagi panasz, nem gyógyuló seb, 65 éves vagy e feletti életkor, 50 év feletti életkor és legalább egy ismert rizikó tényező jelenléte. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 29
A BKI-t mindkét alsóvégtagon meg kell mérni minden új PAD betegben, függetlenül a súlyosságtól, a diagnózis igazolása és egy alap érték meghatározása céljából. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 30
Azokban az esetekben, amikor PAD gyanúja fennáll, de a BKI nem komprimálható erek (általában diabetes, idős kor, krónikus vesebetegség) miatt nem megbízható ajánlott az ujj-kar index megállapítása. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 31
A BKI-t egységesen kell értékelni: nem komprimálható erek 1.4 felett, normál érték 1.00-1.40, határérték: 0.91-0.99, kóros 0.90 vagy ez alatt. (Evidencia szint: B) (I osztályú ajánlás)
A perifériás verőérbetegség diagnózisa egyszerűen felállítható a boka/kar index meghatározásával. A boka/kar index (BKI) a boka magasságában, ill. a felkaron mért systolés vérnyomás hányadosa. A nyomás meghatározására folyamatos hullámú (CW) Doppler készülék használata ajánlott. A BKI normál értéke fekvő helyzetű betegben 1,0-1,4, kórosnak tekintjük, ha az index < A BKI értékének csökkenése korrelációt mutat a betegség progressziójával, ill. klinikai stádiumaival. A BKI szenzitivitása és specificitása a PAD megállapítására igen magas, meghaladja a 90%-ot. A vizsgálat menete a következő:
- A vizsgálat előtt a vizsgált személy legalább 5 percet vízszintesen kell, hogy feküdjön
- Folyamatos hullámú Doppler áramlásmérőt (CW Doppler, 5-10 MHz) kell használni
- A mérőfejet 60°- os szögben kell tartani.
- A mérést az egyik karon kell kezdeni, az azonos oldali alsóvégtagon, majd a másik alsó végtagon folytatni, végül a másik kar nyomás mérésével befejezni. A karon az arteria brachialis-ban, vagy az arteria radialis-ban kell megmérni a szisztolés vérnyomást, a két oldal közül a magasabb értekkel kell számolni. Amennyiben a két kar nyomása között 10 Hgmm-nél nagyobb a különbség, a mérést az első karon meg kell ismételni.
- A boka magasságában az arteria tibialis posterior-ban, majd az arteria dorsalis pedis-ben kell megmérni a szisztolés nyomást, a mandzsettát közvetlenül a boka felett felhelyezve, a két éren mért érték közül a magasabb értékkel kell számolni.
- A felkar és boka mandzsetta azonos méretű kell, hogy legyen.
- Mindig a leeresztésnél kell mérni, soha a felpumpá - lásnál.
- A mandzsettát lassan kell leereszteni (2 Hgmm/sec).
A BKI úgy számítható ki, hogy az adott alsó végtag bokánál mért magasabb szisztolés nyomását elosztjuk a felső végtagon mért magasabb szisztolés nyomással.
A BKI mérése korlátozott lehet, amikor a cruralis erek diffúz sclerosisa következtében az artériák nem komprimálhatók és emiatt a boka magasságában fals magas értéket kapunk, ilyenkor a mérés nem értékelhető. Ez az állapot a Mönckeberg-féle mediasclerosis, amely jellemző diabetes mellitus, végállapotú veseelégtelenség, idős kor esetén. Ezekben az esetekben kiegészítő műszeres vizsgálatok szükségesek a diagnózis felállításához (Doppler görbe értékelés, az öregujjon mért szisztolés nyomás mérése, artériás duplex ultrahang vizsgálat).
7.2. Folyamatos hullámú (CW) Doppler vizsgálat
Ajánlás 32
A folyamatos hullámú Doppler áramlásmérés alkalmas az alsóvégtagi PAD helyének és súlyosságának pontos megítélésére, a progresszió követésére, és a revaszkularizációt követő kvantitatív követésre. (Evidencia szint: B) (I osztályú ajánlás)
A folyamatos hullámú Doppler vizsgálat lehetőséget nyújt az áramlási görbe regisztrálására és ez által információt nyújt az érbetegség helyéről és súlyosságáról. Az alsó végtagon distal felé haladva a magas rezisztenciájú erekre jellemző trifázisos áramlási görbe amplitúdója csökken, de a görbe alakja változatlan marad. Szűkület fennállása esetén az áramlási görbe az elváltozástól proximálisan normális. A stenosis mértékétől függően az elváltozásnak megfelelően az áramlási sebesség gyorsul, bifázisossá válik, tőle distalisan bifázisos, csökkent amplitúdójú áramlás detektálható. A Doppler görbe kvantitatív értékelésére alkalmas a pulzatilitási index (PI= csúcs systolés sebesség és a legkisebb diastolés sebesség különbsége osztva az átlagsebességgel), mely normálisan distal felé haladva nő. A mennyiben két szegmentum között distal felé haladva a PI csökken, ez szűkületre, vagy elzáródásra utal. A végtag több pontján végzett vizsgálattal a szűkület vagy elzáródás helye megállapítható.
7.3. Járópadló terhelés teszt BKI méréssel vagy anélkül, 6 perces járás teszt
Ajánlás 33
A járópadló terhelés teszt ajánlott a járástávolság objektív megállapítására és a terápiás válasz lemérésére. (Evidencia szint: B) (I osztályú ajánlás)
A terheléses tesztek hasznosak lehetnek a következő esetekben:
- alsó végtagi PAD diagnózisának megállapítására, ha a nyugalomban mért BKI normális, ill. alsó végtagi PAD elkülönítésére egyéb, terhelésre jelentkező alsó végtagi fájdalommal járó megbetegedésektől,
- a tünet limitált járástávolság és ennek terápia hatására bekövetkezett változásának objektív dokumentálására,
- kontrollált tréning program előtt a tervezett tréning egyéni megtervezésében.
Ajánlás 34
Motorizált járópadló és standardizált terhelési protokoll használata javasolt a fájdalom mentes és a maximális járástávolság megállapítására. (Evidencia szint: B) (I osztályú ajánlás)
Ha terhelést PAD betegek funkcionális kapacitásának felmérése, terápiájuk hatásának lemérése céljából végezzük, akkor különböző protokollok szerinti, fix vagy egyre növekvő terhelés alkalmazható.
A járópadló terhelés során a rögzíteni kell a fájdalommentes- és maximális járástávolságot, a panaszok oldaliságát, a panaszok által érintett izomcsoportot (glutealis, comb stb.), a teljes járási időt, valamint a terhelést limitáló panaszt (típusos claudicatiós fájdalom, atípusos végtagi fájdalom, izületi fájdalom, általános gyengeség, mellkasi fájdalom, nehézlégzés stb.).
Ajánlás 35
Terhelés előtti és utáni BKI méréssel kombinált járópadló terhelés javasolt az artériás és a nem artériás claudicatio elkülönítésére. (Evidencia szint: B) (I osztályú ajánlás)
Ha a terhelés diagnosztikai, differenciáldiagnosztikai céllal történik, akkor a teszt után ismét meg kell határozni a BKI-et. Egészségesekben terhelés után közvetlenül a BKI nem változik (a felkari és a bokánál mért vérnyomás párhuzamosan emelkedik), alsó végtagi PAD fennállása esetén a terhelés indukálta ischaemiás vasodilatatio hatására nyomásgrádiens képződik a stenoticus érszakaszon keresztül, ami a BKI szignifikáns csökkenését eredményezi.
Ajánlás 36
Ellenőrzött tréning program előtt terheléses járópadló teszt elvégzése javasolt a funkcionális kapacitás megállapítására, a nem vaszkuláris eredetű akadályozó tényezők értékelésére, ill. a terhelés biztonságosságának igazolása céljából. (Evidencia szint: B) (I osztályú ajánlás)
Az ellenőrzött tréning program előtti járópadló terhelés részleteit a 9.1. fejezetben tárgyaljuk.
Ajánlás 37
A 6 perces séta teszt hasznos lehet a claudicatio okozta funkcionális korlátozottság megállapítására és a terápiás válasz lemérésére idős egyéneknél és más járópadló tesztre alkalmatlan betegek esetében. (Evidencia szint: B) (IIb osztályú ajánlás)
Irodalmi adatok szerint, amennyiben a járópadló terhelés - a beteg társbetegsége, kora, vagy a megfelelő tárgyi vagy személyi feltételek hiánya miatt - nem kivitelezhető, helyette alternatívaként a 6 perces séta teszt is elégséges információval szolgálhat a betegek mindennapi funkcionális járásteljesítményéről és annak változásáról.
7.4. Képalkotó vizsgálatok [3, 56,57]
Ajánlás 38
A végtagi Duplex Ultrahang (DUS) hasznos a PAD lokalizációjának és a szűkület mértékének meghatározására. (Evidencia szint: A) (I osztályú ajánlás)
A végtagi Duplex UH (DUS) eljárás a végtagi artériák szűkületének jellemzésén túl alkalmas az érfali kalcifikáció, az aneurizmák, disszekciók, az ereket körülvevő szövetek vizsgálatára is. A szűkületek megítélése döntően a szűkületekben létrejövő áramlás gyorsulás mérésén alapul. A csúcs szisztolés sebesség, illetve a szűkületek előtti és utáni szisztolés áramlási sebesség arányának meghatározása az artéria iliaca-tól az arteria poplitea szintjéig 90-95%-os szenzitivitással, specificitással képes jelezni az 50%-ot meghaladó szűkület jelenlétét. A kimutathatóság korlátját jelentheti a nem megfelelő vizualizáció (belek gázossága, súlyos érfali kalcifikáció), valamint a többszörös szűkületek egymásutánja
Ajánlás 39
A DUS ajánlott a femoro-poplitealis és femorotibialispedalis véna bypass rutin ellenőrzésére. Az ellenőrzés a beavatkozás után 3, 6 és 12 hónappal, majd évente javasolt. (Evidencia szint: A) (I osztályú ajánlás)
A végtagi ér szűkületének kimutatásán túl a Duplex UH eljárás alkalmas lehet sebészi vénás bypass-ok ellenőrzésére, bár az ezt vizsgáló tanulmányok eredményei nem konzisztensek . A nem egyértelmű evidenciák ellenére a gyakorlat széles körben elterjedt, általában a beavatkozást követő 4-6 hét múlva, majd 3 havonként az első évben, ezt követően évente. Az eljárás nem javasolható a percutan transluminalis angioplastica és a szintetikus femoropoplitealis bypass átjárhatóságának rutin ellenőrzésére.
Ajánlás 40
A DSA, CTA, MRA vizsgálatok egyaránt alkalmasak a PAD anatómiai lokalizációjának és szignifikáns szűkület fennállásának megállapítására, valamint a revascularizációs lehetőségek megítélésére. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 41
Azokban a betegekben, akiknél revascularizáció indikált, az érintett artériás rendszer képalkotó vizsgálatai során ábrázolódott anatómiai viszonyok és a noninvazív, haemodynamikai tesztek eredményének összevetése alapján kell dönteni a terápiáról. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 42
A korábbi kontrasztanyag okozta reakciót dokumentálni kell a DSA vizsgálat előtt és megfelelő előkezelést kell alkalmazni a kontrasztanyag beadása előtt. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 43
Veseelégtelenségben szenvedő betegek a kontraszt angiographia előtt hydratioban kell részesüljenek. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 44
Noninvazív képalkotó eljárások, mint MRA, CTA ill. color DUS alkalmazhatóak az invazív képalkotás (DSA) előtt, az egyéni diagnosztikus stratégia (bemeneti hely kiválasztás, szignifikáns lézió azonosítás) és az invazív vizsgálat szükségességének megállapítására. (Evidencia szint: B) (IIa osztályú ajánlás)
Ajánlás 45
N-acetylcystein kezelés ajánlott a kontraszt angiographia előtt veseelégtelen beteg esetében (serum kreatinine >176 Ęmol/l). (Evidencia szint: B) (IIa osztályú ajánlás)
8. Kardiovaszkuláris rizikót csökkentő kezelés [58-87]
8.1. Lipid csökkentő szerek
Ajánlás 46
Statin kezelés indikált minden PAD betegnek a 2,5 mmol/l alatti LDL-koleszterin ill. a 4,5 mmol/l alatti össz-koleszterin célérték elérésére. (Evidencia szint: B) (I osztályú ajánlás)
A statin kezelés csökkenti a halálozás és a kardiovaszkuláris események perifériás verőérbetegségben szenvedő betegekben függetlenül a coronariabetegség meglététől. A Heart Protection Study-ban résztvevő 6748 perifériás verőérbeteg 5 éves utánkövetése során a sim - vastatin kezelésben részesülők között 19%-os relatív és 6,3%-os abszolút kockázatcsökkenés volt megfigyelhető függetlenül a kortól, nemtől, valamint serum lipid szinttől. A statin kezelés javíthatja a perifériás verőérbetegek tüneteit is, így például a 4S (Scandinavian Simvastatin Survival Study) vizsgálat retrospektív analízise azt mutatta, hogy simvastatin kezelés hatására az új, vagy romló caludicatio kockázata csökken. Atorvastatinnal végzett prospektív vizsgálat is azt mutatta, hogy atorvastatin hatására nőtt a fájdalommentes (de nem a maximális) járástávolság.
Ajánlás 47
Igen nagy kardiovaszkuláris kockázatú PAD betegeknek statin kezelés ajánlott az 1,8 mmol/l alatti LDL-koleszterin ill. a 3,5 mmol/l alatti össz-koleszterin célérték elérésére. (Evidencia szint: B) (IIa osztályú ajánlás)
Ajánlás 48
Fibrát kezelés hasznos lehet azoknak a PAD betegeknek, akiknél alacsony HDL-koleszterin, normális LDL-koleszterin és emelkedett triglicerid szint van jelen. (Evidencia szint: C) (IIa osztályú ajánlás)
A fibrátok, koleszterinkötők és a niacin kardiovaszkuláris kockázatcsökkentő hatékonysága perifériás verőérbetegekben nem ismert.
8.2. Vérnyomáscsökkentő kezelés
Ajánlás 49
Antihipertenzív terápia ajánlott hypertoniás PADbetegek esetében a<140/90 Hgmm célvérnyomás eléréséhez a szívinfarktus, a stroke, a szívelégtelenség és a CV halálozás kockázatának csökkentése érdekében (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 50
PAD esetében elsősorban a kalciumantagonisták és ACE-inhibitorok alkalmazása javasolt, mert ezek a szerek hatékonyabbak az atherosclerosis progressziójának késleltetésében, mint a diuretikumok és a ß-blokkolók. (Evidencia szint: B) (IIa osztályú ajánlás)
Nagykockázatú betegekben az angiotenzin konvertáló enzimgátló (ACE-gátló) kezelésnek a vérnyomáscsökkentő hatáson felül is igazolható előnyös hatása. A Heart Outcomes Prevention Evaluation (HOPE) vizsgálatban az ACE-gátló ramipril kezelés a kardiovaszkuláris események (szívinfarktus, halál, vaszkuláris események) arányát 25%-kal csökkentette azon tüneteket mutató perifériás verőérbetegekben is, akik nem voltak szívelégtelenek. Ebben a betegcsoportban a ramiprillel ekvivalens hatású volt a telmisartan egy másik vizsgálatban (ONTARGET).
Ajánlás 51
Bár gondos követés szükséges,ß-blokkoló (elsősorban vasodilatátor) nem kontraindikált hypertoniás PAD-betegeknek, mivel úgy tűnik, az alkalmazásuk nincs összefüggésben a PAD tüneteinek progressziójával. (Evidencia szint: B) (IIa osztályú ajánlás)
A béta-blokkoló kezelés nem ellenjavallt perifériás verőérbetegekben, miután a béta-blokkoló terápia nem befolyásolja a betegek funkcionális kapacitását, vagy tüneteit, sőt csökkenti a posztinfarktusos perifériás verőérbetegekben az új coronariaesemények arányát. Emellett műtétre kerülő betegekben a műtétet megelőzően beállított béta-blokkoló kezelés csökkenti a műtéti kockázatot.
Ajánlás 52
Kritikus végtagischaemia (Fontaine III. és IV. stádiumú verőérszűkület: nyugalmi fájdalom, illetve ulcus/gangraena) esetén a végtagvesztés veszélye miatt a célvérnyomás értéket úgy kell megszabni, hogy a boka magasságában mérhető systolés nyomás érték lehetőleg ne csökkenjen 50 Hgmm alá. (Evidencia szint: B) (IIb osztályú ajánlás)
Ajánlás 53
Tünetmentes PAD betegek esetében az ACE gátló kezelés megfontolható a kardiovaszkuláris rizikó csökkentése érdekében. (Evidencia szint: C) (IIb osztályú ajánlás)
8.3. Diabetes mellitus kezelése
Ajánlás 54
Minden diabeteses betegben fontos a megfelelő lábápolás (megfelelő lábbeli viselése, podiátriai ellenőrzés, napi láb ellenőrzés, bőrhidratáló krémek helyi alkalmazása) és a bőr léziókat, ulcerációkat sürgősen kell kezelni. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 55
Diabeteses PAD betegekben a megfelelő glukóz kontroll (HbA1c 6-8%) hatékony lehet a mikrovaszkuláris komplikációk csökkentésében és potenciálisan javíthatja a kardiovaszkuláris prognózist. (Evidencia szint: C) (IIa osztályú ajánlás)
A végtagvesztés kockázatának csökkentése érdekében fontos a megfelelő lábápolás és a bőrléziók korai felismerése céljából a végtagok rendszeres, naponkénti ellenőrzése. A perifériás verőérbetegség klasszikus rizikófaktora a diabetes mellitus, és úgy tűnik a diabetes fennállási ideje és súlyossága összefüggést mutat a cukorbetegség okozta kockázat mértékével.
Ugyanakkor nincs egyértelmű bizonyíték arra nézve, hogy a diabetes agresszív kezelése javítaná a perifériás verőérbetegekben a kardiovaszkuláris kimenetelt és a makrovaszkuláris események arányát. Egy retrospektív analízis alapján 1-es típusú diabeteses betegekben az intenzív inzulin kezelésben részesülőknél a vaszkuláris események (claudicatio, revaszkularizáció és amputáció) statisztikailag nem szignifikáns csökkenése volt meg - figyelhető. A United Kingdom Prospective Diabetes Studyban (UKPDS) pedig 2-es típusú diabetesben az agresszív antidiabetikus kezelésben részesülőknél 10 éves kezelés mellett bár a myocardialis infarctus kockázata 16%-kal csökkent, de sem a halálozás, sem a stroke, sem az amputáció aránya nem változott jelentősen. A mikrovaszkuláris események (nephropathia és retinopathia) kockázatát ugyanakkor az intenzív antidiabetikus kezelés csökkenti.
Mindezek alapján a HbA1c 6-8%, mint célérték perifériás verőérbetegek esetében is széles körben elfogadott.
8.4. A dohányzás beszüntetése
Ajánlás 56
Dohányzó vagy korábban dohányzó betegek esetében minden vizit alkalmával rá kell kérdezni a dohányzási statusra. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 57
A beteg leszokását tanáccsal és leszokási tervvel kell segíteni, mely magában foglalhatja a gyógyszeres kezelést és/vagy a leszokási programra való irányítást. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 58
A dohányzó PAD beteggel foglalkozó minden klinikusnak tanácsolnia kell a dohányzás abbahagyását. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 59
Amennyiben kontraindikáció nem áll fenn, a következő gyógyszeres kezelések egyikét fel kell ajánlani a betegnek: varenicline, bupropion vagy nikotinpótló készítmények. (Evidencia szint: A) (I osztályú ajánlás)
A dohányzás a perifériás verőérbetegség klasszikus rizikótényezője, amely nemcsak a PAD kialakulásának kockázatát növeli 2-6-szorosára, de a szövődmények (amputáció, posztopratív szövődmények, mortalitás) rizikóját is fokozza.
Minden dohányzó verőérbeteg számára javasolt dohányzás leszoktatási programban való részvétel, illetve a dohányzás elhagyását segítő gyógyszerek, így a nikotinpótló készítmények, bupropion, illetve varenicline használata, amelyek biztonságosan alkalmazhatóak kardiovaszkuláris betegségben szenvedőkben. Bupropionnal, illetve nikotin pótló készítménnyel a dohányzás leszokási sikerráta 16-30%-os. A varenicline, amely a nikotin receptor parciális agonistája a leghatékonyabb a dohányzásról való leszoktatás elérésében.
A dohányzásról való leszokás különösen kritikus thrombangiitis obliteransban szenvedő betegek esetében, mert ebben a szindrómában feltételezik, hogy a dohány valamilyen alkotója felelős lehet a sokszor végtag - vesztéshez vezető betegség kialakulásáért.
8.5. Thrombocyta aggregáció gátló kezelés
Ajánlás 60
Szimptómás PAD betegekben (CI, KVI, megelőző revaszkularizáció vagy amputáció) thrombocyta aggregáció gátló (TAG) kezelés indikált a MI, stroke és vaszkuláris halál rizikójának csökkentésére. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 61
Szimptómás PAD betegekben (CI, KVI, megelőző revaszkularizáció vagy amputáció) biztonságos és hatékony TAG kezelésként aspirin adása ajánlott, általában 75-325 mg-os napi dózisban, a MI, stroke és vaszkuláris halál rizikójának csökkentésére. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 62
Szimptómás PAD betegekben (CI, KVI, megelőző revaszkularizáció vagy amputáció) TAG kezelésként ajánlott a clopidogrel (napi 75 mg), mint az aspirin kezelés biztonságos és hatékony alternatívája, a MI, stroke és vaszkuláris halál rizikójának csökkentésére. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 63
A TAG kezelés hasznos lehet a MI, stroke és vaszkuláris halál rizikójának csökkentésére azokban a tünetmentes PAD betegekben, akiknél a BKI kisebb vagy egyenlő 0,90. (Evidencia szint: C) (IIa osztályú ajánlás)
Ajánlás 64
A TAG kezelés haszna a MI, stroke és vaszkuláris halál rizikójának csökkentésére azokban a tünetmentes PAD betegekben, akiknél a BKI határértéken van (0,91-0,99) nem kellően bizonyított. (Evidencia szint: A) (IIb osztályú ajánlás)
Ajánlás 65
Aspirin és clopidogrel kombinációja megfontolható a kardiovaszkuláris események rizikójának csökkentésére azokban a szimptómás PAD betegekben (CI, KVI, megelőző revaszkularizáció vagy amputáció), akiknél fokozott vérzés rizikó nem áll fenn és igen nagy a kardiovaszkuláris kockázat. (Evidencia szint: B) (IIb osztályú ajánlás)
Szimptómás PAD betegekben egy 42 randomizált vizsgálatot (összesen 9706 beteg adatait) feldolgozó metaanalízis (Antithrombotic Trialists’ Collaboration) alapján a vérlemezkegátló kezelés a vaszkuláris halálozás, nem-halálos myocardialis infarctus, és a nem-halálos stroke incidenciáját a placebo kezeléshez képest 23%-kal csökkenti. A kisdózisú (75-150 mg/nap) aspirin hatékonysága nem marad el a nagyobb dózisokétól. Tünetmentes, kiskockázatú PAD betegekben a vérlemez - kegátló (aspirin) kezelés hatékonysága nem egyértelmű, bár ezekben a vizsgálatokban nem a standard klinikai gyakorlatnak megfelelően történt a boka-kar index meghatározás és így a perifériás verőérbetegség diagnózisának felállítása.
A Clopidogrel versus Aspirin in Patients at Risk for Ischaemic Events (CAPRIE) vizsgálatban 6452 perifériás verőérbetegségben szenvedő beteg vett részt. A közel 2 éves utánkövetés alatt a perifériás verőérbetegek között a clopidogrellel kezeltekben a klinikai végpontok (vasz - kuláris halálozás, nem-halálos myocardiális infarctus és nem-halálos stroke) előfordulási gyakorisága kisebb volt, mint az aspirinnel kezeltekben (3,7% versus 4,9%). Ez a különbség nagyobb volt PAD betegekben, mint a coronariabetegekben és a stroke-on átesett betegekben.
A CHARISMA (Clopidogrel for High Atherothrombotic Risk and Ischemic Stabilization, Management, and Avoidance) vizsgálat alapján bizonyos nagykockázatú betegekben a kettős vérlemezkegátló kezelés – amennyiben nincs fokozott vérzésveszély – meggondolandó, bár az európai ajánlás ezt a fokozott vérzésveszély miatt nem támogatja.
Perifériás verőérbetegekben az új vérlemezkegátló kezeléssel (prasugrel, ticagrelor, vorapaxar) kapcsolatban evidencia egyelőre nem áll rendelkezésre.
9. Claudicatio intermittens kezelése [1, 3, 88-114]
9.1. Ellenőrzött tréning és PAD rehabilitáció
Ajánlás 66
CI-ben szenvedő betegnek, amennyiben nincs súlyos ischaemiás tünete, első kezelésként az ellenőrzött tréning ajánlott. (Evidencia szint: A) (I osztályú ajánlás)
A PAD betegek kezelésének központi szereplője lett a rendszeres ellenőrzött fizikai tréning, melynek következtében csökkennek a claudicatio-s panaszok, javul a járás sebessége, növekszik a panasz nélkül megtehető távolság. Mivel a PAD betegek között nagy arányban vannak koronária betegek, hypertoniások, kardiálisan dekompenzáltak, ezért a tréning megkezdése előtt a szisztémás keringés ellenőrzése, 12 elvezetéses EKG, vérnyomásmérés feltétlenül szükséges. A kórrajz teljes felvétele, teljes körű fizikális vizsgálat, a PAD súlyosságának megállapítása, a lábak funkcionális kapacitásának megítélése részét kell képeznie a program előkészítésének. A beteg számára elfogadható terápiás tervet kell készíteni.
Ajánlás 67
Az ellenőrzött tréning gyakorlatot 30 - 45 perces időtartamban ajánlott végezni, legalább heti 3 alkalommal, legalább 6 hónapon keresztül. (Evidencia szint: A) (I osztályú ajánlás)
Sok tanulmány született az irányított tréning kialakítása tárgykörében. Gardner és Poehlman, akik maguk is elkötelezettjei a fizikai tréning gyakorlati alkalmazásának, 21 tanulmány metaanalízisét elvégezve azt találták, hogy a fájdalom nélküli járástávolság 180%-kal, a maximális járástávolság 120%-kal növekedett. Kiemelték, hogy a legnagyobb eredmény a járás képességben akkor történt, ha legalább heti 3 alkalommal, egy-egy alkalommal több, mint 30 percig tartó, a maximális fájdalmat megközelítő tréninget legalább 6 hónapon át végezték. A programidő és eredményesség kapcsolatát áttekintve megállapítható, hogy a tréning idő első 4 hónapban növekszik mind a fájdalom nélküli, mind a maximális járástávolság, azt egy kb. 2 hónapig tartó plátó követi. Mindezek alapján a 3-6 hónapon át tartó tréning idő mondható optimálisnak.
A tréning módját illetően a vizsgálatok eredményei azt mutatják, hogy a rezisztencia gyakorlatok direkt módon nem javítják a járásképességet, tehát a dinamikus mozgást alkalmazó tréning választandó. A láb amputáltak számára alternativ tréning lehetőség a kar ergometria, mely javítja a cardiovascularis erőnlétet, erősíti a kar és a mellkas izmait.
Ajánlás 68
Nem ellenőrzött tréning terápia indikált, ha a felügyelt tréning nem kivitelezhető vagy nem elérhető. (Evidencia szint: C) (I osztályú ajánlás)
Számos vizsgáló összevetette a szakember irányította, intézeti rendszeres fizikai tréninget az otthoni, csupán előírás alapján végzett tréning hatásosságával. Minden vizsgálat a kontrollált tréning előnyét bizonyította. Hazánkban a valóság szabta lehetőségek egyelőre többnyire csupán a kevésbé hatásos otthoni, előírással irányított fizikai tréningre van mód. Minden erővel arra kell törekedni, hogy országszerte kialakítsuk mind a személyi-, mind az infrastrukturális feltételeket, hogy az eddigitől lényegesen nagyobb életminőség és életesély javulást biztosíthassunk a PAD betegeknek.
9.2. Gyógyszeres kezelés
Ajánlás 69
Cilostazol ajánlott a claudicatiós tünetek enyhítésére és a járástávolság növelésére CI esetén, amennyiben kontraindikáció (szívelégtelenség) nem áll fenn. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 70
A cilostazol kezelést fel kell ajánlani minden betegnek, az életvitelt akadályozó mértékű claudicatio esetén, amennyiben kontraindikáció nem áll fenn. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 71
Naftdirofuryl kezelés megfontolható a claudicatiós tünetek enyhítésére és a járástávolság növelésére az életvitelt akadályozó mértékű CI esetén. (Evidencia szint: B) (IIa osztályú ajánlás)
Ajánlás 72
Pentoxifyllin kezelés megfontolható a claudicatiós tünetek enyhítésére és a járástávolság növelésére CI esetén. (Evidencia szint: B) (IIb osztályú ajánlás)
A tünetek enyhítése, a járástávolság növelése érdekében claudicatio intermittens esetén alkalmazott konzervatív kezelés két formája a mozgásterápia és a gyógyszeres kezelés.
A gyógyszeres terápiával kapcsolatos evidenciák általában korlátozott értékűek, az alkalmazott szerek pontos hatásmechanizmusa sokszor nem egyértelmű.
A cilostazol egy foszfodieszteráz-3 gátló szer, vazodilatátor és vérlemezkegátló hatású, amely placebohoz képest növeli a járástávolságot (+40-60%, 12-24 hetes utánkövetés során). Hatása dózisfüggő, 2x100 mg adagban hatásosabb, mint 2x50 mg adagban. Szívelégtelenségben és < 25/ml kreatinin-clearence esetén nem adható.
A naftidrofuryl egy 5-hydroxytryptamin-2 antagonista, amely gátolja a vörösvértestek és vérelemezkék aggregációját. Metaanalízis alapján 26%-kal növeli a fájdalommentes járástávolságot palcebohoz képest.
A pentoxifylline methyxanthine származék, amely egyes tanulmányok szerint javítja a vörövértest és fehérvérsejt rugalmasságát, csökkenti a vér és a plazma viszkozitását, gátolja fehérvérsejtek adhézióját és aktivációját és így fejti ki rheologiai hatását, bár más tanulmányok ezen hatásokat igazolni nem tudták. Javítja a járástávolságot (+20-30%- kal). Nem befolyásolja a boka-kar indexet.
9.3. Endovasculáris kezelés
Az endovasculáris ér-rekonstrukciós technikák elmúlt évtizedben bekövetkezett dinamikus fejlődése nagyszámú alsó végtagi érszűkületben szenvedő beteg számára nyitotta meg a minimal invasív kezelés lehetőségét. Világviszonylatban egyre több központ működik az elsődleges endovasculáris kezelés elve szerint, csökkentve ezzel morbiditását és mortalitását, s csupán az intervencióra alkalmatlan esetekre tartja fenn a sebészi reconstructió lehetőségét. Az optimalis kezelési startégiák megválasztására vonatkozóan, endovascularis vs. sebészi kezelés kérdéskörében adekvát randomizált klinikai vizsgálat nehezen kivitelezhető a katéteres technikák gyors fejlődése, változása miatt. A vascularis központokban szoros kooperációban tevékenykedő érsebész és interventios szakember minden esetben egyénre szabottan választja meg a legmegfelelőbb terápiát, melynek fő szempontjai a laesio anatomia sajátságain és a beteg társbetegségein túl, a helyi tárgyi és személyi feltételek; valamint végül, de nem utolsó sorban a beteg preferenciája kell, hogy legyen. Az endovasculáris technikák fejlődése sok belgyógyászt a percután intervenciók liberálisabb indikációjára sarkallja. Azonban míg kritikus végtag - ischemiában (KVI) a revascularizáció lehetőség szerint kötelező, addig enyhe vagy közepes klaudikáció esetén a gyógyszeres és fizikoterápiás kezeléssel szemben az endovasculáris rekonstrukció hosszú távú haszna nem meggyőző. Amennyiben a claudicatio a mindennapi életvitelt korlátozza, az endovasculáris beavatkozás is csak azon esetekben indikált, ha várhatóan számottevő javulást eredményez majd, és a beteg előzetes konservatív kezelése megfelelő eredményt nem hozott. Kivételt képez ez alól az aorto-iliacalis lokalizáció, melynek esetében az endovasculáris intervenció hosszas előzetes konzervatív kezelés nélkül is megfontolható. Az endovasculáris megoldások hátránya a sebészi megoldással szemben a rosszabb hosszú távú nyitvamaradás. Az elsődleges nyitvamaradás legjobb az a. iliaca communison végzett intervenciókat követően, és egyértelműen rosszabb, ha az elváltozás disztalisabb, hosszabb szakaszú, többszörös, illetve diffúz; valamint gyenge kifolyótraktus, cukorbetegség és veseelégtelenség esetén is. Jelenleg a stent beültetésen kívül nincs más igazoltan hatásos módszer, amivel az angioplasztikák legalább középtávú átjárhatóságát javíthatnánk. A gyógyszerkibocsátó ballonok alkalmazása ígéretesnek látszik, de egyelőre a rendelkezésre álló adatok nem elegendőek általános ajánlás megfogalmazásához. Általában panaszmentes betegnél, profilaktikus céllal endovasculáris beavatkozás végzése nem indokolt.
Stent beültetésének elsődleges céljai: a) az angioplasztika elégtelen eredményének (residuális szűkület, vagy jelentős visszaszűkülés, disszekció) korrekciója, b) a hosszútávú nyitvamaradás javítása. Általánosságban mellőzni kell stent beültetését hajlítási zónákba (csípő, térd) - bár újabban erre speciális eszközöket fejlesztettek ki - és ugyancsak kerülendő alkalmazásuk egy esetleges bypass anastomosisának helyén is.
9.3.1. Ajánlások az aorto-iliacalis szakaszra vonatkozóan
Ajánlás 73
Amennyiben revascularizáció szükséges, elsődleges endovasculáris kezelés ajánlott valamennyi aortoiliacalis lokalizációjú TASC A-C típusú elváltozás esetén (ld. I. táblázat). (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 74
Elsődleges endovasculáris kezelés megfontolható aorto-iliacalis TASC D elváltozások esetén is, ha súlyos társbetegségek állnak fenn, illetve a beavatkozást nagy gyakorlattal bíró intervenciós szakember végzi el. (Evidencia szint: C) (IIb osztályú ajánlás)
Ajánlás 75
Aorto-iliacalis elvátozások esetén inkább megfontolható a prímer stent beültetés szemben a provizórikus stenteléssel. (Evidencia szint: C) (IIb osztályú ajánlás)
Az endovasculáris technikák alkalmazásának preferált helye az obstruktív arteriosclerosis aorto-iliacalis lokalizációja. Valamennyi TASC A-C lézió esetén az elsődleges endovasculáris kezelés létjogosultságát igazolja az alacsony morbiditás és mortalitás mellett a >90% feletti technikai sikerességi ráta is. Tapasztalt központokban TASC D elváltozások primer percután kezelése is megkísérelhető. A primer és az angioplasztikát követően is fennmaradó nyomás grádiens esetén végzett provizórikus stentelés összehasonlító randomizált vizsgálata nem igazolta primer stentelés bármiféle előnyét sem. Régebbi, meta-analízisen alapuló vizsgálat szerint az a. iliaca comm. (AIC) és az a. iliaca externa (AIE) elsődleges stentelése ajánlható, nyitvamaradásuk kedvező, összehasonlítva a sebészi revaszkularizációval.
A ballonos és öntáguló stentek alkalmazása főleg a beavatkozást végző személy egyéni preferenciái szerint történik. A ballonos stentek legfontosabb előnyei a magasabb radialis stiffness és a pontosabb pozícionál - hatóság, melyek különösen fontosak bifurkációhoz közeli elváltozások esetén. Az AIE vonatkozásában a disszekció és elasztikus visszaszűkülés alacsonyabb rizikója miatt a primer öntáguló stent implantációja a preferált a provizó - rikus stenteléssel szemben.
Az elváltozások beosztása a TransAtlantic Inter- Society Consensus for the Management of Peripheral Arterrial Disease (TASCII) szerint:
Aorto-iliacalis szakasz:
A típus
- Az a.iliaca com.(AIC) egy vagy kétoldali szűkülete
- Az a.iliaca ext. (AIE) egy vagy kétoldali rövid szakaszú (< 3cm), egyszeres szűkülete
B típus
- Az infrarenalis aorta rövid szakaszú (< 3 cm) szűkülete
- Egyoldali AIC elzáródás
- Az AIE egyszeres vagy többszörös szűkülete (3-10 cm), mely nem terjed az a.femoralis com.-ra (AFC)
- Az AIE egyoldali elzáródása, mely nem érinti az a. iliaca int. (AII) szájadékát, illetve az AFC-t
C típus
- Kétoldali AIC elzáródás
- Kétoldali 3-10cm között hosszúságú AIE szűkület, mely nem érinti az AFC-t.
- Egyoldali AIE szükület, mely érinti az AFC-t is
- Egyoldali AIE elzáródás, mely érinti az AII és/vagy AFC eredését
- Egyoldali AIE elzáródást okozó, erősen meszes plaque, az AII és/vagy AFC eredések érintettségétől függetlenül
D típus
- Infrarenalis aorto-iliacalis elzáródás
- Az aorta és mindkét iliaca artériák kezelést igénylő diffúz arteriosclerotikus érintettsége
- Egyoldali AIC, AIE és AFC diffúz, többszörös szűkülete
- Egyoldali AIC és AIE elzáródás
- Az AIE kétoldali elzáródása
- Hasi aorta aneurysmás, iliaca szűkületes betegek, akik endograft beültetésére nem alkalmasak, illetve más okból nyitott aorta vagy iliaca rekonstrukció szükséges
9.3.2. Ajánlások a femoro-poplitealis szakaszra vonatkozóan
Ajánlás 76
Amennyiben revascularizáció szükséges, elsődleges endovasculáris kezelés ajánlott valamennyi femoropoplitealis lokalizációjú TASC A-C típusú elváltozás esetén (ld. II. táblázat). (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 77
Primer stent beültetés megfontolandó femoropoplitealis TASC B típusú elváltozások esetén. (Evidencia szint: A) (IIa osztályú ajánlás)
Ajánlás 78
Elsődleges endovasculráris kezelés ugyancsak megfontolható femoro-poplitealis TASC D elváltozások esetén is, ha súlyos társbetegségek állnak fenn, illetve a beavatkozást nagy gyakorlattal bíró intervenciós szakember végzi el. (Evidencia szint: C) (IIb osztályú ajánlás)
A femoro-poplitealis szegmens endovasculáris kezelés egyik fő problémáját a diffúz érintettség gyakorisága jelenti. A femoralis artériát a végtag mozgásai közben különböző erőhatások ismétlődően deformálják. Manapság - hála a technológia fejlődésének és az egyre gyakorlottabb interventios szakembereknek - magas technikai sikerességgel és alacsony kockázattal végezhetővé váltak a femoropoplitealis traktus hosszú szakaszú és komplex megbetegedéseinek endovasculáris reconstrukciói is. A korábbi gyakorlatot, mely szerint stent beültetése csak az angioplasztika (PTA) sikertelenségekor, vagy késői restenosis kapcsán jött szóba; jelentősen megváltoztatta az öntáguló nitinol stentek megjelenése. Középhosszú a. femoralis spf. (AFS) elváltozások esetén, növekvő számú, randomizált klinikai vizsgálat eredménye szerint a javuló középtávú nyitvamaradásnak köszönhetően, primer nitinol stent beültetése ajánlható, mint elsődleges kezelés. 1-2 év távlatában a primer stentelést követő restenosisok aránya 20-30%-kal alacsonyabb, mint az angiplasztikánál (PTA). Ha a klinikum alapján a revascularisatio szükséges a laesio hossza és komplexitása alapján AFS stentelése mellett dönthetünk. Kritikus végtagischemiában (KVI) végtagmentés, vagy artériás fekély esetén a stentelés indkációja liberálisabb lehet. Korábban számos olyan tényezőt tartottak számon melynek szerepe lehet a stent törésekben: ilyenek a beültetett stentek száma és hossza, az egymást átfedő stentek, az érfal meszesedésének foka, és a beültetés módja is. Az utóbbi időszakban a legújabb generációs stentek, azonban már jóval kevésbé hajlamosak a törésekre és a hosszú nitinol stentek (akár 20 cm) megjelenése megnyitotta az utat a jóval komplexebb, nehezebb esetek endovasculáris kezelése előtt is.
A stent technika legfőbb hátránya az instent restenosis kialakulásának esélye. Mind a mai napig a stentek tervezésével nem sikerült érdemben befolyásolni a restenosisok kialakulásának arányát. Izolált balon angioplasztika sikertelensége nagyon magas a restenosisok korrekciója esetében. Több egyéb kezelési lehetőség vizsgálata is folyamatban van, azonban nincs olyan study, mely valamelyik technika egyértelmű elsődlegességét igazolná. Számos klinikai vizsgálat foglalkozott a femoralis superficialisba beültetett gyógyszer kibocsátó (drug eluting) stentekkel, de ezidáig nem sikerült előnyüket bizonyítani a bare metal nitinol stentekkel szemben. Gyógyszerkibocsátó balon femoro-popitealis szakaszon történő alkalmazásával kapcsolatos korai vizsgálati eredmények jobb rövid távú nyitvamaradást látszanak igazolni az egyszerű balon angioplasztikával szemben.
Komplex AFS laesiok kezelésére jó lehetőségnek látszik covered stentek (stent graftok) alkalmazása, melynek eredményei összemérhetőek a térd feletti bypass műtétekéivel is.
A subintimalis angioplasztika széleskörű alkalmazása ellenére kevés kutatásai adat áll rendelkezésre erre vonatkozóan. Nincs összehasonlító adat az intraluminalis és subintimalis rekanalizáció nyitvamaradására vonatkozóan sem. Azonban interventiok kapcsán sokszor az akaratlan subintimalis passage elkerülhetetlen. Az atherectomiát illetően különböző eszközöket használnak, bizontalan hosszútávú eredményekkel. Jelenlegi indikációjukat súlyosan meszes elváltozások és stentelésre alkalmatlan érszakaszok (a.femoralis comm. és az a. poplitea) jelentik, azonban a technika hátránya lehet a disztalis embolizáció rizikója.
Az elváltozások beosztása a Trans Atlantic Inter- Society Consensus for the Management of Peripheral Arterial Disease (TASCII) szerint [2]
Femoro-poplitealis szakasz
A típus
- Egyszeres szűkület mely <10 cm hosszúságú
- Egyszeres elzáródás mely <5 cm hosszúságú
B típus
- Többszörös elváltozás (szűkület vagy elzáródás), valamennyi <5 cm hosszúságú
- Egyszeres <cm hosszú szűkület vagy elzáródás, mely nem érinti az a. poplitea térd alatti szakaszát
- Egyszeres vagy többszörös elváltozások, disztalis bypassok beáramlásának javítására, a tibialis erek folytonosságának hiányában
- Erősen meszes, <5 cm hosszúságú elzáródás
- Egyszeres poplitealis szűkület
C típus
- Többszörös szűkület vagy elzáródás, kifejezett meszesedéssel vagy anélkül, melynek teljes hossza >15 cm
- Legalább két endovasculáris interventiot követően kialakuló kezelést igénylő restenosis
D típus
- Az AFC krónikus elzáródása, vagy a AFS a. popliteát is érintő >20 cm hosszú elzáródása
9.3.3. Ajánlások az infrapoplitealis szakaszra vonatkozóan
Ajánlás 79
Amennyiben az infrapoplitealis szakaszon revascularizáció szükséges, megfontolandó az elsődleges endo - vasculáris kezelés. (Evidencia szint: C) (IIa osztályú ajánlás)
Ajánlás 80
Infrapoplitealis lokalizációjú elváltozások esetében preferált technika az angioplasztika (PTA), és stent beültetését csak sikertelen PTA esetén kell megfontolni. (Evidencia szint: C) (IIa osztályú ajánlás)
A kritikus végtagischemiában szenvedő betegek többségénél az érszűkület multiszegmentális lokalizációja az infrapoplitealis szakaszt is érinti. Ezért az infrapoplitealis szegment endovascularis kezelésének elsődleges indikációja a végtagmentés, míg klaudikáció esetén általában nem jön szóba az angioplasztika. Egyre inkább erősödő evidencia támogatja az angioplasztika ajánlását KVI esetén, ha súlyos társbetegségek állnak fenn és a diagnosztikus angiographia alapján legalább egy, a lábbfejig egyenes lefutású, reconstruálható artéria ábrázolódik.
Standard ellátásnak számít a primer PTA, mely olcsó és klinikai eredményei elfogadhatóak. A primeren sikeres térd alatti intervenciók végtagmentési aránya minden bizonnyal nagyobb, mint nyitva maradásuk aránya. Éppen ezért a kritikus végtagischemiás betegek tartós klinikai javulásának nem feltétele az interventiók késői átjárhatósága. Infrapoplitealis stentelés általánosságban csak szuboptimális eredményű PTA után jön szóba. Gyógyszerkibocsátó stentek alkalmazásával kedvezőbb restenosis ráta érhető el, ezért ezzel az indikációval Európában elfogadott a sirolimus kibocsátó balon-aplikált stentek használata.
9.4. Sebészi kezelés
Az alsó végtagi ischemia kezelésére az érsebészet különböző revascularizációs technikákkal rendelkezik. Napjainkban hosszú szakaszú elzáródás esetén leggyakrabban a bypasst alkalmazzuk, mely a graft positiója szerint lehet anatomiás vagy extraanatomiás. Bizonyos körülmények esetén a vérkeringés helyreállítására lokalis endarteriectomia végezhető foltplasztikával vagy anélkül. Különböző típusú graftok ismertek. Az autológ vénás vagy artériás graft a legjobb lehetőség, melyek azonban nem mindig állnak rendelkezésre, ezért korlátozottan alkalmazhatóak. Leggyakrabban műér graftok kerülnek beültetésre. A harmadik lehetőséget a homograftok jelentik, melyek alkalmazását különösen infectív szövődmények ellátására tartjuk fenn. Járásképtelen betegeknél, kiterjedt szövetelhalással vagy súlyos fertőzéssel járó üszkösödés esetén legjobb megoldás az amputáció. Az amputáció a legutolsó sebészi lehetőség az irreversibilis végtagischemia megoldására, mely lehetőséget adhat a beteg felépülésére és protézissel történő rehabilitációjára. Moribund beteg esetén a megfelelő fájdalomcsillapítás a supportív therápia választása a legjobb megoldás. Estenként kiegészítő sebészi terápiák is megfontolhatóak, mint például kiterjedt szövethiányok bőrrel történő fedése. A lumbalis sympathectomia alkalmazása ellentmondásos, hatékonysága nem bizonyított.
9.4.1. Ajánlások az aorto-iliacalis szakaszra vonatkozóan
Ajánlás 81
Endovasculáris kezelésre alkalmatlan, gyógyszeres és fizikoterápiás kezelésre nem megfelelően reagáló, haemodynamikailag szignifikáns aorto-iliacalis arteriosclerosis esetén bypass műtét végezthető, ha a beteg mindennapi életvitele vagy hivatásszerű aktivitása korlátozott. (Evidencia szint: B) (I osztályú ajánlás)
Ajánlás 82
Axillo-femoralis bypass csak rendkívül szűk indikációs körben végezhető, ha a krónikus infrarenalis aorta elzáródás súlyos, rövid szakaszú klaudikációt okoz és a beteg aorto-bifemoralis bypass műtétre alkalmatlan. (Evidencia szint: B) (IIb osztályú ajánlás)
Kiterjed aoorto-iliacalis megbetegedésben általában aorto-biiliacalis vagy aorto-bifemoralis bypass végzése javasolt. Ha laparotomia végzése kockázatos, módosított retroperitoenalis feltárás és esetleg aorto-unilateralis bypass, valamint femoro-femoralis cross-over bypass végzése jön szóba. További extra-anatomiás lehetőséget jelenthet az axillo-(bi) femoralis vagy throraco- (bi)femoralis bypass készítése. Az aorto-bifemoralis bypassal összehasonlítva az extra-anatomiás reconstructiók rosszabb hosszútávú átjárhatóságot és magasabb szövődmény incidenciát jelentenek. Az aorto-(bi) femoralis bypass 10 éves nyitvamaradása 80-90% közé tehető.
9.4.2. Ajánlások a femoro-disztalis szakaszra vonatkozóan
Ajánlás 83
Amennyiben infrainguinalis elváltozások miatt a sebészi kezelés jön szóba, bypass esetén az autológ saphena a választandó. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 84
Mivel a szintetikus graftok nyitvamaradásának aránya alacsony, térd feletti bypassokhoz történő alkalmazásuk nem kellően megalapozott. (Evidencia szint: B) (IIb osztályú ajánlás)
Ajánlás 85
Autolog vénás femoro-tibialis bypass klaudikáció kezelésére csupán bizonyos betegeknél, ritkán jöhet szóba. (Evidencia szint: B) (IIb osztályú ajánlás)
Ajánlás 86
Klaudikáció kezeléseként femoro-tibialis bypass készítéséhez szintetikus graft nem alkalmazható. (Evidencia szint: C) (III osztályú ajánlás)
Ha a claudicatiot infrainguinalis érszűkület okozza, a beavatkozás indikációjának kérdése vitatottabb, mint az aorto-iliacalis lokalizáció kapcsán. Függ a tünetektől az a. femoris profunda és az ebből eredő kollateralis keringés minőségétől, valamint a lokális haemodynamikai statustól is. Ezzel szemben kritikus végtag ischaemia esetén a beteg bármely proximalis artériája - az iliaca, femoralis comm., spf. és a profunda, valamint a poplitea - szolgálhat beáramlásként egy disztalis bypasshoz. Az autológ vénás graft (in situ, reverz, vagy ellenoldalról eltávolított) biztosítja a legjobb nyitvamaradást. Műér graftok használata akkor javasolt, ha autológ nem áll rendelkezésre. Ellentmondóak az eredmények arra vonatkozóan, hogy a vénás cuff javítja-e a bypass átjárhatóságát. Dacron és a PTFE femoropoplitealis graftok hét egyidejű klinikai vizsgálatának legújabb meta-analysise megállapította, hogy 3 és 5 év után a kumulatív elsődleges nyitvamaradásuk hasonló (60.2% vs. 53.8%; valamint 49.2% vs. 38.4%). Három, kizárólag térd feletti femoro-poplitealis bypassokkal foglalkozó study eredményeinek összesítése alapján a Dacron graftok primer elzáródásának aránya alacsonyabb a PTFE graftokénál. A femoro-distalis (tibialis és pedalis) bypassok vonatkozásában az összesített, súlyozott adatok szerint az 1-,3- és 5- éves átjárhatóság 85, 80 és 70% vénás graftok, míg 70, 35 és 25% műér gtaftok beültetését követően. Térd feletti bypassok 4 éves elsődleges és másodlagos nyitva maradása a vénás graftoknál 73 és 90%-os, PTFE műereknél 47és 47%, míg Dacron protézisek esetében 54 és 60%. Két vizsgálat hasonlította össze az "in situ" és a "reverz" térd fölé, illetve alá vezetett saphena graftokat és nem talált különbséget sem a primer vagy secunder átjárhatóságot, sem pedig a végtagmentés arányát illetően sem. Három vizsgálat hasonlította össze a PTFE és a humán umbilicalis véna graftokat, igazolva az utóbi szignifikánsan magasabb másodlagos nyitvamaradását. Nincs különbség az átjárhatóságban a vénás folttal, vagy a nélkül alkalmazott térd fölötti PTFE graftoknál, viszont a térd alá vezetett bypassok esetében vénás a cuff-val jobb 2 éves primer nyitvamaradást igazoltak.
Csupán egy randomizált klinikai vizsgálat hasonlítja össze az infrainguianlis endovasculáris és bypass műtétek eredményeit. A BASIL vizsgálatban (Bypass vs. Angioplasty in Severe Ischemia of the Leg) 452 infrainguinalis érszükület következtében kialakult, súlyos végtag ischemiában szenvedő beteget randomizáltak percután angioplasztikára illetve bypass műtétre. Az elsődleges végpont az amputáció mentes túlélés volt. Másodlagos végpontként vizsgálták a mortalitást, morbiditást, a reintervenciók arányát, az életminőséget és a kórházi kezelési költségeket. A 30 napos halálozás hasonló volt mindkét csoportban (5% a bypass és 3% az angioplasztika esetében). Mindamellett a sebészi kezelés magasabb morbiditással járt (57% vs. 41%), döntően myocardialis infarctusoknak és sebfertőzéseknek köszönhetően. A sebészi kezelés az első évben költségesebbnek is bizonyult a hosszabb kórházi ápolás miatt. A 6 hónapos végtagmentési ráta azonos volt mindkét kezelés vonat - kozásában. Az első évben az angioplasztikák esetében a reocclusio aránya jóval magasabb (20% vs. 3%), szükségessé téve nagyobb számú reintervenciót (27% vs. 17%) is. Ezen eredmények a sebészi revascularizatio elsődlegességét támasztják alá amennyiben a beteg a bypasshoz megfelelő vénával rendelkezik. Az újabb, hosszabb után követésről szóló adatok (>3 év) szerint nincs szignifikáns különbség túlélést és az amputáció mentes túlélést illetően a két kezelés között. Bár a randomizációt követően legalább két évet megélő betegek számára az elsődleges sebészi revascularizáció szignifikánsan javította a későbbi túlélést és a végtagvesztés mentes túlélést is.
Egy kisebb randomizált study a térd feletti bypassokat hasonlította össze a stenteléssel és 12 hónapot követően nem talált különbséget a primer és secunder átjárhatóságban. További vizsgálatok szükségesek az infrainguinalis bypassok és a stent implantációk összehasonlítására.
Az infrainguinalis sebészi rekonstrukciók egy másik formája az a. femoris profunda eredésénél lévő szűkület korrekciója, a profunda plasztika. Szóba jöhet disztalis bypass műtét helyett, ha a beáramlás kellően jó, a szűkület a profunda proximalis harmadán van és megfelelő a kollateralizáció a cruralis erek felé.
Másodlagos amputáció akkor válhat szükségessé, ha a reconstructio elzáródott és nincs további reinterventiós lehetőség, vagy ha nyitott graft ellenére végtag állapota rosszabbodik a kiterjedt a szövetelhalás vagy infectió miatt. A másodlagos amputáció célja a fájdalom csökkentése, az elhalt, illetve fertőzött szövetek eltávolítása révén a detoxikálás, valamint egy protetizálásra alkalmas csonk kialakítása révén a beteg rehabilitációja és járóképességének helyreállítása.
Bármilyen reconstructiós beavatkozást követően a beteg utánkövetése javasolt, melynek során a klinikum megítélésén túl a BKI (boka-kar index) mérése is szükséges. Bár az utánkövetést iletően konszezuson alapuló protokoll jelenleg nincs, a revascularizált végtag rendszeres ellenőrzése megteremtve egy esetleges sürgős szerviz beavat - kozás lehetőségét, növeli a hosszútávú nyitvamaradást. 594 vénás grafttal végzett bypasson átesett beteg bevonásával végzett klinikai vizsgálat nem igazolta a DUS (Duplex UH) szűrőjellegű vizsgálatként való alkalmazásának hatékonyságát sem a nyitva maradást, sem pedig a végtag megmaradást illetően; ugyanakkor kevésbé bizonyult költséghatékonynak mint a klinikai utánkövetés. Klinikai megfigyelésen alapul, hogy a Duplex UH hasznos lehet azon magas rizikójú műér graftok kiválasztásában, melyeknél tartós anticoagulálás szükséges a graft thrombosis megelőzése céljából.
9.4.3. Ajánlások az alsó végtagi revascularizációt követő aggregatio-gátló és antikoaguláns kezelésekre vonatkozóan
Ajánlás 87
Valamennyi alsó végtagi érszűkület miatt angioplasztikán átesett beteg esetében ajánlott az aspirinnal történő aggregatio-gátló kezelés, a szisztémás vasculáris események rizikójának csökkentése céljából. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 88
Legalább 1 hónapig aspirinnal és clopidogrellal/ - ticlopidinnel történő kettős aggregatio-gátló kezelés ajánlott infrainguinalis bare-metal stent beültetése után. (Evidencia szint: C) (I osztályú ajánlás)
Ajánlás 89
Infrainguinalis bypass műtéteket követően aspirinnel vagy aspirinnel és dipirydamollal történő aggregatio-gátló kezelés ajánlott. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 90
Autolog vénával történő infrainguinalis bypasst követően megfontolható K-vitamin antagonistával történő antithromboticus kezelés. (Evidencia szint: B) (IIb osztályú ajánlás)
Ajánlás 91
Térd alá vezetett, műér beültetésével végzett bypasst követően megfontolható az aspirin és clopidogrel kombinációjával történő kettős aggregatio-gátló kezelés. (Evidencia szint: B) (IIb osztályú ajánlás)
A thrombocyta aggregatio gátló kezelés azon túl, hogy a PAD-os betegek cardiovasculáris és cerebrovasculáris eseményeik számát potenciálisan csökkenti, javítja a revascularizált érszakasz nyitvamaradását is. 16 infrainguinalis reconstructióval foglalkozó study meta-analysisét végezték el a postoperatív thrombocyta aggregatió gátlószer kezelés hatékonyságára vonatkozóan. Az aspirinnel vagy aspirinnel és dipyridamollal történő aggregatió gátlást 12 hónappal a beavatkozást követően pozitív hatásúnak találták. Az alcsoport analysisek alapján a műér graftos betegek méginkább profitáltak a kezelésből, mint a vénás bypasson átesettek. A multicentricus, prospektív Dutch Bypass Oral Anticoagulants or Aspirin (BOA) vizsgálat 2690 alsó végtagi bypasson átesett beteget két csoportba randomizált: antikoaguláció (INR céltartomány 3.0-4.5 között) vs. thrombocyta aggregatió gátlószer kezelés (aspirin 80 mg/nap). A nyitvamaradásban összességében nem volt különbség, de az alcsoport vizsgálatok szerint a vénás graftok tekintetében az antikoaguláció az aspirinnel szemben javította az átjárhatóságot, ezzel szemben viszont az műerek vonatkozásában az aspirin bizonyult hatékonyabbnak szemben az antikoaguláns kezeléssel. Fontos megjegyezni, hogy a vérzéses szövődmények aránya kétszer gyakoribb volt az antikoagulált csoportban. Egy másik vizsgálatban 665 femoro-poplitealis reconstructión átesett beteget randomizáltak aspirin (325 mg/nap) + warfarin (a vizsgálat INR céltartománya: 1.4-2.8) vs. aspirin önmagában (325mg/nap) csoportokba. A vizsgálat nem igazolta a kettős therápia hatékonyságát a graftok átjárhatóságát illetően, bár az előnyösebbnek látszott a műér graftos betegek számára. A vérzésés szövődmények gyakoriságát a warfarin kezelés kétszeresére emelte. 56 magas rizikójú (gyenge kiáramlás, előnytelen vénás graft, vagy többszöri reinterventio szükségessége miatt) vénás bypasson átesett beteg anyaga alapján összehasonlították a warfarin (INR céltartomány: 2.0-3.0) + aspirin (325mg/nap) hatékonyságát az aspirin önmagában való alkalmazásával (325 mg/nap). Igazolódott, hogy a 3 éves kontrollnál szignifikánsan magasabb volt a graft nyitvamaradás és a végtagmentés aránya a kombinált terápiában részesülőknél, viszont emelkedett a vérzéses szövődmények gyakorisága is. A térd alá vezetett bypasson átesett betegeket vizsgáló CASPAR (Clopidogrel and Acetylsalicylic Acid in Bypass Surgery for Peripheral ARterial disease) randomizált, kettős-vak study-ban megvizsgálták, hogy a clopidogrel+aspirin kezelés szemben az aspirin monoterápiával javítja-e a primer átjárhatóságot, a végtagmentés arányát és a betegek túlélését. A randomizált 851 beteg 70% vénás 30% műérrel történt reconsruction esett át. 1 éves utánkövetés után a két csoport között nem volt különbség a primér végpontokat illetően. Az alcsoport analysis a clopidogrel+aspirin therápia előnyös hatását jelezte a műéres csoportban.
Három prospektív, randomizált klinikai vizsgálat foglalkozik az infrainguinalis ballon angioplasztikát és stentelést követő anticoaguláns terápia szerepével. A nyitvamaradásra vonatkozóan ezen vizsgálatok egyike sem igazolta az antikoagulálás hatékonyságát, viszont a vérzéses szövődmények számának emelkedését észlelte. Jelen pillanatban az antikoaguláns terápia rutinszerű alkalmazása nem ajánlható alsó végtagi endovasculáris beavatkozásokat követően.
Újabb angiogenesisen alapuló terápiák fejlődése – mint az őssejt kezelés vagy az angiogeneticus faktorok alkalmazása - a neovascularizáció stimulácója révén a collateralis keringést fokozzák, így csökkentik a panaszokat, s akár a végtagvesztést is megelőzhetik. Ez idáig egymásnak ellentmondó eredményeket publikáltak, egyes vizsgálatok a panaszok mérséklődését, a járóképesség javulását és az amputációk számának csökkenését vélték igazolni, mások ezen bíztató eredményeket viszont nem tudták megerősíteni.
Emberben az autológ sejt átültetés forrásai a csontvelőből és a vérből izolált őssejtek és progenitor sejtek lehetnek. Jelenleg leginkább a csontvelő eredetű sejteket alkalmazzák, mert ezek használatához nem szükséges bonyolult izolációs eljárás; ugyanakkor terápiás előnyt jelenthet, hogy több őssejt típust is tartalmaznak, szemben a szelektált, azonos sejtvonalhoz tartozóakkal. Az őssejt terápiára használható számos sejttípus közül egyelőre nem egyértelmű, hogy melyik a legígéretesebb. 37 vizsgálat meta-analizise az autológ sejtterápiát találta a leghatásosabbnak a szubjektív panaszok csökkenése, az ischemiás index javulása és a végpontok (fekély gyógyulás, amputáció) tekintetében egyaránt. Az őssejt kezelés általában eredményesebb Bürger kórban szenvedő betegeknél, mint arteriosclerosis obliteransban. A TAMARIS study a legnagyobb randomizált, placebo kontrollált gén-terápiás vizsgálat, melybe 30 ország több mint 520 olyan toficus zavarral bíró, KVI-s (kritikus végtagischemia) betegét vonták be akik revascularizációra alkalmatlanok voltak. A csoportok között nem volt szignifikáns különbség az elsődleges végpontok vonatkozásában (exitus letalis, a kezelt végtag maior amputációja). Jelenleg az angiogeneticus gén terápia és az őssejt-terápia intenzív kutatás tárgya, s így alkalmazásukkal kapcsolatos erős ajánlások megfogalmazása túl korai volna.
10. Krónikus kritikus végtag ischaemia kezelése [1-3]
A krónikus KVI kezelése komplex multidisciplináris ellátást igényel, mely magában foglalja az atherosclerois rizikó - faktorainak kontrollját, a revascularizáció lehetőség szerinti maximális kivitelezését, korszerű sebkezelést, megfelelő cipő viselését, a gyulladás kezelését és a korai rehabilitációt.
Ajánlás 92
KKVI-ben amikor csak lehetséges revaszkularizáció ajánlott a végtag megmentésére. (Evidencia szint: A) (I osztályú ajánlás)
Ajánlás 93
Amennyiben technikailag kivitelezhető és elérhető, első vonalbeli kezelésként endovaszkuláris beavatkozás javasolt. (Evidencia szint: B) IIb osztályú ajánlás)
Ajánlás 94
Amennyiben revaszkularizáció nem lehetséges prostanoid kezelés megfontolható. (Evidencia szint: B) (IIb osztályú ajánlás)
10.1. Gyógyszeres kezelés
Ajánlás 95
7-28 napos, parenteralis PGE-1 vagy iloprost kezelés megfontolható KVI-ben szenvedő betegekben, az ischaemiás fájdalom csökkentése és a fekély gyógyulás elősegítése céljából. (Evidencia szint: B) (IIb osztályú ajánlás)
Abban az esetben, ha KKVI esetén nincs lehetőség revascularizációra, illetve a mérsékelt effektivitású revascularizáció kiegészítése szükséges, a gyógyszeres kezelés a kötelező thrombocyta aktiváció gátlása és statin terápia mellett prostanoidokkal mutatott némi pozitív hatást randomzált vizsgálatok alapján. Az eredmények azonban még nem egyértelműek, további vizsgálatok szükségesek az evidencia szintjének javítása érdekében. PGE1 vizsgálatok az ischemiás fekély méretének csökkentését mutatták. Az Iloprosttal történt vizsgálatok nagyobb esélyt adnak a túlélésre (55% vs. 35 %) és a végtagok megtartására valamint úgy tünt hogy az esetek körülbelül 40%-ban hasznosnak bizonyult a kezelés azoknak a betegeknek, akiknek revascularizáció nem kerülhetett szóba. Nehéz azonban előjelezni a hatásosság mértékét a hosszú ideig tartó kezelésnek, ezért műszeres diagnosztikával pontosan meghatározott esetekben javasolt csak az alkalmazása.
További potenciális lehetőség a terápiás angiogenezis, melynek eredményességéről illetve az alkalmazás módjáról még nem áll rendelkezésre elégséges adat.
10.2. Endovaszkuláris kezelés
Lásd 9.3. fejezet
10.3. Thrombolysis
Akut kritikus végtagischemia (AKVI) gyógyszeres kezelésére katéteres thrombolysis, mechanikus thrombus extrakció és aspiráció kerülhet szóba. Fontos azonban a megfelelő stratégia meghatározásához annak eldöntése, hogy thrombussal vagy embolussal állunk-e szemben, hová lokalizálható az elzáródás, mennyi ideje áll fenn az ischemia, natív arteriával vagy grafttal allunk-e szemben.
Ajánlás 96
A katéteres thrombolysis hatékony és előnyös, ezért indikált 14 napnál rövidebb ideje fennálló akut végtag ischaemiában (Rutherford I és IIa). (Evidencia szint: A) (I osztályú ajánlás)
Az intraarteriás thrombolysis különböző thrombolytikumokkal lehetséges. Úgy tűnik hatékonyabbak, ha a készítményt a thrombusba jutattjuk Szisztémás thrombolysisnek nincs helye akut kritikus végtag ischemiában. A legjobb eredményt akkor észlelték, ha a kezelés a tünetek jelentkezését követő két héten belül történik meg. Ezt követően nem volt már hatásosabb, mint a klasszikus sebészi megoldások.
Ajánlás 97
Kiegészítő kezelésként mechanikus thrombectomiás eszközök használhatóak perifériás artériás elzáródás okozta akut végtag ischaemiában. (Evidencia szint: B) (IIa osztályú ajánlás)
Mechanikus thrombuseltávolítás lehetséges önmagában, illetve thrombolysissel kombinálva, aminek előnye, hogy csökkenti a reperfúzióig eltelt időtartamot.
A legmodernebb, amikor a két módszert együttesen alkalmazzák, ami csökkenti a 6 hónapos amputáció rátát.
Ajánlás 98
Katéteres thrombolysis vagy thrombectomia megfontolható 14 napnál hosszabb ideje fennálló akut végtag ischaemiában (Rutherford IIb). (Evidencia szint: B) (IIb osztályú ajánlás)
A két hétnél később végzett katéteres thrombosis és/vagymechanikus thrombectomia hatása kevésbé kifejezett, így csak válogatott esetekben javasolható.
10.4. Sebészi kezelés
Lásd 9.4. Alfejezet
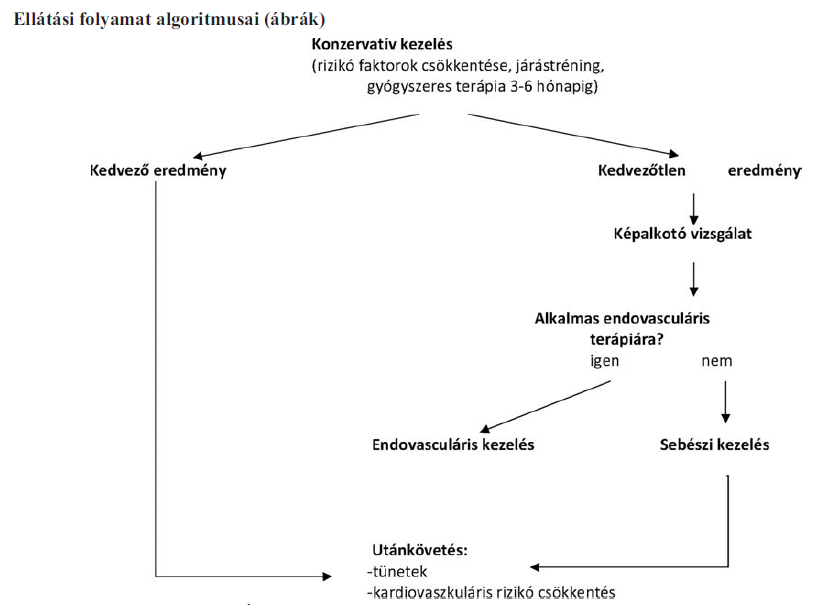
1. ábra
A claudicatio intermittens ellátásának algoritmusa
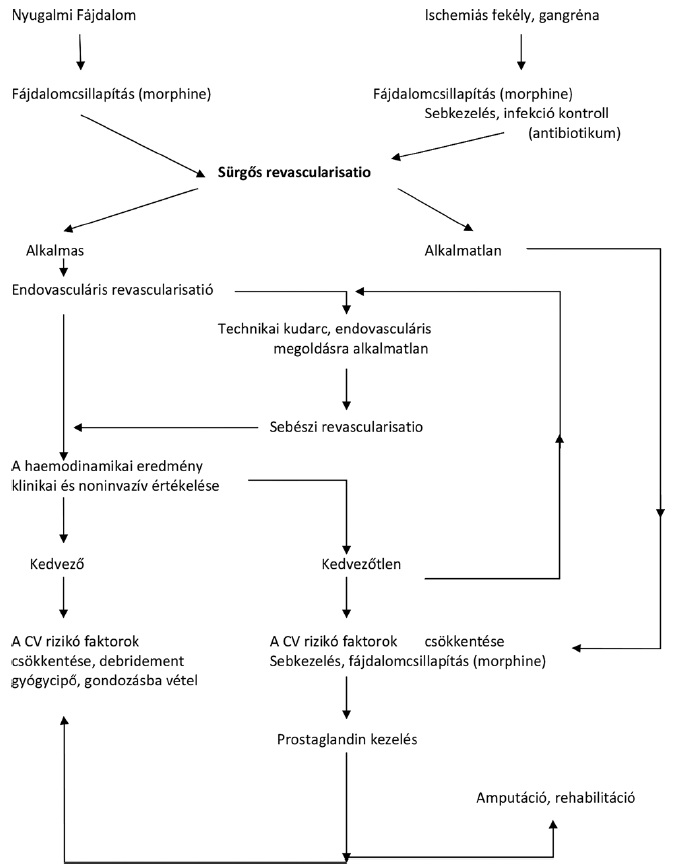
2. Ábra.
A kritikus végtag ischaemia ellátásának algoritmusa
Írta: Emberi Erőforrások Minisztériuma
Érbetegségek: 2017/2. 41-62. oldal


