Acut subarachnoidealis vérzést, a vérzés kialakulásával egyidőben és azt követően 48-72 óráig mutatja ki a CT. Ezt követően a vérzés isodenssé válik, ekkor az esetleges szövődmények (oedema, infarktus, hydrocephalus) kimutatására, vagy kizárására alkalmas a CT. Bizonyos kautelák figyelembevétele mellett kimutathatja a tünetmentes aneurysmát. Nem váltja ki azonban a CT a 4 ér angiográfiát, mellyel kimutatható az esetleges multiplex aneurysma, a vasospasmus mértéke és kiterjedése.
Érbetegségek: 1996/2. - 13-25. oldal
KULCSSZAVAK
Agyi aneurysmák, subarachnoidealis vérzés, CT-vizsgálat, vasospasmus
Bevezetés
A circulus Willisii-t alkotó erek, nem egyszer multiplex aneurysmájának rupturáját követően kialakuló acut subarachnoidealis vérzés műtéti megoldása az acut szakban vitális indikációt jelent. Célom az volt, hogy meghatározzam, milyen az információs tartománya a CT-nek a "néma" aneurysmák diagnosztikájában, acut subarachnoidealis vérzésben, kiválthatja-e a CT a 4 ér angiográfiát, milyen lehetőséget nyújt a beteg követésében.
1. Vérzést megelőző időszak
a.) Klinikum
A congenitális éranomaliákra az esetek túlnyomó többségében a rupturát követő acut (subarachnoidealis) vérzés hívja fel a figyelmet. Aneurysma, mint differenciális diagnosztikai probléma jön szóba valamely agyidegtünet (n. oculomatorius laesio, n. opticus atrophia, chiasma tünetcsoport), pedunculus compressio, epilepsziás rosszullétek elemzésében. A "migrain ophthalmologique" leggyakoribb oka az artéria communicans posterior eredésénél elhelyezkedő aneurysma. Aneurysmák lehetnek transiens ischaemiás attack hátterében, okozhatnak reverzibilis ischaemiás károsodást, de vezethetnek "progressing stroke"-hoz is.
b.) Pathológia (19)
Az aneurysma az érfal körülírt tágulata, az esetek túlnyomó többségében az érfal veleszületett anomáliájának következménye. A saccularis aneurysma leggyakrabban az a. carotis interna elágaződásánál, az a. cerebri anterior és a. communicans anterior találkozásánál és az a. cerebri posterior, a. communicans posterior egyesülésének környékén helyezkedik el. Aránylag ritkább az a. cerebri anterior és az a. cerebri média distális ágainak területében. Az aneurysmák az a. basilarison, ahol műtéti megoldásuk igen nehéz, csak mintegy 15%-ban fordulnak elő. Az aneurysma az esetek 20%-ában többszörös. A saccularis aneurysmák manapság, mint műtéti anyag kerülnek szövettani vizsgálatra.
Az aneurysmák nyakánál megszűnik a normális artéria szerkezet. A média hiányzik, az elastica interna degeneratív elváltozásokat szenvedett. Magának az aneurysma falának a szerkezete szabálytalan, sok helyen csak kötőszövetből áll, másutt rendszertelenül találjuk meg az érfalat felépítő szövetelemeket. Ez mutatja, hogy az aneurysma nem hegesedés, hanem fejlődési anomália. A szabálytalanul felépített gyenge érszakaszok adnak alkalmat az aneurysma megrepedésére. Hegesedést legfeljebb a tisztán kötőszövetes szakaszok jelentenek. Az aneurysmákban történtekről tanúskodnak a haemosiderin szemcsék, mint az időnként lezajlott vérzés jelei.
c.) CT elváltozások (27)
AneurysmaAneurysma
A natív felvételen hyperdens, posztkontrasztosan általában homogén halmozást mutató, jellegzetes lokalizációjú elváltozás. Inhomogén lehet a giant aneurysma halmozása, ha falában vagy lumenében thrombus van. Néha az aneurysma falában finom vonalas vagy rögös mész van (1. ábra). Az aneurysma CT-vel való kimutathatósága függ:
- nagyságától (5-6 mm-nél nagyobb),
- falának mésztartalmától,
- kontraszthalmozásától,
- a készülék felbontóképességétől.
Nem ábrázolódik az aneurysma:
- ha kicsi, és nem meszes falú,
- ha a vérzés elroncsolta,
- ha a vérömlenyen belül helyezkedik el, és ennek hyperdensitása az aneurysmáét elfedi,
- ha thrombotizált,
- ha vasospasmus következtében nem telődött.
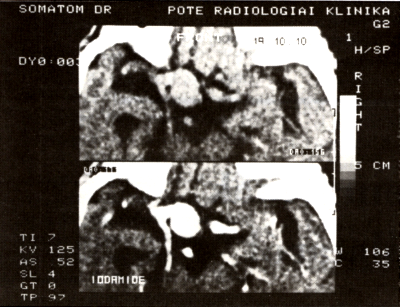
1. ábra:
Bal artéria cerebri anterior vagy communicans anterior aneurysmája.
2. Acut subarachnoidealis vérzés (1, 2, 23)
Az aneurysma megrepedésének jellegzetes klinikuma: a beteg hirtelen, ütésszerű fejfájást érez, melyet követően változó mértékű agytörzsi tudatzavar (somnolentia, sopor, coma) jelentkezik. Meningeális izgalmi tünetek, esetleg n. oculomotorius laesión kívül neurológiai kórjel nem szokott lenni, romló neurológiai status szövődmény jele.
CT elváltozások: (2. ábra) (1, 2, 5, 23, 27)
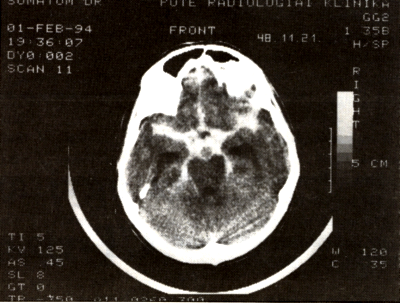
2. ábra:
Acut subarachnoideális vérzés:
a basalis cisternákban lévő vér körberajzolja az artéria basilarison elhelyezekdő aneurysmát.
A jobb Sylvius árokban tócsaszerű vérgyülem a jobb artéria cerebri médián lévő aneurysma rupturájának gyanúját veti fel. Műtét: acut vérzés a jobb artéria cerebri média aneurysmából chronicus vérzés jelei az artéria basilaris aneurysma környezetében.
Az ictust követő első 24 órában végzett vizsgálaton a subarachnoidealis vérzés jellegzetes képét látjuk. Masszívan, homogénen hyperdensek a basalis cisternák, a Sylvius árkok, a fissura interhemisphaerica anterior, finoman foltosán hyperdens a convexitást borító subarachnoidealis tér. A kamrarendszer változó mértékben lehet hyperdens. A hyperdensitás, a vérzés súlyosságától, a liquorterekben lévő vér mennyiségétől függően kb. 3-5 napig látható. A hyperdensitás megszűnése emellett a liquorcirculatio sebességétől függ. Típusos anamnesis és klinikai jelek esetében, ha a vizsgálat 24 órán túl történt, és esetleg vér már nem mutatható ki, CT-vel az acut subarachoidealis vérzés lehetősége nem zárható ki. Maga az aneurysma a hyperdensitáson belül nem különíthető el, és nem is lehet célja a vérzésforrás pontos megjelölése a CT-nek. A subarachnoidealis térben a vérzés eloszlásának jellegzetességei lehetnek: így a fissura interhemisphaerica anterior hátsó harmadában és a praeclinoidealisan, a basalis cisternákban lévd masszív hyperdensitás a. communicans, esetleg a. cerebri anterior, a fissura Sylviiben, a. cerebri média, esetleg az a. carotis interna supraclinoidealis szakaszának, a c. ambiens féloldali masszív hyperdensitása a. communicans posterior aneurysma ruptura jele lehet. Az agytörzset övező cisternák hyperdensitása, mely már esetleg supratentorialisan nem követhető, a. basilaris aneurysma lehetőségére hívja fel a figyelmet (5, 27).
3. A subarachnoidealis vérzés korai szövődményei
A tudatzavar változatlan volta, esetleges további romlása, fokális neurológiai kórjelek megjelenése a korai szövődményekre hívja fel a figyelmet.
Ezek lehetnek:
- a vérzés ismétlődése,
- agyoedema,
- hydrocephalus,
- vasospasmus, melynek következményeként anaemiás vagy haemorrhagiás infarctus alakulhat ki (8),
- állományi vérzés.
Ezek együttesen az intracraniális nyomás emelkedéséhez vezethetnek, így ennek tünetcsoportja tovább rontja a beteg állapotát és megváltoztatja a CT-s elváltozásokat. A fenti elváltozások elkülönítésére, esetleges izolált, vagy egymással kombinálódó megjelenésének ábrázolására alkalmas a CT.
A vérzés ismétlődésére a klinikai tünetek mellett a CT ad információt. Az első vérzést követően - szövődménymentes esetekben - a subarachnoidealis tér már liquordensitású, a vérzést követő első 3-5 napon túl. Vérzés ismétlődésére hívja fel a figyelmet, ha ezen időhatáron túl is az extra- és intracerebrális liquorterek hyperdensek, vagy a korábbi hyperdensitás súlyosabb.
Agyoedema:
Az acut subarachnoidealis vérzés számos esetben az acut szakban a vér-agy gát károsodásához vezet. Dóczi (4) és munkatársai klinikai és állatkísérletes megfigyeléseket folytatva, megállapították, hogy a permeábilitás-fokozódás az agy-vízháztartási, azaz térfogatszabályozási zavart okoz. Az agy elektrolit, és víztartalmát három sejtcsoport (a capilláris endothel, a plexus chorioideus secretoros sejtjei és az astroglia), valamint a Pacchioni granulatio képletei szabályozzák. E membránok vízpermeabilitását a keringésben lévő vasopressin (AVP) szabályozza. Subarachnoidealis vérzésben szenvedő betegek jelentős hányadában észleltek AVP secretio fokozódásra utaló agyoedemát. Tekintettel arra, hogy a liquorban több olyan hormont is izoláltak (22, 30), amelyek a szervezet folyadék homeostasisának ismert szabályozói (AVP, atriális natridiureticus peptid-ANP, endogen digoxin), és melyek nem a szisztémás keringésből, hanem közvetlenül a hypothalamusból jutnak a liquorba és az interstitiális folyadékba, azt feltételezik, hogy az agyszövet víz- és folyadékháztartását centrális, a perifériától az agyi gátrendszerek által elválasztott és független neuro-endocrin rendszer szabályozza. Állatkísérletek alapján arra a következtetésre jutottak, hogy a liquor AVP tartalmának acut, valószínűleg rövid ideig tartó nagyfokú emelkedése a capilláris permeábilitás növelése útján szöveti vízakkumulációt eredményez, legyőzve a plexus chorioideus és a liquor-felszívó apparátus ellentétes irányú hatását. Acut subarachnoidealis vérzésben szenvedő betegnél intracraniális nyomás monitorizálásának a kezdetén a magas (20 Hgmm-nél nagyobb) intracranialis nyomás esetén a liquor és a plazma AVP szintje szignifikánsan magas volt. Az agyoedema izoozmolaris Glycerinnel történő csökkentésében a Glycerin amellett, hogy elsődlegesen ozmotikus dehydrálószerként is hathat, a barrieren átjutva gyorsan képes csökkenteni a liquor Na koncentrációját - hígításos mechanizmussal, illetve a plexus chorioideus és az ependyma Na-transportjának befolyásolásával. Ez mind a szisztémás, mind az ún. centrális AVP felszabadulást gátolja. Az agyszövet ennek következményeként dehydrálódik, oly módon, hogy előbbi a szérum hyperozmolaritását, az utóbbi az agyi capillárisok vízperme- abilitásának csökkentését hozza létre. CT-n jól ábrázolódik a félteke vagy az egész agy oedemája: a sulcusok elkeskenyednek, a gyrusok szélesek, a kamrarendszer kifejezetten szűkké válik, a basalis cisternák szűkek, esetleg tentoriális, tonsilláris herniatio jelei láthatók. A féltekék szabályos szerkezete nehezen ismerhető fel, a fehér- és szürkeállomány határa elmosódott lesz (3. ábra). CT-vel követhető az oedema csökkenése is.
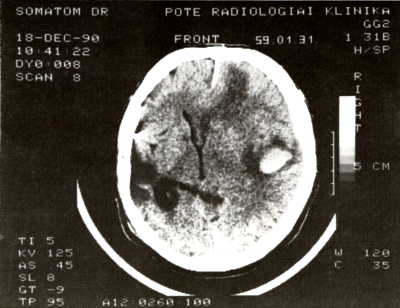
3. ábra:
A jobb temporalis lebenyben és Sylvius árokban vérzés látszik, melynek forrása a jobb a. cerebri média aneurysma rupturája. A perifocalis oedemát a vérzést övező hypodensitás, a jobb félteke globális oedemáját szerkezetének elmosott volta, az extracerebralis liquorterek virtuális jellege jelzi. A kamrarendszer a contralateralis oldalra dislocált és a funkcionális Monro blockád jeleként a bal occipitalis szarv tág.
Hydrocephalus: (4., 5/a., 5/b. ábra)
Foltz és Ward (6) az acut subarachnoidealis vérzést követően kialakuló hydrocephalusnak acut és chronicus formáját különíti el.
Az acut forma órákkal, napokkal a vérzés után alakul ki, véralvadékkal tömeszeli el a foramen Magendie-t és a basalis cisternát.
A chronicus forma 2-6 héttel az ictus után alakul ki. A basalis cisternákat és a convexitáson nagy területeket fibrosis tölt ki, arachnitis alakul ki, mely részben a liquorkeringést, részben az abszorpciót akadályozoza. Yasargil (31) hívta fel a figyelmet ezen állapotokban a shunt-műtét fontosságára.
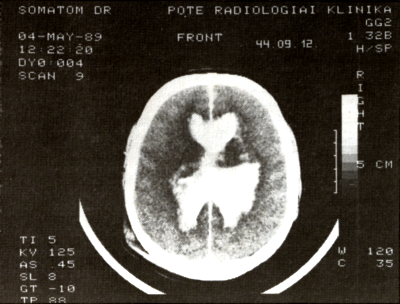
4. ábra:
A tágult kamrarendszert feszesen vér tölti ki: haemocephalus.
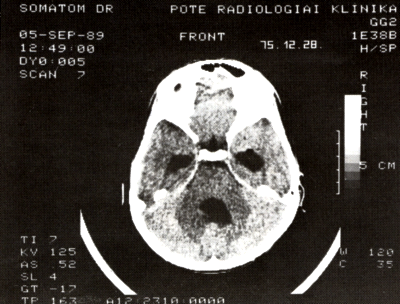
5/a. ábra:
15 éves fiú, a vizsgálat előtt 1 héttel acut subarachnoideális vérzés, melynek forrása angiográfiával sem volt tisztázható.
Klinikailag akinetikus mutismus.
A IV. kamra tág, a bal recessus lateralisban lágyrészdensitású terime.
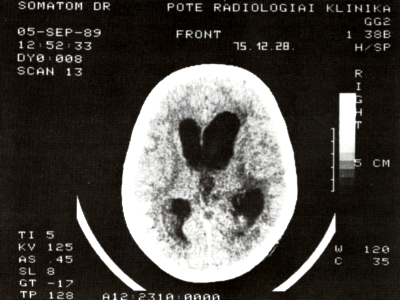
5/b. ábra:
A supratentorális kamrarendszer is nagy mértékben tágult, mindkét occpitalis szarvban szabálytalan, lágyrészdensitású terime.
Vélemény: hydrocephalus, ventriculitis (liquorlelettel is igazolt).
Julow (15) szerint a hydrocephalust okozó fibrosisnak a következő fokozatai vannak:
0. fokozat: nincs eltérés.
1. fokozat: minimális elváltozás; enyhe arachnoidea megvastagodás, helyenként tibrosis.
2. fokozat: kifejezetten arachnoidealis megvastagodás, keringési zavart okozó fibrosis.
3. fokozat: a subarachnoidealis tér diffúz fibrosisa, mely keringési zavart okoz.
4. fokozat: a subarachnoidealis tér teljes elzáródása, ahol már keringés nem lehetséges.
A liquor keringésdinamikájára hasznos vizsgálat az izotópos liquorkeringési vizsgálat, mellyel vizsgálható, van-e elzáródás valamely liquorútban, elhúzódik-e a felszívódás, van-e kamrai reflux. Az irodalomban acut subarachnoidealis vérzést követően a klinikai állapottal korreláló liquordina- mikai elváltozásokat találtak (4, 5).
CT: a vizsgálattal jól követhető a kamrarendszer tágasságának változása, a hydrocephalus non-occlusív jellege. Az esetek egy részében az arachnitis, ventriculitis finom jelei láthatók. A CT lehetőséget ad annak elkülönítésére, hogy a liquorkeringési zavarban esetleg magának a vascularis malformatiónak a lokalizációja ad magyarázatot, vagy a vérzést követő arachnitis felelős érte. Ugyancsak jól követhető a shunt beültetését követően, annak működése.
Vasospasmus: (6. ábra)
Az intracraniális aneurysma rupturából származó subarachnoidealis vérzés egyik következménye és kísérő jelensége lehet a vasospasmus. Robertson 1949-ből származó leírása óta számos közlemény számol be a vasospasmus okozta ischaemiás idegrendszeri elváltozásokról, kutatva annak lehetséges okait. A kutatások részben modellkísérleteken, részben klinikai megfigyeléseken alapulnak. Avasospasmus aetiológiája nem tisztázott. Számos szerző számol be a vasospasmus lehetséges okáról, de csaknem ugyanannyi tanulmányban olvashatunk a korábbi adatok cáfolatáról, és más tényezőket figyelembevéve újabb hatásmechanizmusokról.
Ezen kutatások közös alapja, hogy a subarachnoidealis vérzés kezdetekor meginduló kórélettani mechanimusok révén a spasmus fokozatosan súlyosabbá válik, bár egy ideig klinikai tüneteket nem okoz. Egy nem definiálható, kritikus ponton túl az erek legkisebb szűkülése is jelentősen fokozza az ischaemiát. Az irodalom szerint a vasospasmus önmagában ischaemiát nem okoz. Bár kétségtelen, hogy a vérzést követó'intracraniális nyomásfokozódás, a megváltozott vérkeringési és liquorkeringési dinamika, esetleg a műtét (nagy éren történő' manipulatió, marginális ischaemia) tovább ronthatják a spasmus hatását, de egyértelmű oki tényezőként nem fogadhatók el.
Hansen (12) szerint a haemoglobin vasoaktív anyag, amely a széteső vörösvértestekból a 2.-4. napon lép ki, gyulladásos jellegű vasculopathiát (subintimális szövetszaporulat, myonecrosis) okozva, mely kb. 6-12 hétig tart. A vasospasmus autoregulatiós zavart okoz, amely eredményeként csökken az agyi erek CO2 érzékenysége. A calcium blokkoló Nimodipine csökkenti az intracellularis calcium koncentrációt, és így protektív hatású az idegsejtek ischaemiás károsodásában. A hypervolaemia, haemodilutió szerepét vizsgálva megállapítja, hogy a csökkent vérnyomás, a túlzott antihypertenzív kezelés, a vér fokozott viszkozitása és a túlzott thrombus képződési hajlam vasospasmust előidéző okok.
Hirashima (13) és munkatársai vizsgálták a thrombocyta funkciót, a thrombocyta aktiváló faktort (PAF) és a PAF acetylhydrolase aktivitást, valamint az antiphospholipoid antitest (aPLs) koncentrációt vasospasmusban. Úgy találták, hogy megnövekedett a plasma PAF és PLs szint a subarach- noideális vérzést követő vasospasmusban.
Kasuya (17) szerint a subarachnoideális vérzés következményeként kialakuló vasospasmus oka az endothel-dependens vasodilatatio károsodása. Normál körülmények között az endothelsejtek által felszabadított NO biztosítja a simaizomsejtek relaxáciőját, aktiválva a guanylate cyclase solubilis formáját az izomsejtekben. Állatkísérletekben azt találta, hogy solubilis guanylate cyclase szint csökkent, és feltételezi, hogy ez játszik szerepet az endothel-dependens vasodilatatio károsodásában.
Sano (26) szerint az ischaemiás elváltozások az intracraniális nyomásfokozódással függnek össze. A szabad radicalisok felszaporodnak, mert a liquorkeringést a megnövekedett intracraniális nyomás akadályozza. Ezek a szabad radicalisok lipid peroxidatiót okoznak. A lipid peroxidatió a membrán phospholipidek, különösen a phosphatidylcholine (PC) és a phyophatidylethanolamine (PE) csökkenését eredményezik, és megemelkedik a diacylglycerol (DAG) intracellularis szintje, valamint az intrinsic protein kinase C (PKC). A szabad radicalisok subendothelialis sejtproliferá- ciót, myonecrosist okoznak. Az intracellularis DAG szint emelkedése és a PKC rendszer aktiválódása eredményezi emellett a simaizomsejt tartós összehúzódását. így kialakul a vasospasmus képe, amely felelős az ischaemiás elváltozásokért.
Haciyakupogli (10) megfigyelései szerint is a szabad radicalisok vasculopathiát okoznak. A glutathione protektív hatású az ischaemiás kárododásokban. Kisebb mértékű vasospasmust talált az intraarteriálisan glutathionével kezeitekben, mint az intracisternálisan adott kezelések esetében és a kontroll csoportban. Az arteriafal elváltozása ezzel korrelált.
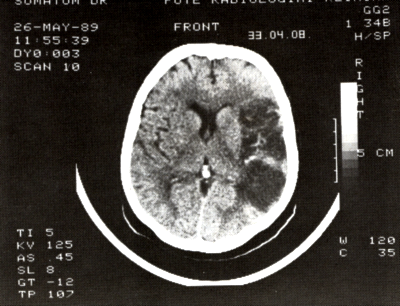
6. ábra:
Jobb artéria cerebri média aneurysma rupturát követően kialakult anaemiás infarctus a fehérállományban, mely a törzsdúcokat és a jobb oldalkamrát comprimálja.
Afsar (3) abból a feltevésből kiindulva, hogy az oxihaemoglobin vasocontrictív hatású, és a NO rapidan megköti, úgy gondolta, hogy a subarachnoideális vérzést követő vasospasmus kialakulásában a NO csökkenésének van szerepe, mely NO jelentós a normál agyi vasotőnus fenntartásában. Kísérleti úton létrehozott vasospasmus kapcsán, NO infúzióval kezelt állapotban a következő megfigyeléseket tette: NO hatására megnövekedett az agyi átáramlás, csökkent a cerebrovascularis resistentia, megelőzhető volt az angiográfia által előidézett vasospasmus, csökkent a vérátáramlás sebessége a vasospasticus artériákban, anélkül, hogy a szisztémás vérnyomás csökkent volna. Felveti a NO therápiás jelentőségét.
Mosiewicz (21) tanulmányában a vasoactív neuropeptidek szerepét ismerteti a vasospasmus kialakulásában. A calcitonon-Gene-Related-Peptid (CGRP) és a Vasoactive Intestinal Polypeptid (VIP) csökkenése okozná a vasospasmust subarachnoidealis vérzést követően. Ezek a peptidek vasodilatátorként hatnak az agyi erekre. A subarachnoidealis vérzést követően az 1.-2. héten a periarteriális idegrostokban koncentrációjuk szignifikánsan csökken, és az okozná a vasospasmust.
Juul (16) betegekben vizsgálta a CGRP, a substance P (SP) és a Vasoactive-Intestinal-Peptide (VlP)-like immunre- activity (LI) szintet a véna jugularis externában és a liquorban közvetlen a subarachnoideális vérzést követően, az aneurysma clippelését követően Nimodipine kezeléssel kombinálva. Szignifikáns korrelációt talált a vasospasmus-index és a CGRP-LI szint között. Nem találtak változást az SP és a VIP-LI szintben. Feltételezi, hogy a vasospasmus kialakulásában a CGRP-nek van jelentős szerepe.
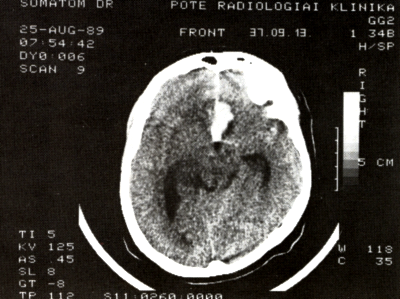
7. ábra:
Jobb oldalon frontobasalisan a fehérállományban keskeny perifocalis oedemával övezett vérzés látszik: a. communicans anterior vagy a. cerebri anterior aneurysma rupturából származó intracerebralis vérzés.
Mindkét peripeduncularis cisterna és pedunculus compressiója tentorialis herniatio jeleként.
Seifer (29) az endothelin koncentrációt vizsgálta subarachnoidealis vérzéses betegekben, összefüggésben a beteg életkorával, a vasospasmus fokával és a haemorrhagia kiterjedésével. Plazmában és liquorban meghatározta az endothelin (ET)-l, ET-3 és a makro ET-L koncentáriót. A liquor makro ET-1, ET-1 és ET-3 szint szignifikánsan magasabb volt subarachnoidealis vérzéses betegekben, mint a más betegségben szenvedőknek és a normál controllokban. Ugyancsak magasabb volt ezen endothelinek koncentrációja az idősebbekben, mint a fiatalokban. A postoperatív időszakban, amikor is a neurológiai tünetek alapján vasospasmus lehetősége merült fel, és ezt a Doppler vizsgálat megerősítette, magas szinten maradt, vagy tovább emelkedett az endothelinek szintje. Ahol nem alakult ki a postoperatív időszakban vasospasmus, ott időarányosan csökkent az endothelinek koncentrációja. A két csoport közt az eltérés szignifikáns volt.
Handa (11) feltételezte, hogy a vasospasmus immungyulladásos elváltozás, meghatározta az intracellularis adhesion molecule 1 (ICAM-1) eloszlást. Modell kísérletekben patkányok artéria basilarisában a subarachnoidealis vérzést követő 2. napon nemcsak az endothelben, hanem a médiában is kimutatott ICAM-t. Úgy gondolja, hogy a vasospasmus és a kísérő érfal elváltozás cellularis immunválasz.
Sakaguchi (25) humán lymphocyta antigén típusokat határozott meg subarachnoideális vérzésben szenvedőkben: a HLA-A31 szignifikánsan nagyobb frequentiával fordult elő, mint a HLA-B40. A vasospasmus és a következményes ischaemiás deficit eseteiben a HLA-Bw60 antigén szignifikánsan gyakrabban fordult elő, míg azokban a betegekben, ahol vasospasmus nem alakult ki, a HLA-Aw33 és Cw4 antigének gyakoribbak. Úgy gondolja, hogy a HLA-Bw60 antigén praedisponáló szerepet játszik a vasospasmus kialakulásában, míg a HLA-Aw33 és Cw4 protektív hatásúak.
Fisher (5) követte a suabarachnoidealis vérzés kialakulását követően a vérzés mennyisége és a suabarachnoidealis térben való megoszlása, valamint a kialakuló vasospasmus összefüggését. Erre érzékeny, és jól reprodukálható eljárásnak tartotta a CT-t. Azt tapasztalta, hogy a diffúzán a subarachnoidealis teret kitöltő vérzések esetében és amikor CT- vel a subarachnoidealis térben vért már nem látott, mert az ictus és a vizsgálat közt eltelt időben a vérzés már isodenssé vált, a vasospasmus kialakulásának már kisebb a veszélye. Feltételezése szerint, ha adott nagyságnál (körülírt vérzésnél 5x3 mm, diffúz vérzésnél 1 mm-nél vastagabb) nagyobb a cisternát kitöltő vérrög, nagy a valószínűsége az adott területen futó ér vasospasmusának. Befolyásolja ezt a liquorkeringés változása és az intracraniális nyomás emelkedése, mely következményes. Megfigyelései szerint legnagyobb a vulnerabilitása az a. cerebri anterior-communicans anteriornak, majd az a. cerebri médiának. Kisebb a rizikója a hátsó scala subarachnoidealis tereiben lévő vérgyülemnek, és így a secunder vasospasmus kialakulásának, mert itt a liquorcirculatiót a cisterna magna és a spinális subarachnoidealis tér sokáig biztosíthatja. Nagy a vasospasmus lehetősége az idősebb betegekben, mert itt a subarachnoidealis tér tág, és lehetőséget ad széles vérrög kialakulásának. A vasospasmus kimutatása, pontos lokalizációja, az esetleges collaterális keringés kimutatása az angiográfia feladata. CT-vel a következményként kialakuló anaemiás és haemorrhagiás infarc- tus jól kimutatható.
Intracerebrális vérzés: (7. ábra) (5, 9, 14, 20, 24)
A különböző aneurysma rupturából származó állományi vérzésnek jellegzetes lokalizációja van:
- az artéria cerebri anterior vagy communicans anterior aneurysmákból származó vérzés szétfeszíti a fissura interhemisphaerica anterior hátsó harmadát, és rendszerint mindkét oldalon frontobasalisan tör az állományba,
- az a. cerebri média aneurysmák a fissura Sylvii mélyén törnek a temporális fehérállományba,
- az a. communicans posterior aneurysmák a temporális pólus mediális részén roncsolnak,
- az a. basilaris aneurysmák a thalamus irányába törhetnek.
Gondos reconstructiókkal az állományba törés jól ábrázolható. A basis irányából történő vérterjedés útjának ábrázolása egyben elkülönítő jel lehet a hypertoniás vérzéstől, amelyben a vér felszínre törését a convexitás irányába széles, hyperdens sáv jelzi.
4. A korai praeoperatív szövődmények
A vérzés ismétlődése, oedema, ischaemiás károsodások, hydrocephalus stb. kimutatására a CT igen szenzitív. A szövődmények sora kibővülhet az egyéb, bármely a koponya megnyitásához társuló szövődménnyel, így a burki vérzések (episubdurális) kialakulásával. Ezek kimutatására alkalmas a CT (9/a., 9/b. ábra).
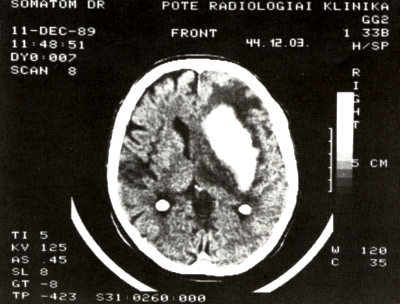
8/a. ábra:
Jobb oldalon a temporalis fehérállományban lencse alakú hyperdens terime, mely beterjed a nucleus lentiformisba. A jobb thalamus hypodens és comprimált.
Összenyomott a jobb frontalis szarv.
A vérzést perifocalis oedema övezi.
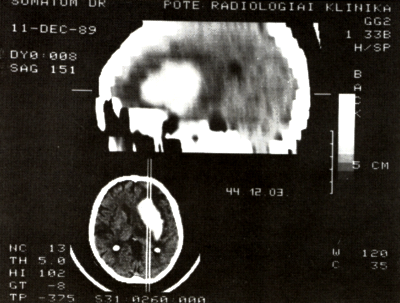
8/b. ábra:
Sagittális reconstructió: a vérzés a basalis cisternák irányából tör a temporalis fehérállományba. Vérzésforrás: a jobb artéria cerebri média, vagy a jobb carotis interna supraclinoideális aneurysmája.
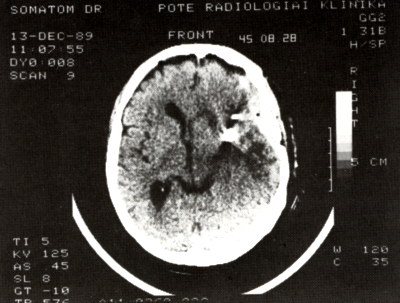
9/a. ábra:
Jobb artéria cerebri média aneurysma műtét. A craniotomiás lebeny alat sarló alakú terime jelzi a subduralis haematomát.
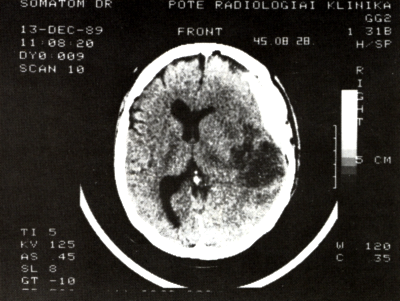
9/b. ábra:
A temporalis fehérállomány foltos hypodensitása a temporalis média ágak területében kialakult anaemiás infarctus jele.
A jobb félteke globális oedemáját jelzi, hogy a gyrusok szélesek, a sulcusok virtuálisak. A fenti folyamatok következményeként lingularis herniatio.
A beteg követése során a chronicus hydrocephalus, körülírt atrophia (10. ábra), ischaemiás károsodások ábrázolására, az ezekben bekövetkezett változások regisztrálására szintén alkalmas Az acut subarachnoidealis vérzés kezelésében alapvető elv, hogy CT-vel történő igazolást követően a 4 ér angiográfia végzése elengedhetetlen. Ezt követően, ha a beteg állapota megengedi (Hunt skála), az aneurysma tüneti ellátása következik. A korai műtét preventív jellegű, a vérzés ismétlődésének, a vasospasmus kialakulásának és az acut hydrocephalusnak a megelőzését szolgálja (1, 2, 5, 6).
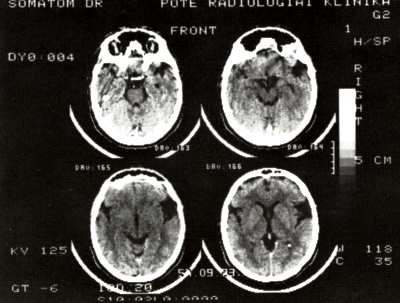
10. ábra:
32 éves nő. Jobb oldalon a perisylvicus és insularis cisternák körülirtán tágak: körülírt atrophia.
Az aneurysmák 8-29%-ban multiplexen fordulnak elő, és ezekben az esetekben a mortalitás 15-50%. A multiplex aneurysmák műtéti ellátásnak kérdése nem egységes. A vérző' aneurysmát ebben az esetben is azonnal el kell látni. Az aneurysma rupturából származó acut subarachnoideális vérzés. a koponya megnyitása, a vérző aneurysmán történő manipulatio, jelentősen megváltoztatja az agy haemodinamikai viszonyait. Ezen változások az asymptomás aneurysmák rupturáját idézhetik elő. így a még nem vérzett aneurysmá- kat is meg kell operálni egy ülésben, bár itt még az is vitás, hogy csak azokat-e, amelyek egy műtéti feltárásból elérhetők, vagy azokat is, melyek egy feltárásból nem érhetők el (11. ábra) (18).
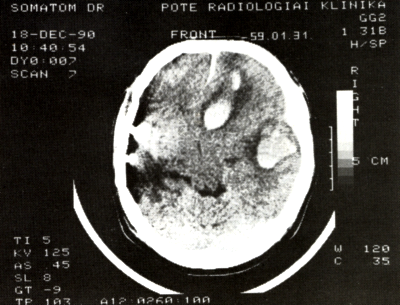
11. ábra:
31 éves férfi: 1988-ban a bal artéria cerebri média aneurysmájának műtéti zárása.
Ütésszerű fejfájás, comatosus.
Jobb oldalon frontobasalisan és temporalisan perifocalis oedemával övezett állományi vérzés, mely comprimálja és a falx-szal együtt a contralateralis oldalra dislocálja a kamrarendszert. Összenyomja a jobb pedunculust és az orális agytörzset balra dislocálja.
Jobb artéria cerebri anterior és artéria cerebri média aneurysma ruptura?
Irodalom
- Adams, H. P. et al: CT and clinical correlations in recent aneurysmal subarachnoid hemorrhage. A preliminary report of the Cooperative Aneurysm Study. Neurology (Cleveland) 33: 981-988, 1983.
- Adams, H. P.: Early management of the patient with recur- rent aneurysmal subarachnoidaeal hemorrhage. Stroke, 17: 1068-1070, 1986.
- Afsar, J. K. et al: Effect intracarotid nitric oxidé on primate cerebral vasospasm after subarachnoid hemorrhage. J. Neu- rosurg., 83: 118-122, 1995.
- Dóczi T.: Az agy térfogatszabályozása. Doktori disszertáció. 1992.
- Fischer, C. M. et al: Relation of cerebral vasospasm to subarachnoid hemorrhage visualized by computerized tomog- raphic scanning. Neurosurgery 6: 1-9, 1980.
- Foltz, E. et al: Communicating hydrocephalus from subarachnoideal bleeding. J. Neurosurg. 13: 546-549, 1956.
- Gács Gy. és mtsai: Az agyi arteriovenás angiomákról. Ideggyógy. Szemle, 25: 279-288, 1972.
- Gastaut, H.: Microangiographic study of ischemic cortical lesions. (Outside the supply-territory following carotid thrombosis) in: Cerebral circulation and stroke. Züich K. J. ed Berlin. Springer Verlag, pp. 23-39. 1971.
- Gates, P. C.: Primary intraventricular hemorrhage in adults. Stroke 17: 872-877, 1986.
- Haciyakupoglu, S. et al: Effect of GSH on cerebral vasospasm in dogs. Neurosurg. Rev. 17: 283-289, 1994.
- Handci, Y. et al: Epxression of intracellular adhesion molecule 1 (ICAM-1) on the cerebral artery following subarachnoid hemorrhage in rats. Acta Neurochir. 13: 2: 92-97, 1995.
- Hansen, D. et cd: Therapeutischer stellenwert von Kalziumantagonisten, hypervolamischer Haemodilution und induzierter arterieller Hypertension. Anaesthesist, 44: 219- 229, 1995.
- Hirashima, Y. et al: Platelet-activating factor and antip- hospholipid antibodies in subarachnoid hemorrhage. Acta Neurochir. 128: 144-149, 1994.
- Honton, D. R. et cd: The value of histological examination of surgically removed blood clot in determing the etiology of spontaneous intracerebral haemorrhage. Stroke, 15: 517- 520, 1984.
- Julow, J. et cd: Subarachnoidealis vérzés utáni változások a subarachnoideális térben. Ideggyógyászati Szemle. 34: 206-220, 1981.
- Juul, R. et al: Alterations in perivascular dilatory neuropeptides (CGRP, SP, VIP) in the external jugular vein and ín the cerebrospinal fluid following subarachnoide haemorr- hage in man. Acata Neruochir. 132: 32-41, 1995.
- Kasuya, H. et al: Nitric oxydesynthase and guanylate cyclase levels in canine basilar artery after subarachnoid hemon-hage. J. Neurosurg. 82: 250-255, 1995.
- Kopa J.: A multiplex intracranális aneurysmák és műtéti ellátásuk. Ideggyógy. Szemle Supp. 639-642, 1982.
- Környey I.: Neuropathológia. Akadémiai kiadó. Budapest, 1987.
- Krayenbühl M. et al: Small vascular malformations as a ca- use of primary intracerebral hemorrhage. J. Neurosurg. 22:7-11, 1965.
- Mosiewicz, A. et al: Vasoactive neuropeptides CGRP (cal- citonin gene-related peptide) and vasospasm during subarachnoid hemorrhage from ruptured intracranial aneurysm. Neurol. Neurochir. Pol.: 28: 899-905, 1994.
- Needlemann, ['.: The expanding physiological roles of atriae natriuretic factor. Nature 321: 199-200, 1986.
- Rinkel, G. J. E. et al: Subarachnoid hemorrhage without detectable aneurysm. Stroke, 24: 1403-1409, 1993.
- Sacco, R. L.: Subarachnoid and intracranial hemorrhage. Neurology (Cleveland) 34: 847-854, 1984.
- Sakaguchi, J. et al: HLA-type of cerebral vasospasm patients after aneurysmal subarachnoid hemorrhage. Neurosurg. Rev. 17: 67-71, 1994.
- Sano, K.: Acute ischaemic and delayed ischaemic neurological deficits as the causes of bad grading in aneurysmal subarachnoid haemorrhage. Neurol. Res. 16:35-39, 1994.
- Schinz Radiologische Diagnostic in Klinik und Praxis. Band V. Teil I. Georg Thieme Verlag, Stuttgart, New York, 1986.
- Shirakami, G. et al: Changes of endothelin concentration in cerebrospinal fluid and plasma of patients with aneurysmal subarachnoid hemorrhage. Acta Anaesthesiol. Scand. 38: 457-461, 1994.
- Seifert, V. et al: Endothelin concentrations in patients with cerebral vasospasm, deleyed ischemic neurological deficits and volume of hematoma. J. Neurosurg. 82:55-62, 1995.
- Tulassy T.: Pitvari natriureticus peptid és egyéb vasoactiv hormonok szabályozó szerepe a folyadék- és elektrolit háztartásban. Doktori értekezés, 1988.
- Yasargil, M. G.: The operatíve approach to aneurysms of the anterior communicating artery. In: Advances and Tech- nical Standards in Neurosurgery Vol. 2 113-115, 1975.
Dr. Nádor Györgyi
POTE Radiológiai Klinika
7624 Pécs, Ifjúság u. 13.
Érbetegségek: 1996/2. - 13-25. oldal


