A verőérbetegségek patogenezise a számos kísérleti és klinikai vizsgálat ellenére még nem teljesen ismert. Kísérleti adatok és klinikai megfigyelések utalnak arra, hogy a nyirokkeringés zavarának, az érfalból történő fehérjetranszport elégtelenségének szerepe van számos verőér-betegség kialakulásában, az érfalkárosodás létrejöttében és progressziójában. Az érfal táplásában az endothel rétegen keresztüli plazmaáramlásnak és az adventiliában lévő capillaris rendszernek (vasa vasorum) fontos szerepe van. Az érfalba filtrált protein- és lipoproteinmolekulák elszállítása azonban kizárólag az advenlitiában lévő nyirokércapillárisok (vasa lymphatica) útján történik. Ha az endothelréteg sérül, vagy kórosan megnő a lipoprotein-filtratio, úgy ezáltal az érfali nyiroktranszport dinamikus elégtelensége jön létre; a következmény: fehérje- és lipoproteinakkumuláció az érfalban, melyet fibrinlerakódás és érfalkárosodás követ. A verőérbetegségek ezen leggyakoribb típusa - endolheliális érkárosodás - mellett a másik, ritkább érbetegségtípus, az advenlitialis érkárosodás. Ilyenkor az adventitia körüli gyulladás és hegesedés a betegség kezdete. A következmény a vasa vasorum és a vasa lymphatica sérülése, ezt az érfali nyiroktranszpori súlyos zavara - az érfali nyirokkeringés mechanikai elégtelensége - követi.
A nyirokkeringés etiológiai szerepét bizonyítja a verőérbetegségek kialakulásában az, hogy az érfali nyiroktranszport károsításával állatkísérletekben érfali károsodást lehet létrehozni: ún. lymphaticus arteriopathiákat. A coronariák területén, az aorta ascendens és az artéria femoralis érterületén hoztak létre a szerzők lymphaticus arteriopathiát. Az érfal károsodását az érfal biokémiai sajátosságainak kóros megváltozása követi a nyirokkeringés blokádja után. Klinikai megfigyelések is utalnak a nyirokkeringés és a verőérbetegségek kapcsolatára. A mediastinalis nyirokcsomók megbetegedését, a mediastinalis nyirokcsomók röntgenbesugárzását nem ritkán coronariabetegség kialakulása követi. Lymphoedema területén nem ritka a helyi érkárosodás kifejlődése. A nyirokpangás elősegíti az atlierosclerosis kifejlődését és progresszióját. A nyirokkeringés és más érbetegségek kapcsolata még kevéssé ismert. E referátum fő célja az, hogy az ilyen irányú további vizsgálatok fontosságára rámutasson.
Érbetegségek: 1996/1. 8-14. oldal
KULCSSZAVAK
érfali nyiroktranszport, vasa lymphatica, érfali fehérjeakkumuláció, érfali károsodás, lymphaticus vasculo pathia, érbetegségek patogenezise
Az érbetegségek patogeneziséról alkotott ismereteink ugyan jelentősen gyarapodtak az elmúlt évtizedben, de az érbetegségek keletkezése és progressziója még nem teljesen ismert. A verőérbetegségek számos fajtája ismeretes ugyan és az érfalkárosodások szövettani képe változatos, mégis az érfali károsodás patomechanizmusa alapján kétféle típusú artériás betegség különíthető el: 1. Endotheliális típusú arteriopatiák; 2. Adventitiális típusú arteriopátiák.
A verőérbetegségek nagyobb része az endothel réteg sérülése, károsodása után - nagy részben ennek folyománya révén - alakul ki. Az intima károsodását követi rendszerint a média és adventitia megbetegedése. Az endotheliális arteriopátia fő képviselője az atherosclerosisos érbetegség.
Az adventitiális érbetegségek kialakulásában az adventitia károsodása az elsődleges. Az érfal körüli gyulladás, illetve az adventitiában lévő vasa vasorumok sérülése az érbetegség kiváltó oka. Az adventitia megbetegedése többnyire a média rétegére, ritkán az intimára is ráterjed. A vasculitisek nagyobb része és a periaortitis, periarteritis sorolható az adventitiális arteriopátiák csoportjába. A verőérbetegségek egyik közös vonása az, hogy kialakulásában több tényező játszik szerepet; pluricausalis eredetűek. Az utóbbi évtizedben végzett kutatások eredményei azt bizonyítják, hogy az artériafal nyirokkeringésének elégtelensége szerepet játszik bizonyos arteriopatiák kialakulásában. Kísérleti vizsgálatok eredményei és klinikai megfigyelések arra utalnak, hogy az artériafal nyirok drenázsának insufficienciája érbetegség kialakulására vezet. A jelen referátum célja egyrészt az, hogy az artériafal károsodásának kialakulásában a nyirokkeringés szerepére rámutasson, másrészt az, hogy tanulmányozza, feltárja a nyirokkeringés és az artériás érbetegségek patogenezise és progressziója közötti összefüggéseket.
Az érfal szerkezete és anyagcseréje
A verőérbetegségek kialakulásának megértéséhez át kell tekinteni az érfal szerkezetének, anyagcseréjének és vérellátásának sajátosságait. Az érfal funkciójának (értónus, vasodilatatio, vasoconstrictio) fenntartásához szükséges az érfali sejtek, szövetek vér- és 02-ellátása és az érfalba került salakanyagoknak az érfalból történő elszállítása. Az érfal táplálására és anyagcseréjénekfenntartására a transmurális plazmaáramlás, az adventitialis nutritív capillariskeringés (vasa vaso rum) és az adventitialis nyirok elszállítása (vasa lymphatica révén) szolgál. Az 1. számú ábrán szemléltetjük az érfali normális anyagcsere, O2 felvétel és fehérjetranszport sajátosságait.
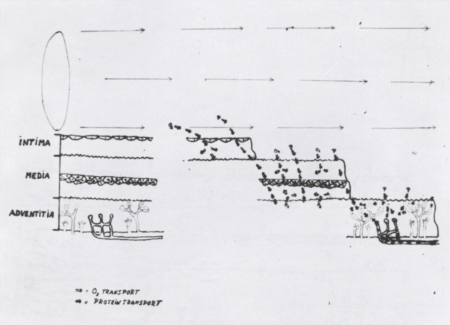
1. ábra.
Az érfalon keresztüli - transmuralis - normális anyagcsere. Az érlumenből az endothel rétegen keresztül O2, plazma (folyadék) és fehérje filtratio történik az intimába, majd innen a médiába és részben az adventitiába; O2 és plazma filtratio történik még az adventitiális capillarisokon keresztül is. Az érfalba jutott protein transzportja az adventitiában lévő vasa lymphatica rendszer útján történik az érfalból.
Az érlumenből az endothel sejteken az intimába plazmaáramlás történik. Elektrolytek, glucose, O2 jutnak az intimába, majd innen az érfalon keresztül a médiába és részben az adventitiába is. Egyidejűleg az adventitiában lévő ércapillarisokon keresztül az artériás száron vér filtráció és a vénás száron reabsorptio folyik. Az intima és a média belső rétegének O2 és glucose ellátását főleg az érlumen felőli plazmaáramlás, míg a média középső és külső rétegének, továbbá az adventitiális szövetek ellátását döntően a capillaris vérfiltráció biztosítja. A nem fehérje molekulák (micromolekulák, elektrolytek) nagyobb részben az adventitialis capillaris resorptio útján, kisebb részben az intima rétegén, hosszanti plazmaáramlás révén az endothel sejteken keresztül az érlumenbe jutva kerülnek elszállításra az érfalból. A proteinek, lipoproteinek, macromolekulák kizárólag a nyirokutak - vasa lymphatica - közvetítésével szállítódnak el. Az érfal struktúrájának funkciója, épsége a szöveti vérellátás és elszállítás egyensúlyától függ.
Az ér endothel rétegének sérülése, károsodása (a legtöbb verőérbetegség kezdete) az érfali fehérjetranszport károsodásához vezet. Az érlumen felől kórosan megnő a plazma (folyadék) és fehérjefiitráció. Az érfalba jutó nagy tömegű protein, lipoprotein teljes elszállítását a vasa lymphatica rendszer nem tudja elvégezni, bekövetkezik az érfali nyirokkeringés dinamikus elégtelensége (high lymph output failure). Az eredmény protein, lipoprotein akkumuláció az érfalban: következménye fibrosis, érkárosodás kialakulása (2. ábra).
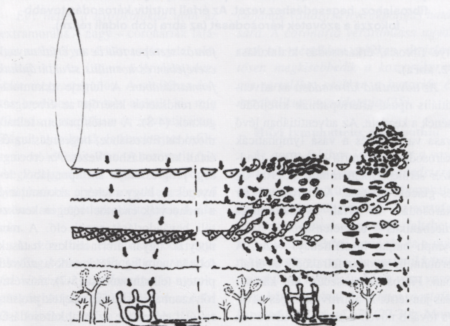
2. ábra.
Az érfali nyirokkeringés dinamikus elégtelensége az endothel sérülés hatására. Az endothel réteg károsodása folytán az endothel sejtek permeabilitása kórosan megnő, nagy mennyiségű protein, lipoprotein jut az érfalba (az ábra középső' része). A nagy tömegű proteinmolekulák elszállítására az adventitiális nyirokrendszer képtelen lesz, az érfali nyirokkeringés dinamikus elégtelensége alakul ki. A protein, lipoprotein megreked az érfalban, szöveti károsodás alakul ki, és fibrosis, hegesedés jön létre. A sérült intima felületén thrombocyták rakódnak le és fali thrombus alakulhat ki (az ábra jobb felén).
Az adventitia károsodása az adventitiális típusú arteriopathiák kifejlődésének a kezdete. Az adventitiában lévő vasa vasorum és a vasa lymphaticák károsodnak. A nutritív capillaris-rendszer sérülése miatt romlik az érfal O2 és glucose ellátása. A nyirokrendszer károsodása az érfali nyirokkeringés mechanikus elégtelenségére (low lymph output insuffitiency) vezet. A protein, lipoprotein felrakódik az érfalban. Fibrosis, hegesedés, fali károsodás jön létre. A nutritív keringés zavara tovább növeli a média és adventitia szöveteinek károsodását (3. ábra).
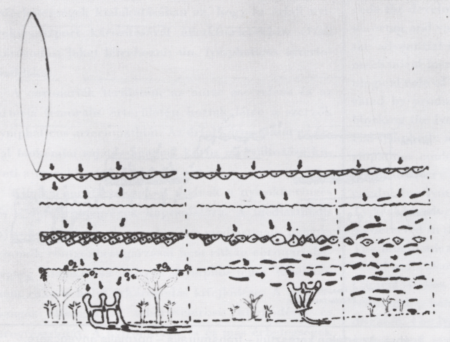
3. ábra.
Az érfali nyirokkeringés dinamikus elégtelensége az adventitiális vasa lymphatica rendszer sérülésének hatására. Az adventitiális vasa vasorum és vasa lymphatica károsodása az adventitiális típusú arteriopathiák kezdete. Romlik az érfal nutritív keringése, a nyiroktranszport mechanikus elégtelensége alakul ki. Protein, lipoprotein akkumuláció jön létre az érfalban (az ábra középső része). A protein akkumuláció fibrosishoz, hegesedéshez vezet. Az érfali nutritív károsodás tovább fokozza a szövetek károsodását (az ábra jobb oldali része).
A transmurális plazmaáramlás és az érfali fehérjetranszport teóriája hűen szemlélteti az érfali anyagcsere sajátosságait és termékenynek bizonyult az érbetegségek patomechanizmusának tanulmányozásában (1-3). Az érfali fehérjetranszport révén a nyirokkeringés fontos szerepet tölt be az érfal anyagcseréjében és normális struktúrájának fenntartásában. A fehérje akkumuláció rendszeres kísérője az érbetegségeknek (4-8). A tartós protein felhalmozódás fibrosishoz, hegesedéshez és érfali károsodáshoz vezet. Az érbetegség progressziója szempontjából lényeges az, hogy a fehérje akkumuláció a monocyták endothel rétegen keresztüli bevándorlását segíti elő. A monocyták ugyan fibrinolitikus hatásuk folytán némileg csökkentik a szöveti protein felhalmozódást (5-7), másrészről azonban a simaizomsejtek proliferatióját elősegítve az érfal károsodását siettetik. A monocyta bevándorlás növeli a low density lipoproteinek érfalba való jutását és ezáltal az atherosclerosis kialakulását és progresszióját fokozza. Figyelemre méltó az, hogy a vénafal nyirok transzportja kedvezőbb, mint az artériafalé. A vénák fala vékonyabb, ugyanakkor a vasa lymphatica rendszere a vénákban fejlettebb (9). Elképzelhető az, hogy a vénafal jobb nyiroktranszportja a magyarázata annak, hogy miért kisebb az érfali károsodás vénás betegségekben, mint az artériafali arteriopathiákban. Kiemelendő még az is, hogy a nyiroktranszport elégtelensége miatt romlik az érfal anyagcseréje, ezért kórosan megváltozik annak biomechanikai tulajdonsága és károsodik az érfal struktúrája.
Az artériafal nyirokkeringésének elégtelensége és a verőér betegségek közötti kapcsolat
Az artériafal nyiroktranszport insufficientiában az érfal károsodása jön létre. A szerzők egy kisebb csoportja csak érfali ödémát (interstitialis és intercellularis ödémát) és az adventitiában fehérje lerakódást észlelt művi nyirokpangás hatására (10, 11). Gondosan végzett érfal körüli nyirokér lekötés, illetve regionális nyirokblokád hatására azonban az artériafal súlyos, rendszerint az érfal mindhárom rétegére kiterjedő károsodása figyelhető meg (8, 12-16). A nyirokkeringés és a verőérbetegségek közötti összefüggésre utal az a megfigyelés is, hogy a verőérbetegség kialakulása során a regionális nyirokerek falában is kóros elváltozás figyelhető meg (10, 17).
Művi lympaticus arteriopathia
Az érfali nyirokkeringés és az érbetegségek kialakulása közötti kapcsolatok feltárásában nagy segítséget nyújtott a művi lympaticus anteriopathiák tanulmányozása.
Az artériafal nyiroktranszport elégtelenségének létrehozására kétféle kísérleti modell szolgál:
- Az érfali nyirokkeringés insufficientiájának létrehozása az elvezető fő nyiroktörzs - ductus thoracicus - lekötésével. Ez a módszer az adventitiális típusú arteriopathiák egyik modelljének is tekinthető. A módszer előnye: könnyen kivihető (kis állatokban is); hátránya: a nyirok elfolyásának súlyos akadálya általános, szekunder anyagcserekárosodást is okozhat. A létrejövő artériafali elváltozások rendszerint nem súlyosak és főleg az adventitiában észlelhetők (6).
- Az érfali nyiroktranszport blokádja a vasa lymphatica rendszer károsításával. Többnyire az artériákat kísérő nyirokfonat, nyirokutak vagy regionális nyirokcsomók lekötésével hozható létre az érfali nyirokkeringés blokádja. Az érfali károsodás rendszerint súlyos és az érfal valamennyi rétegére kiterjed, az adventitiában a nyirokpangás jelei jól kimutathatóak. Az endotheliális típusú arteriopathiák egyik modelljének tekinthető; az endothel előzetes sértése, ami fokozza az érkárosodást.
Kísérletes lymphaticus coronariopathia
A koszorúerek területén nyirokblokád hatására érfali károsodás, intima párnaképződés és ezt követően a lumen szűkülete jön létre. Bradham és munkatársai (18) csak kisfokú és átmeneti károsodást észleltek a coronáriák falában nyirokpangás hatására, azonban az utánvizsgálatok azt igazolták, hogy a művi szív-nyirokpangás után a coronáriák típusos megbetegedése: lymphatieus coronariopathia jön létre. A szív nyirokkeringésének regionális blokádja után már 24 órával megfigyelhető proteinfelhalmozódás a coronariafalban; jellemző a plazma beivódás, az intima duzzanata (párnaképződés), interstitialis és intracellularis ödéma (19, 20). A szív-nyirokpangást követően jellemző a kis coronariaerek megbetegedése a nagyobb koszorúerek mellett (21-23) és arteriovenosus mikroshun- tök képződése (14).
Ez az adat összhangban áll a cholesterin etetéses művi coronaria atherosclerosisos kísérletek eredményeivel; a nagyobb coronariák érfalának atherosclerosisos elváltozásai mellett a kis erekben (arteriolák) is hasonló elváltozások jöttek létre (21).
Egy héttel a nyirokblokád után az extramurális - nagy - coronariák falában már súlyos érkárosodás jelei alakultak ki. Az intima ödémásán duzzadt, megvastagodott. A médiában foltos hyalinos necrosis alakult ki, míg fibrosis a médiában és adventitiában. Tágult nyirokutak és kereksejtes infiltratio az adventitiában. A coronaria fala megvastagodott, a lumen szűkebb. A lymphatieus coronariopathia jellemző szövettani képét szemléltetjük a 4. ábrán.
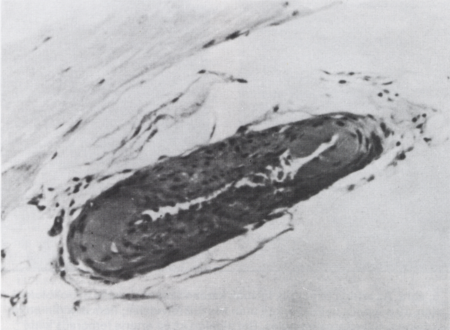
4. ábra.
A coronariafal károsodása szív-nyirokpangás hatására. 14 nappal a regionális szív-nyirokcsomók és az elvezető nyiroktörzsek lekötése után készült fénymikroszkópos felvétel; Mallory phosphatung acid-hematoxyllin festés, 400-szoros nagyítás. A coronaria fala megvastagodott, lumene erősen szűkült. A médiában foltos hyalinos necrosisok láthatók. Sejtes beszűrődés, ödéma az érfalban. Fibrosis jelei a médiában és az adventitában.
A szövettani elváltozásokkal egyidejűleg kórosan változik a coronariafal biokémiai tulajdonsága is nyirokpangás hatására (21). Csökken az érfal O2 felvétele, nő a CO2 leadása; a glycogen lebontás anaerob irányba tolódik el. Nő az érfal tejsav, sialsav és kollagéntartalma. Jellegzetes az érfalban a hexosamin (proteoglycan) felszaporodás is. Az érkárosodás nagyrészt maradandó; pár hónappal a szívnyirokblokád után is kimutatható (24). Sajátos még a koszorúkeringés regulációjának változása nyirokpangás hatására. A coronaria véráramlása ugyan csak kis mértékben csökken, de jelentősen megkisebbedik a koszorúkeringés tartaléka, csökken a hypoxiás és metabolikus vasodilatatio (25).
Művi lymphatieus aortopathia
Az aorta falában igen fejlett a vasa vasorum és vasa lymphatica rendszere, és az aortafal körül kiterjedt lymphatieus érfonat található (26). Az aortafal károsodás genezisében ezért feltehető volt a nutritív érfali keringés és a nyirokkeringés szerepe. Az aortafal körüli nyirokfonat lekötésével és a vasa vasorum károsításával kísérletes aortafal károsodás idézhető elő (27-30). Munkacsoportunk részletesen tanulmányozta a nyirokkeringés hatását az aorta ascendens falának szövettanára és struktúrájára. 24 kutyában hoztunk létre nyirokpangást az aortafal körüli (pa- raaorticus) nyirokcsomók lekötésével. Súlyos fali károsodást észleltünk az aorta falában. A médiában a simaizomsejtek foltos necrosisa jött létre interstitiális és intracelllularis ödéma kíséretében. Az adventitia ödémásán kiszélesedett, tágult nyirokutak, nyirokpangás jelei és kereksejtes beszűrődés is kimutatható volt az adventitiában (15, 31, 32). A vérnyomás emelésére (az aorta descendens falának szűkítésére) az aortafal aneurysmaszerű dilatatiója is kialakult.
Művi perifériás - artéria femoralis - lymphaticus arteriopathia
Az artériás érbetegségek leggyakoribb helye az alsó végtagi - perifériás - árterület. Kutyában az alsó végtagon létrehozott krónikus lymphödémában az artériák és vénák falában fali károsodás jön létre (10, 12). Tartós végtagi nyirokpangás hatására - a medencei nyirokcsomók és elvezető nyiroktörzsek lekötésére - a nagyobb artériák és vénák falában észlelt fali károsodásokon felül a kiserek (arteriolák) falában is kóros szövettani elváltozások jöttek létre és arteriovenosus shuntkeringés kifejlődése is kimutatható volt (33). Munkacsoportunk az artéria femoralis falában a nyiroktranszport blokádját hozta létre 36 kutyában a periadventitialis nyirokutak lekötésével (16, 34). A nyirokblokádot követő 2-3 nap múlva már a fali károsodás korai jelei (intima kiszélesedése, interstitiális ödéma az intimában, tágult nyirokutak, kereksejtes beszűrődés, fibrin lerakódás) kimutathatók voltak. Egy hét után már a médiában a simaizom sejtek foltos necrosisa és az érfalban fibrosis jelei észlelhetők. Jellemző az érfal kötőszöveti állományának károsodása nyirokpangás hatására: amorf, vacuolizált anyag (glycosaminoglycan) felhalmozódása a kötőszöveti rostok között. Az 5. ábrán az artéria femoralis szövettani elváltozásait szemléltetjük nyirokpangás hatására.
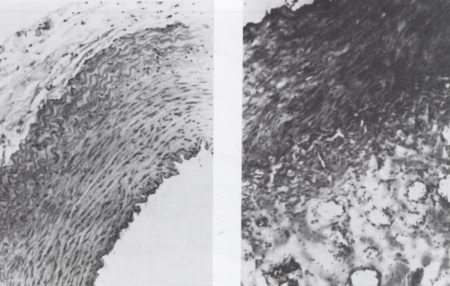
5. ábra.
Az artéria femoralis falának károsodása regionális nyirokblokád után. 10 nappal a nyirokblokád után készült felvételek; hematoxylin-eosinfestés, 400-szoros nagyítás. Bal oldalon az ép artéria femoralis képe látható (ezen a végtagon csak álműtét történt). Normális szövettani kép, az intima, a média és adventitia ép. Jobb oldalon az artéria falában súlyos károsodás fedezhető fel a nyirokpangás hatására. Az intima és a subendotheliális réteg ödémás. A médiában interstitiális és intercelluláris ödéma látható a simaizom-réteg károsodásával. Az adventitia ödémásán kiszélesedett, monocyta-sejtes beszűrődés, tágult nyirokerek is felismerhetők.
Az érfalkárosodás szövettani jeleit kóros biokémiai változások kifejlődése kísérte. Csökkent az artéria falának O2 felvétele, nőtt a CO2 leadása. Megnőtt az érfal tejsav, sialsav, kollagén és hexosamin tartalma (a lymphaticus coronariopathiás biokémiai változásokhoz hasonlóan). A nyirokpangás hatására az artéria femoralis falának biomechanikai tulajdonságai is kórosan változtak: az érfal vastagsága nőtt, elasticitása szignifikánsan csökkent (35, 36).
Az érfali nyirokkeringési elégtelenség és az artériás betegségek klinikai vonatkozásai
A nyirokpangás és a coronariasclerosis közötti kapcsolatra utalnak azok a klinikai megfigyelések, hogy a mediastinális nyirokcsomók megbetegedéseiben (lymphogranulomatosis, lymphoma malignum) és a mediastinális nyirokcsomók besugárzása után gyakran coronariabetegség kifejlődése észlelhető (37-39). Érdekes jelenség az, hogy az intramurális koszorúerekben rendkívül ritka a coronaria falának megbetegedése; elképzelhető az, hogy e jelenség egyik oka az lehet, hogy ezen a szívterületen a nyirokhálózat igen bőséges, azaz az érfali nyiroktranszport kedvező (40). Figyelemre méltó az a sectios adat is, miszerint súlyos coronasclerosis eseteiben 80- 90%-ban localis lymphostasis vagy nyirokér gyulladás található (41). Az aorta aneurysmák a multicausalis érbetegségek közé tartoznak. Bár a média elasticus rostjainak - veleszületett - károsodása és a fokozott elastase aktivitás a legfontosabb tényező az aneurysmák (Marfan-kór, Erdheim-kór) kialakulásában, mégis egyéb tényezők szerepe sem hanyagolható el. Az adventitialis nutritív keringésnek (vasa vasorum) és a nyiroktranszportnak (vasa lymphatica) igen fontos szerepe van az aortafal anyagcseréjében és táplálásában. Aortafal körüli gyulladás (periaortitis) gyakran előzi meg az aneurysma keletkezését és progresszióját (42-44). Az adventitia körüli gyulladás a periadventitialis nyirokfonat károsodásához, a nyirokút elzáródásához vezet, melynek következménye az érfali nyiroktranszport elégtelensége és az aortafal károsodása.
A perifériás atherosclerosis obliteratív verőérbetegség a leggyakoribb ilyen jellegű betegség. A nyirokkeringésnek az atherogenesis kifejlődésében fontos szerepe lehet. Kiemelendő az, hogy generalizált nyirokérbetegség és regionális nyirokcsomóduzzanat nem ritkán található obliteratív perifériás verőérbetegségben (45).
Az artériás betegségek többségében az érfali károsodás atherosclerosis talaján fejlődik ki. Az atherosclerosisos érkárosodás létrejöttében az érfali nyiroktranszport dinamikus elégtelenségének szerepe van. Említésre érdemes az, hogy nyirokút-, nyirokcsomóbetegséget okozó egyes lymphogen vírusok adásával kísérletesen lymphopathia és arteriopathia idézhető elő (46-48). Még kézenfekvőbb a nyirokkeringés szerepe az atherosclerosis progressziójában. Kísérletes és humán patológiai vizsgálatok azt tanúsítják, hogy az atherosclerosisos érfolyamatok progresszióját (vagy regresszióját) befolyásolja az érfali nyirokkeringés - vasa lymphatica rendszer - funkciója (1, 2, 4).
A diabeteszes arteriopathia gyakori érbetegség. Kifejlődésében a diabeteszes érfali anyagcserezavarnak kiemelkedő szerepe van, azonban a diabeteszes angiopathiák patogenezisében még számos faktor is szerepet játszik. Diabeteszes angiopathiában végzett vizsgálatok azt igazolják, hogy a betegség során az érfali nyirokrendszer károsodik és a nyiroktranszport zavarának nagysága befolyásolja a diabeteszes arteriopathia további alakulását (50).
Következtetések:
- Az érfali nyiroktranszport fontos szerepet tölt be az arteriafal anyagcseréjében és normális funkciója fenntartásában.
- Az artériafal nyirokdrenázsának elégtelensége a verőérbetegségek kialakulásában és progressziójában fontos szerepet játszik.
- Az érfali nyirokrendszer és az artériabetegségek közötti összefüggés még kevéssé feltárt, további jól tervezett kísérletes és klinikai vizsgálatokat igényel tanulmányozása.
- Viszonylag több adattal rendelkezünk a nyirokkeringés szerepéről a koszorúérbetegség, perifériás obliteratív verőérbetegség és az aorta aneurysmák patogenezisét illetően.
- A leggyakoribb artéria betegségtípus, az atherosclerosis kialakulásában és progressziójában az érfali nyirokkeringés részvétele biztosnak tekinthető.
Irodalom
- Doer, W.: Perfusionstheorie der Arteriosklerose. Abhandl. Norm. Pathol. Anat., 13: 1-10 (1963)
- Lemole, G. M.: The role of lymphostasis in atherosclerosis. Ann. Thorac. Surg. 31.: 290-2 (1981)
- Jellinek, IH.: Detre, Z, Veress, B.: Transmural plasmaílow in atherogenesis. Akadémia Kiadó, Budapest, 1983. 20-22.
- Smith, E. B.: Transport interactions and retention of plasma protein of the intima. Europ. Heart. J., 11: 72-81 (1990)
- Földi, M.: Physiology and pathology of the lyinph flow. In: Lymphedema. edit. Clodi-us, L., Thieme, G" Suttgart, 1977. 1-12.
- Schneider, F., Jellinek, H.: Ductus thoracicus ligaturát követő elváltozások patkány aortában. Morph. Ig. Orv. Szemle, 25: 3-9 (1985)
- Gevrity, R. G., Nailo, H. K., Richardson, M., Schwartz, C. J.: Dietary induced atherosclerosis in swine. Am. J. Physiol. 95: 775-92 (1979)
- Jellinek, H., Veress, B., Bálint, A., Nagy, Z: Lymph vessels of rat aorta and their changes in experimentál atherosclerosis. An electron microscopic study. Exp. Mol. Pathol., 13: 370-75 (1970)
- Johnson, R. A.: Lymphatics of blood vessels. Lymphology, 2: 45-56 (1969)
- Altorfer, J., Clodius, L.: Pathologische Veranderung bei experimentell chronischer Lymphostase. In: Basic Lymphology. edit. Földi, M. Schattauer, F. K., Suttgart, 1976. 51-62.
- Cremer, H., Müller, N.: Histological findings in the aorta of rats after experimentál ligature of the thoracic duct. Fólia An- giologica, 21: 270-3 (1973)
- Huth, F.: Morphologische Veránderungen und verschiedener Organe. Fólia Angiologica, 21: 253-61 (1973)
- Jellinek, II., Füzesi, Sz., Hársing, J., Solti, F., Gloviczky, P., Zelmanovics, L.: Aorta elváltozások ultrastruktúrája az érfal transzport zavarát követően. Morph. Ig. Orv. Szemle, 21: 258-65 (1981)
- 1Solti, F., Ungváry, Gy., Gloviczky, P., Sebestyén, M., Tátrai, E., Töreky, G.: The effect of cardiac lymphostasis on the microcirculation of the heart. Lymphology, 14: 122-26 (1981)
- Gloviczky, P., Solti, F., Szlávy, L., Soltész, L., Jellinek, H., Zelmanovics, L.: Aortic wall destruction caused by local lymphstasis. In: Advances in Lymphology. Edits. Bartos, V., Davidson, J. W. Avicenum, Prague, 1982. 236-41.
- Solti, F., Jellinek, II., Schneider, F., Lengyel, I, Bérezi, V., Kékesi, V.: Lymphatic arteriopathy; damage to the wall of the canine femoral artery after lymphatic blockade. Lymphology, 24: 55-9 (1991)
- Zsdanev, D. O.: On senile changes in lymphatic capillaries and vessels. J. Cardiovasc. Surg., 7: 108-16 (1966)
- Bradham, R. R., Parker, E. F" Greene, W. B., Hennigar, G. R.: Effects of cardiac lymphatic obstruction on coronary arteri- es. J. Thorac. Cardiov. Surg., 69: 876-91 (1975)
- Jellinek, II., Gábor, Gy., Solti, F" Veress, B.: The problem of the coronary changes due to disturbance of vascular wall per- meability. Angiology, 18: 179-89 (1967)
- Nagy, Z, Jellinek, II., Veress, B., Kóczé, A., Bálint A., Solti, F.: Effect of experimentál lymph congestion on coronary artery permeability in the dog. Acta Morp- hol. Acad. Sci. Hung., 17: 167-70 (1969)
- Kuo, L., Davis, M. J, Cannon, M. S., Chilian, W. M.: Pathophysiological consequences of atherosclerosis extend into the coronary microcirculation. Circulat. Res., 70: 465-76 (1992)
- Ratcliffe, H. L, Redfeld, E.: Atherosclerotic stenosis of the extramurai and intramural coronary arteries of man. Virchows Arch. Abt., 357: 1-10 (1972)
- Parl, F., Gottstein, W. H., Glasser, M.: Relationship of small and large coronary disease to myocardial ischemia. Arch. Path. Labor. Med., 104: 70-4 (1980)
- Solti, F., Lengyel E., Jellinek, H., Schneider, F., Juhász-Nagy, S., Kékesi, V.: Coronary arteriopathy after lymphatic blockade: an experimentál study in dogs. Lymphology: 27: 173-80 (1994)
- Solti, F" Kékesi, V., Juhász-Nagy, S.: Effect of acute cardiac lymph stasis on metabolic coronary adaptation in the dog. Lymphology, 18: 136-42(1985)
- Lee, F. C.: On the lymphatic vessels in the wall of the thoracic aorta of cat. Anat. Rec., 23: 343-9 (1922)
- Shionaioya, S., Griss, P.: Zur Pathogenese der Takayasu-Krankheit. Arthus phanomen an den Vasa Vasorum. Virchows Arch. Abt., 348: 269-80 (1969)
- Zellweger, J. P., Chapuis, G., Mirkovitch, V.: Consequences morphologiques de l'emballage de l'aorte du chien dans une membrane du caotchouc silicone. Virchows Arch. Abt. 350: 22-35 (1970)
- Nakata, Y., Shionaya, S.: Structure of the periaortic tissues and vascular lesions caused by disturbance of the lymphatics. Lymphology, 12: 18-9 (1979)
- Stefanadis, Chr. I., Stratos, C. G" Vlachopoulos, V., Dontas, I. A., Toutouzas, P. K.: Mediái necrosis and acute alterations in aortic distensibility following removal of the vasa vasorum of canine ascending aorta. Cardiovasc. Res., 27: 951-6 (1993)
- Jellinek, H., Füzesi, Sz-, Solti, F" Gloviczky, P., Zelmanovics, L: Ultrastructural study of canine aortic damage caused by disturbance of transmural transport. Exper. Mol. Pathol., 44: 67-75 (1986)
- Schneider, F.: Az adventicia szerepe az aortafal nemspecifikus válaszreakciójának kialakításában. Kandidátusi Értekezés, Budapest, 1984.
- Solti, F" Ungváry, Gy" Bálint A., Nagy, Z.. The regulation of the limb circulation in lymph-oedema (Development of arteriovenous shunt circulation in experimental lymphoedema of the leg. ) Angi- ologica, 8: 117-27 (1971)
- Solti, F., Jellinek, 11., Lengyel, E.: Lymphostase und Arteriopathie. Vasomed, 9: 502-5 (1993)
- Bérezi, V., Solti, F., Schneider, F., Monos, E.: Decreased vascular contraction and elastic stiffening after intramura] lymphostasis. Am. J. Physiol., 255: 1289-94 (1988)
- Nádasy, G. L, Solti, F., Monos, E" Schne ider, F., Bérezi, V., Kovách, A. G. B.: Effect of two week lymphatic occlusion on the mechanical properties of dog femoral arteries. Atherosclerosis, 78: 251-60 (1989)
- Engeset, A.: Irradiation of lymph nodes and vessels. Acta Radiol. (Stockholm), 56:: 970-6 (1964)
- Amromin, G. D.: Gildenhortn, R. D., Solomon, R. D.: The synergism of X irradiation and cholesterol fat feeding on the development of coronary artery lesions. J. Atherosclerosis Res., 4: 325-31 (1964)
- Leong, S. A.: Forbes, 1. J., Ruzic, T.: Radiation related coronary artery disease in Hodgkin's disease. Austr. N. Z. J. Med., 9: 423-5 (1979)
- Miller, A. J., De Boer, A., Palmer, A.: The role of the lymphatic system in coronary atherosclerosis. Medical Hypotheses, 37: 31-6 (1992)
- Hausaman, E.: Die Koronarsklerose in hohen Alter, in ihrer Beziehung zur Koronarsklerose der Jugendlichen. Cardio- logia, 14: 225-36 (1949)
- Baskerville, P. A., Blakeney, C. G., Young, A. E., Browse, N. L.: The diagnosis and treatment of periaortic fibrosis. Br. J. Surg., 59: 609-14 (1972)
- Baskerville, P. A., Browse, N. L.: Periaortic fibrosis progression and regression. J. Cardiovasc. Surg., 28: 30-1 (1987)
- Cohle, S. IX, Lie, J. T.: Inflammatory aneurysms of the aorta, aortitis and coronary arteritis. Arch. Pathol. Lab. Medl., 112: 11121-5 (1987)
- Mader, E.: Die generalizierte lymphavasculáre Induration der Lymphknoten und Lymphgefasse. Verh. Dtsch. Ges. Path., 39: 209-12 (1955)
- Fabricant, C. G., Fabricant, J., Litrenta, M. M., Minick, C. R.: Virus induced atherosclerosis. J. Exp. Med., 148: 335-40 (1978)
- Minick, C. R., Fabricant, C. G., Fabricant, J., Litrenta, M. M.: Atherosclerosis induced by infection with herpes virus. Am. J. Pathol., 96: 673-80 (1979)
- Paterson, J. C.: Cottral, G. E.: Experimentál coronary-sclerosis in chickens. Arch. Pathol., 49: 699-709 (1952)
- Holman, R. L, Mc Gill, H. C. Jr., Strong, J. P., Goer, J. C., Guidry, M. A.: The ar- terial wall as an organ. In: Hormones and atherosclerosis. edit. Pincus. G. Acade- mic Press, New York, 1959. 123-9.
- Kauftnann, A., Molnár, B., Craciun, C., Haus, H.: An optical and electron mic- roscopic study. Lymphology, 13: 202-6 (1980)
Dr. Solti Ferenc
SOTE Ér- és Szívsebészeti Klinika
1122 Budapest, Városmajor u. 68.
Érbetegségek: 1996/1. 8-14. oldal


