A praeeclampsia (PE) az egész anyai szervezetet érintő súlyos terhespathológiai kórkép, amelynek okát az intenzív kutatások ellenére sem ismerjük. Egyre több irodalmi adat támasztja alá azt a feltételezést, ami szerint a PE alapját az endothelsejt betegsége képezi, amelynek kórélettanában az endothelsejt diszfunkció feltehetően központi szerepet játszik. Megfigyelések szerint a PE-ás serum cytotoxieus hatása, csökkent aiitioxidáns aktivitása és/vagy a lipid peroxidok emelkedett serumszintje felelős lehet az endothelsejt-káro- sodásért. A következményes kifejezett vasoeonstrietio, a különböző mediátor rendszerek (thromboxan-prostaeyclin, endothelin - nitrogén-monoxid) közötti érzékeny egyensúly megbomlása, továbbá a vascularis per- meabilitas megváltozása, a véralvadási rendszer aktiválódása számos szervben - beleértve a foetoplacentaris egységet is - csökkent véráramláshoz és súlyos klinikai tünetek (hypertonia, proteinuria, thrombocytopenia, disseminalt intravasalis coagulatio, magzati retardatio slb.) kifejlődéséhez vezet. A PE-ra jellemző endothelsejt diszfunkció főbb okainak és következményeinek összefoglalását a kórkép gyakorlati jelentősége indokolja.
Érbetegségek: 1996/2. 7-12. oldal
KULCSSZAVAK
praeeclampsia, vascularis endothelium, endothelsejt diszfunkció
1. A vascularis endothelium, mint funkcionális egység
A vascularis endotheliumnak számos funkciója ismert. Egyrészt passzív barriert alkot az erek belső felszínén, másrészt az endothelsejtekben igen sok anyag képződik, amelyek szervezetünkben több élettani funkció szabályozásában vesznek részt. Ezen vegyületek közül kiemelt jelentőségű a prostacyclin (PGI2), amelynek lehetséges szerepét a terhesség indukálta magasvérnyomás betegség pathomechaniz- musában régóta vizsgálják. Az utóbbi években a tudományos érdeklődés középpontjába került a nitrogén-monoxid (NO), amely szintén az endotheliumból szabadul fel különböző agonisták, például acetylcholin, P-anyag, histamin, serotonin, vasopressin, bradykinin, adenin nucleotidok, oxytocin (1) stb. hatására, de agonista stimuláció nélkül is (2), és a PGl2-vel synergista hatást fejt ki a vasodilatatióban és a thrombocyta-aggregatio gátlásban (3). Az endothelsejtekben trhomboxan (TxA2), angiotensin II, vasopressin, pitvari natriuretikus peptid (ANP), P-anyag, kalcitonin-szerű peptid (CGRP) (4), továbbá különböző enzimek, például az angiotensin konvertáló enzim (ACE) - ninináz II-nek is nevezik -, amely az angiotensin I, angiotensin II átalakulásban betöltött szerepén kívül a bradykinin inaktivátoraként is működik, valamint a NO szintézisét végző nitrogén-monoxid-szintáz (NOS) en- dothelialis isoformája (5) is megtalálható. Az endothelsejtek közelebbről még nem azonosított endothelium de- pendens hyperpolarizáló faktort (EDHF) is termelnek (3). E molekula valószínűleg az arachidonsav egyik metabolitja: epoxid vagy lipoxid. Az endotheliumból felszabaduló vasoconstrictor hatású anyagokat endothelium eredetű contrahalo faktor (EDCF) gyűjtőnéven foglalják össze. Ide sorolják a TxA2-t, a superoxid aniont és az endothelint (6), amely a ma ismert leghatásosabb vasoconstrictor peptid (7). Aminosav szekvenciája alapján ez utóbbi molekulának emberben 3 formája különíthető el: az endothelin-1, az endothelin-2 és az endothelin-3 (8), amelyek szöveti elosztása eltérő (4). Az endothelin felfedezésével világossá vált egy endothelium médiait kontrollrendszer létezése az érrendszerben. Az endothelsejtek ugyanis a különböző kémiai és haemodinamikai hatásokra válaszolva endothelium dependens relaxalo és contrahalo faktorokat termelnek. Az endothelsejtek elősegítik egyes anyagok, például serotonin sejtbe jutását. Szabályozzák a neutrophil granulocyták adhesióját és migratióját, továbbá interleukin 1-et és egyéb immunkompetenciáért felelős molekulákat, ezenkívül thrombocyta eredetű növekedési faktort (PDGF) is termelnek (9). A haemostasis szabályozásában szerepet játszó anyagok közül kiemelendő, hogy az antithrombin III, a szöveti plasminogen aktivátor, a plasminogen aktivátor inhibitor és a von Willebrand-faktor is az endothelsejtekben képződik (9). Mindebből tehát látható, hogy az endothelium fizikai, mechanikai, valamint metabolikus barriert képezve biztosítja az egész érrendszer strukturális és funkcionális épségét.
2. Az endothelsejt-károsodás lehetséges mechanizmusai praeeclampsiában
A vascularis dezintegritás legismertebb formája az atherosclerosis, amely következményei és gyakorisága miatt a kutató és a gyógyító-megelőző munkában egyaránt központi helyet foglal el. Az endothelsejt-károsodás azonban más kórképek pathomechanizmusában is centrális szerepet játszik. Ilyenek például a PE, a haemolysissel, emelkedett májenzimekkel és alacsony thrombocytaszámmal jellemezhető syndroma (HELLP), a thromboticus thrombocytopenias purpura, továbbá a haemolyticus uraemias syndroma stb. Az sem kizárt, hogy a felsorolt betegségek nem önálló kórképek, hanem ugyanannak a betegségnek a részei (10). A PE-ben meglévő endothelsejt-károsodás okát számos munkacsoport tanulmányozta. Roberts és mtsai. in vitro kísérletben króm izotóppal jelölt humán umbilicalis vena endothelsejtek PE-ás anyai serummal történő inkubációja után az endothelsejtekből fokozott króm 51 (51Cr) felszabadulást észleltek (11), amely minden bizonnyal a sejtek elhalása miatt következett be. Mások PE-ás és normál terhesekből származó serum sejtkárosító hatásának összehasonlítása során arra az eredményre jutottak, hogy a betegek seruma in vitro kifejezett károsodást okoz endothelsejtekben, összehasonlítva egészséges terhességből származó serum hatásával (12). Chronicus1 és gestatios2 hypertoniában szenvedő nők esetében, akik a PE egyéb tüneteivel nem rendelkeztek, az endothelsejtkárosodást illetően nem volt szignifikáns eltérés a normál terhesek serumának hatására megfigyelt elváltozásoktól. Mindebből az a következtetés vonható le, hogy a PE-ás betegek seruma feltehetően olyan faktort vagy faktorokat tartalmaz, amely(ek) az endotheliumra nézve cytotoxicus(ak).
|
1Chronicus hypertonia: a 20. terhességi hét előtt kialakult vagy már a terhesség előtt fennálló hypertonia. |
A serum természetes antioxidáns tulajdonsága révén képes a fiziológiás Iipid peroxidáció biztosítására. A lipid peroxidok károsítják a sejtmembránt, így emelkedett szintjük a PE-ás anyai vérben összefüggésbe hozható az endothelsejt-károsodással (13, 14). Egészséges terhes asszonyokkal összehasonlítva PE-ás nők serumában a lipid peroxidok szintje a PE enyhébb eseteiben is emelkedett, a betegség súlyosabb formájában azonban kifejezett növekedését észlelték. Az antioxidans tulajdonságú E vitamin serum-szintje súlyos PE-ban szignifikánsan alacsonyabb volt egészséges terhesekhez képest. A lipid peroxid-E vitamin arány a PE különböző súlyosságú formáiban egyaránt emelkedett, a súlyos esetekben azonban kifejezettebb mértékben (13). Davidge és mtsai. PE-ás serum hatására szintén a lipid peroxidok felszaporodását észlelték agy homogeni- zátumon történő vizsgálataik során (15). A lipid peroxidok lehetséges aetiopathogenetikai szerepét erősíti az az érdekes megfigyelés, amely szerint diabetes mellitusban magasabb a lipid peroxidok plasmaszintje (16), és e betegség fokozott kockázatot jelent a PE kialakulása szempontjából (14).
Összefoglalva megállapítható, hogy a PE-ás serum feltehetően olyan cytotoxicus faktort tartalmaz, amely az endothelsejtek károsodását okozhatja. A betegségben megfigyelt lipid peroxid és antioxidáns egyensúly felborulása, a következményes fokozott lipid peroxidáció és az antioxidans aktivitás csökkenése az endothelsejt diszfunkció okaként fontos szerepet játszhat a PE pathofiziológiájában.

1. táblázat.
A praeeclampsia pathológiájában feltehetően szerepet játszó főbb endotheliális eredetű anyagok és hatásaik.
3. Az endothelsejt diszfunkció következményei
A. Vasoconstrictio
A PE pathogenesisében feltehetően alapvető szerepet játszó vascularis endothelium diszfunkció a vasodilatator hatású vegyületek csökkent termelődésében is megnyilvánul, ami a perifériás rezisztencia növekedéséhez vezet. Wang és mtsai. kimutatták, hogy a PGI2 serumszint enyhe és súlyos PE- ban egyaránt szignifikánsan alacsonyabb, mint egészséges terhesekben (13). Érdekes, hogy a foeto-placentomaternalis egység károsodott PGI2 termelése annak metabolitjai révén már a betegségre jellemző klinikai tünetek megnyilvánulása előtt kimutatható a vizeletben (17). A vizelettel ürített 6- keto-PGF1a (stabil prostacyclin metabolit) PE-ban csökkent (18) és a thromboxan B2 és e metabolit arányát PE-ás asszonyok vizeletében szignifikánsan emelkedettnek találták, összehasonlítva normotoniás terhesekkel (19). Ezeknek a megfigyeléseknek ellentmondani látszik, hogy PE-ás serum hatására a 6-keto-PGF1α termelődésének szignifikáns növekedését észlelték monolayer humán endothelsejt-tenyészetben végzett vizsgálatok során (20). Ez az eredmény azt mutatja, hogy a PE-ás nők seruma in vitro inkább fokozza a PGI2 produkciót, mintsem csökkenti. A jelenséget a betegek serumában feltételezett faktornak tulajdonítják, amely aktiválja az endothelsejteket. Ez az anyag nem feltétlenül azonos a már korábban említett cytotoxicus faktorral. Az in vivo megfigyelt elégtelen PGI2 termelődést valószínűleg a különböző mediator rendszerek közötti érzékeny egyensúly megbomlása eredményezi. Az irodalmi adatok azt mutatják, hogy a NO csökkent vascularis termelődése is feltehetően lényeges tényező a PE pathomechanizmusában (21, 22). A NO szintézis tartós gátlásával ugyanis terhes patkányokban a PE-ban is megfigyelhető tünetek (hypertonia, proteinuria, thrombocytopenia, magzati retardatio) idézhetők elő (21), valamint e betegségben szenvedő asszonyok umbilicalis endo- thelsejtjeiből csökkent NO felszabadulás tapasztalható (23).
A vasoconstrictor hatású anyagok közül PE-ban fokozott TxA2 szintézist észleltek (24); továbbá az érrendszer angiotensin II-vel, noradrenalinnal, valamint vasopressinnel szembeni megnövekedett érzékenységét figyelték meg (18, 25, 26). Több tanulmányban kimutatták, hogy az endothelin plasmaszintje PE-ban emelkedett (19, 27, 28). Ezen eredmények alapján feltételezhető, hogy e molekula fokozott szintézise valószínűleg szerepet játszik a PE pathomechanizmusában. Ezzel ellentétben Benigni és mtsai. az endothelin-1 plazmaszintjében nem találtak különbséget PE-ás és egészséges terhesek között (8). Ennek lehetséges oka e molekula felgyorsult degradációja PE-ban, amelyet in vitro kísérletben már korábban megfigyeltek (29). A fenti eredmények alátámasztják, hogy a megfeleld véráramlás fenntartásában igen fontos szerepet játszó vasoconst- rictor és vasorelaxans hatások (PGI2- TXA2, NO-endothelin) eltolódása a vasoconstrictor vegyületek fokozott szintézise és/vagy a vasodilatatióért felelős molekulák elégtelen termelődése révén a vasoconstrictio irányába hypertoniát és csökkent szöveti perfúziót eredményez. A praeeclampsia kórélettanában felthetően szerepet játszó főbb endotheliális eredetű vasoaktív anyagokat az 1. táblázat foglalja össze.
B. A véralvadási rendszer diszfunkciója
A PE-ban megfigyelt véralvadási rendszer aktiválódásának hátterében is felvetődött az endothelsejt-laesio lehetősége, A plasmában a fibrinopeptid A (a véralvadás specifikus markere) szintet egészséges kontroll csoporthoz viszonyítva PE-ás asszonyokban szignifikánsan magasabbnak (30), az antithrombin III szintet pedig alacsonyabbnak találták (31). Mindezek egyéb tényezők mellett szerepet játszhatnak a fokozott véralvadás és a PE-ban megfigyelt disseminalt intravasalis coagulatio (DIC) létrejöttében. A pathomechanizmus tisztázása azonban még további vizsgálatokat igényel. Taylor és mtsai. humán umbilicalis vena endothelsejt-kultúrán végzett vizsgálataik során érdekes eredményekre jutottak a PE-ás serum véralvadási rendszerre kifejtett hatására vonatkozóan (32). Kimutatták, hogy a PE-ás serum növeli a cellularis fibronectin felszabadulást, azonban sem a szöveti faktor (endogen procoagulans molekula) aktivitását, sem pedig a von Willebrand-faktor (VIII. véralvadási faktor fő komponense) expressióját nem fokozza. Az endotoxinnal történő összehasonlítás során kiderült, hogy az előbb leírtakkal ellentétben az endotoxin kifejezetten növeli a szöveti faktor aktivitását és a von Willebrand-faktor mennyiségét a kezelt szövetekben, ugyanakkor a cellularis fibronectin szintet csak minimális mértékben emeli (11). Ezen eredményekből arra következtethetünk, hogy a PE-ás serum nem generalizált, hanem szelektív hatással bír az endothelsejtek procoagulatios fehérje termelésére, és a betegek serumában feltételezett faktor valószínűleg nem azonos az endotoxinnal.
C. Megváltozott thrombocytafunctio
Monolayer humán sejt kultúrán végzett vizsgálatokkal kimutatták, hogy PE-ás asszonyokból származó serum az endothelsejtekben in vitro stimulálja a thrombocyta dependens növekedési faktor (PDGF) mRNS- ének és a fehérjének az expressióját (33). A klinikai tapasztalat szerint e betegséget a thrombocytaszám szignifikáns csökkenése jellemzi (30), amely valószínűleg a fokozott vérlemezke felhasználódás eredménye. Ezt az elképzelést támasztja alá a thrombocyta- aggregatio gátló vegyületek (PGI2, NO) csökkent termelődése és az endothelsejt-károsodás markereként számon tartott cellularis fibronectin emelkedett szintje a PE-ás anyai vérben. Ez utóbbi molekula egyben a thrombocyta-aggregatio mediatora is (32), plazmaszintjének emelkedése megelőzi a PE-ra jellemző tünetek kialakulását (34). A vérlemezke aktiváció és diszfunkció együttesen lehet felelős a következményes klinikai tünetekért.
D. Veselaesio
A hypertonia mellett a proteinuria a másik fő tünete a PE-nak. PE-ás betegek veséjéből származó biopsiás anyagban megfigyelt morfológiai változások, például glomerulus megnagyobbodás, capillaris endothelsejt-duzzanat (35), glomerularis endotheliosis a glomerulusok vascularis endothel-sejtjeiben intracellularis zárványokkal (36) alátámasztják azt az elképzelést, amely szerint a proteinuria lehetséges oka a renalis endothelsejtek károsodássa (37). Az immunhisztológiai vizsgálatok a vesében nem specifikus suben- dothelialis immunkomplex depositumokat mutattak ki (35), továbbá szoros összefüggést találtak a klinikai paraméterek és a veselaesiok között. A hypertonia és a proteinuria korrelált a glomerularis károsodás súlyosságával és a betegség progressiójával (35). Normál vesekéreg szövetben PE-ás serum hatására immunfluorescens festés segítségével az arteriolákhoz IgG típusú immunglobulin kötődést figyeltek meg azokban az esetekben, amelyekben a betegek vérében antivascularis- endothelsejt-antitestet találtak (38). Mindezek alapján feltételezhető, hogy a PE-ban megfigyelt nephropathiában a pathomorfológiai elváltozások alapja az endothelsejt-károsodás, következményes hypertoniával és proteinuriával.
E. Hyperlipidaemia és endothelsejt-károsodás
PE-ban a lipid metabolizmusban bekövetkező változás eredményeképpen hyperlipidaemia figyelhető meg (39). Endothelsejt kultúrán végzett vizsgálatok során azokban a sejtekben, amelyek a betegek serumával kerültek kapcsolatba, nagy számban sudanophil granulumokat találtak, amelyek triglyceridnek (TG) bizonyultak (39). A PE- ás asszonyokban megfigyelt magasabb serum TG szint (40) az endothelsejtekben in vitro fokozott TG akkumulációt indukál. Kimutatták továbbá, hogy a VLDL (very low density lipoprotein) PE-ás anyai erekben kifejezett endothelsejt-károsodást okoz (37). E betegségben tapasztalt emelkedett serum lipid koncentráció szerepe a PE-ás endothelsejt-laesio kórélettanában valószínűleg nem elhanyagolható. Az endothelsejt-károsodás lehetséges okait és következményeit az 1. ábra foglalja össze.
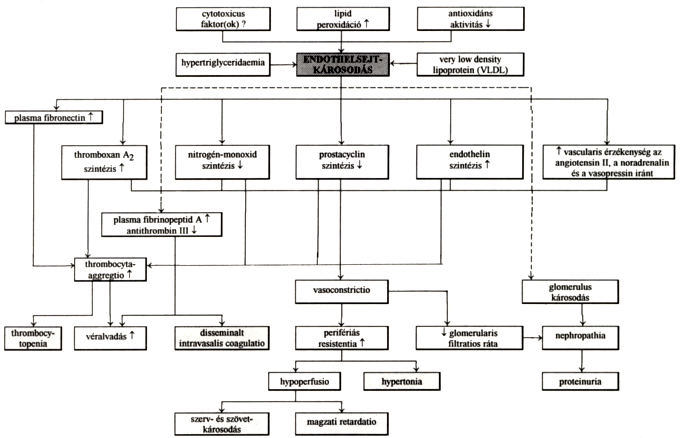
1. ábra.
Az endothelsejt-károsodás lehetséges okai és következményei.
Bár a PE pathomechanizmusában számos részjelenséget ismerünk, a betegség kórélettanában feltehetően központi szerepet játszó endothelsejt diszfunkció okának megismerése további vizsgálatokat és ismereteket kíván. A PE gyakorlati jelentősége - súlyos következményei miatt - nagy, ezért a betegség kórélettanának megismerése méltán tart számot napjainkban is a kutatás és a klinikum érdeklődésére.
Irodalom
- Furchgott, R. F" Vanhoutte, P. M.: Endothelium-derived relaxing and contracting factors. FASEB J. 3: 2007-2018 (1989)
- Schulz, R., Triggle, C. R.: Role of NO in vascularis smooth muscle and car- diac muscle function. TiPS 255-259 (1994)
- Vanhoutte, P. M., Shimokawa, H.: Endothelium-derived relaxing factor and coronary vasospasm. Circulation 80: 1-7 (1989)
- Farsang Cs.: Az endothelin legfontosabb humánbiológiai vonatkozásairól. Orvosképzés 68: 327-330 (1993)
- Förstermann, U., Nakane, M., Tracey, W. R., Pollock, J. S.: Isoforms of nit- ric oxidé synthase: functions in the cardiovascular system. Eur. Heart J. 14 (Suppl. I): 10-15 (1993)
- Vanhoutte, P. M.: Platelet-derived serotonin, the endothelium, and cardiovascular disease. J. Cardiovasc. Phar- macol. 17 (Suppl. 5): S6-S12 (1991)
- Yanagishawa, M., Kurihara, H., Kimura, S., et al.: A növel potent vaso- constrictor peptide produced by vascular endotheliel cells. Nature 332: 411-415 (1988)
- Benigni, A., Orisio, S., Gaspari, F. et al.: Evidence against a pathogenetic role for endothelin in preeclampsia. Br. J. Obstet. Gynecol. 99: 798-802 (1992)
- Káli A.: Vascular integritás és vascularis remodeling. Érbetegségek 2: 1-6 (1994)
- Sibai, B. M., Kustennann, L., Velasco, J.: Current understanding of severe preeclampsia, pregnancy-asso- ciated hemolytic uremic syndrome, thrombotic thrombocytopenic purpu- ra, hemolysis, elevated liver enzymes, and low platelet syndrome, and postpartum acute renal failure: diffent clinical syndromes or just diffe- rent names? Curr. Opin. Nephrol. Hypertens. 3: 436-455 (1994)
- Roberts, J. M" Edep, M. E., Goldfien, A., Taylor, R. N.: Sera from pre- eclamptic women specifically acti- vate humán umbilical vein endothe- lial cells in vitro: morphological and biochemical evidence. Am. J. Repród. Immunol. 27: 101-108 (1992)
- Tsukimori, K., Maeda, H., Shingu, M. et al: The possible role of endot- helial cells in hypertensiove disor- ders during pregnancy. Obstet. Gynecol. 80: 229-233 (1992)
- Wang, Y. P., Walsh, S. W" Guo, J. D., Zhang, J. Y.: The imbalance between thromboxane and prostacyclin in preeclampsia is associated with an imbalance between lipid preoxides and vitamin E in maternal blood. Am. J. Obstet. Gynecol. 165 (6 Ptl): 1695-1700 (1991)
- Hubel, C. A., Roberts, J. M" Taylor, R. N. et al: Lipid peroxidation in pregnancy: New perspectives on preclampsia. Am. J. Obstet. Gynecol. 161: 1028-1034 (1989)
- Davidge, S. T" Hubel, C. A., Brayden, R. D. et al.: Sera antioxidant activity in uncomplicated and preeclamptic pregnancies. Obstet. Gynecol. 79: 897-901 (1991)
- Nishigaki, I., Hagihara, M., Tsunekawa, H. et al.: Lipid peroxide levels of serum lipoprotein fractions of diabetic patients. Biochem. Med. 25: 373-378 (1981)
- Zahradnik, H. P., Schafer, W., Wetzka, B., Breckwoldt, M.: Hypertensive disorders in pregnancy. The role of eicosanoids. Eicosanoids 4: 123-136 (1991)
- Pedersen, E. B., Christensen, N. J., Christensen, P. et al.: Preeclampsia - a state of prostaglandin defici- ency? Urinary prostaglandin excretion, the renin-aldosterone system, and circulating catecholamines in preeclampsia.
- Kraayenbrink, A. A., Dekker, G. A., van Kamp, G. J., van Geijn, H. P.: Endothelial vasoactive mediators in preeclampsia. Am. J. Obstet. Gynecol. 169: 160-165 (1993)
- Branch, D. W., Dudley, D. J., LaMarche, S., Mitchel, M. D.: Sera from preeclamptic patients contain factor(s) that stimulate prostacyclin production by human endothelial cells. Prostaglandins Leukot. Essent. Fatty. Acids. 45: 191-195 (1992)
- Molnár M., Sütő S., Tóth T., Hertelendy, F.: Prolonged blockade of nitric oxidé synthesis in gravid rats produces sustained hypertension, proteinuria, thrombocytopenia and intrauterine growth retardation. Am. J. Obstet. Gynecol. 170: 1458-1466 (1994)
- Seligman, S. P., Buyon, J. P., Clancy, R. M. et al.: The role of nitric oxidé in the pathogenesis of preeclampsia. Am. J. Obstet. Gynecol. 171: 944- 948 (1994)
- Pinto, A. Sorrentio, R., Sorrentino, P.: Endothelial-derived relaxing factor released by endothelial cells of human umbilical vessels and its impairment in pregnancy-induced hypertension. Am. J. Obstet. Gynecol. 164: 507-513 (1991)
- Fitzgerald, D. J., Rocki, W., Murray, R. et al: Thromboxane A 2 synthesis in pregnancy-induced hypertension. Lancet 335: 751-754 (1990)
- Tulenko, T., Schneider, J., Floro, C., Sicilla, M.: The in vitro effect on arterial wall function of serum from patients with pregnancy-induced hypertension. Am. J. Obstet. Gynecol. 156: 817-823 (1987)
- Schrier, R. W., Briner, V. A.: Peripheral arterial vasodilation hypothesis of sodium and water retention in pregnancy: Implications for pathogenesis of preeclampsia-eclampsia. Obstet. Gynecol. 77: 632-639 (1991)
- Taylor, R. N., Varrna, M., Teng, N. N. H., Roberts, J. M.: Women with preeclampsia have higher plasma endothelin levels than women with normál pregnancies. J. Clin Endocri- nol. Metab. 71: 1675-1677 (1990)
- Nova, A., Sibai, B. M" Barton, J. R. et al: Maternal plasma levels of endothelin is increased in preclampsia. Am. J. Obstet. Gynecol. 165: 724- 727 (1991)
- Branch, D. W., Dudley, D. J" Mit chell, M. D.: Preliminary evidence for homeostatic mechanism regulating endothelin production in preeclampsia. Lancet 337: 943-945 (1991)
- Saleh, A. A., fíottoms, S. F., Farag, A. M. et al.: Markers for endothelhelial injury, clotting and platelet activation in preeclampsia. Arch. Obstet. Gynecol. 251: 105-110 (1992)
- Roberts, J. M., Taylor, R. N., Musci, T., et al.: Preeclampsia: An endothelial cell disorder. Am. J. Obstet. Gynecol. 161: 1200-1204 (1989)
- Taylor, R. N.t Casal, D. C., Jones, L. A., et al: Selective effects of preeclamptic sera on humán endothelial cell procoagulant protein expression. Am. J. Obstet. Gynecol. 165 (6Ptl): 1705-1710 (1991)
- Taylor, R. N., Musci, T. .J., Rodgers, G. M., Roberts, J. M.: Preeclamptic sera stimulate increased platelet-derived growth factor mRNA and protein expression by cultured humán endothelial cells. Am. J. Repród. Immunol. 25: 105-108 (1991)
- Taylor, R. N., Crombleholme, W. R., Freidman, S. A. et al.: High plasma cellular fibronectin levels correlate with biochemical and clinical features of preeclampsia but cannot be attributed to hypertension alone. Am. J. Obstet. Gynecol. 165: 895-901 (1991)
- Gartner, H. V.: Nephropathy in pregnancy- and endothelial lesion? Zentralbl. Gynakol. 116: 123-137 (1994)
- Florijn, K. W" Derkx, F. H. M., Visser, W. et al: Plasma immunoreactive endothelin-1 in pregnant women with and without preeclampsia. J. Cardiovasc. Pharmacol. 17(Suppl.7): S446-S448 (1991)
- Arbogast, B. W., Leeper, S. C., Merrick, R. D. et al: Which plasma factors bring about disturbance of endothelial function in pre-eclampsia? Lancet 343: 340-341 (1994)
- Rappaport, V. .J., Hirata, G., Yap, H. K., Jordan, S. C.: Anti-vascularis endothelial cell antibodies in severe preeclampsia. Am J. Obstet. Gynecol. 162: 138-146 (1990)
- Lorentzen, B., Endresen, M. J., Hovig, T. et al: Sera from preeclamptic women increase the content of triglycerides and reduce the release of prostacyclin in cultured endothelial cells. Thromb. Res. 63: 363-372 (1991)
- Potter, J. M., Nestel, P. J.: The hyperlipidemia of pregnancy in normál and complicated pregnancies. Am. J. Obstet. Gynecol. 130: 165- 170 (1979)
Visontai Zsuzsanna Zsófia
SOTE Klinikai Kísérleti
II. sz. Élettani Intézet
1082 Budapest, Üllői út 78/B
Érbetegségek: 1996/2. 7-12. oldal


