A tartós vénabiztosítás centrális vénás port-ok alkalmazásával az utóbbi évtizedekben, az onko ló - giában is elfogadott módszer, melyre az oki és tüneti kezelés fejlődésével egyre nagyobb szakmai igény mutatkozik. A szerzők az irodalomból ismert javallatok és ellenjavallatok, a korai és késői szövődmények bemutatása után saját tapasztalataikról számolnak be. Összesen 70 centrális vénás port-ot inplantáltak intervencós radiológiai módszerrel, csaknem kizárólag a vena subclaviába, Seldinger technikával. Leggyakoribb szövődményeik a lokális fertőzés, a beteg fogyása miatti port-okozta bőr-nekrózis voltak; trombózis az eszköz megfelelő gondozása mellett ritkán fordult elő. Hangsúlyozzák, hogy a szakmai igény jelentősen meg - haladja a finanszírozott eszközök mennyiségét, s célszerűnek tartják, hogy minden onkológiai központban teremtsék meg a szakmák közötti együttműködéssel a tartós vénabiztosítás lehetőségét a kezelés biztonsága és a betegek jobb életminősége érdekében.
Érbetegségek: 2015/1. - 3-9. oldal
KULCSSZAVAK
tartós véna port, eredmények,szövődmények
Bevezetés
A centrális vénák kanülálását korábban, elsősorban a sürgősségi ellátás, az intenzív terápia és a kardiológia területén alkalmazták. Az utóbbi időben, az onkológiában is egyre elterjedtebb a tartós vénabiztosításnak ez az alternatívája, melyet az Amerikai Egyesült Államok után Nyugat-Európában is már közel 30 éve alkalmaznak. Hazánkban a Sugárterápiás és Onkológiai Szakmai Kollégium, az Anaesthesiologiai és Intenzívterápiás, valamint a Sebészeti Szakmai Kollégiumok egyetértésével 2004-ben kiadott módszertani levele a szolid tumoros betegek 30-35 %-ánál tartotta szükségesnek a tartós vénás port behelyezést [31]. Az eltelt időben az adjuváns kezelések időtartamának megnyúlásával (pl. a szokásos fél éves kezelések helyett a trasztuzumabot egy éven át alkalmazzák), és több daganatban az alkalmazható kezelési vonalak száma, és ezzel a vénapunkciók igénye még tovább nőtt. Becslésünk szerint az infúziós daganatellenes kezelést kapó, vagy aktív szubsztitúcióban részesülő betegek akár felénél is indokolt lehet a tartós vénabiztosítás alkalmazása [7].
A szerzők célja, tartós centrális vénás portok onkológiában betöltött szerepének megismertetése, kiegészítve saját tapasztalatainkkal.
Az onkológiai betegeknek, az úgynevezett "szokásos" betegpopulációval szemben, több, sajátos jellemzője van. - A betegség kezdetén, a panaszok és tünetek okának felderítését célzó kivizsgálás során gyakran lehet szükség laborvizsgálatokra. A tumor-kutatás, valamint a betegség stádiumának meghatározása során végzett képalkotó vizsgálatok egy részénél (CT, MR, PET/CT, csont-szcintigráfia) intravénás kontrasztanyagot, intravénás izotópot alkalmaznak. Ugyanakkor a már megkezdett daganatellenes kezelés hatékonyságának megítélésére, meghatározott időközönként - általában 2-3 havonta - szintén szükség lehet vérvételre (tumor-marker meghatározások), valamint kontroll képalkotó vizsgálatokra, melyek során ugyancsak alkalmazhatnak intravénás kontrasztanyagot. A kezelés effektivitásának követésére, a diagnózis felállításához alkalmazott képalkotó vizsgálatot, célszerű a későbbiekben is elvégezni, azaz ha a kivizsgálás során CT vizsgálat történt, akkor a kontroll vizsgálatok során is CT-vel követjük a beteget (ugyanez igaz MR esetében is). A hatás lemérésére általánosan elfogadott RECIST (response evaluation criteria in solid tumours) jellegzetesen kontrasztanyaggal végzett axiális képalkotást ír elő [11, 21, 25, 34].
- Az onkológia rohamos fejlődésével a terápiás lehetőségek jelentősen bővültek. Több, egymást követő terápiás "vonalra" építhetünk, ezért a kezelés hónapokon, éveken át tarthat. Különösen igaz ez az emlő-, vastagbél-, petefészek-, prostata-daganatok és a melanoma malignum esetében [1, 3, 4, 8, 9, 13, 19, 20, 27, 29].
- Az alkalmazott citosztatikumok, biológiai válaszmódosító szerek, kevés kivétellel intravénás infúzió formájában használatosak.
A citosztatikumok nagy része károsítja a vénákat (pl. fluorouracil, antraciklinek), ennek következtében gyakori az ismétlődő, többé-kevésbé kifejezett, perifériás thrombophlebitis.
- Az aktív onkológiai kezelés, az onkológiai gondozás és a terminális állapot során egyaránt szükséges lehet a daganatos beteg szupportálása. Ennek során az antiemetikumok analgetikumok, antibiotikumok egy részét intravénásan is alkalmazzuk, valamint egyre gyakrabban történik részleges vagy teljes parenterális táplálás, mely szintén vénán keresztül történik. A pumpával végzett intravénás fájdalomcsillapítás teljes bio-hasznosulást és a PCA (patient controlled analgesia) bizonyos előre beállított határok között lehetővé teszi a fájdalom fokozódások (úgynevezett "áttörő fájdalmak") kivédését [14, 15, 22, 28].
- Mindezek mellett, figyelembe véve azt a tényt, hogy minden kezelés előtt és néhány kezelés után is indokolt a hemostátusz, valamint a klinikai-kémiai laborparaméterek ellenőrzése, ezeknél a betegeknél gyakran van szükség vénapunkcióra.
- A felsorolt okok miatt bekövetkezett mechanikai és kémiai károsítás következtében a kezdetben még kanülálható perifériás vénák egyre nehezebben szúrhatóak. A többszöri sikertelen vénapunkciós kísérlet kellemetlenségei miatt előfordulhat, hogy a beteg nem vállalja a további kezelést. Az is megtörténhet, hogy a nehezen kanülált, apró, felületes vénából kimozdul a kanül, vagy nem bírja az infúzió volumenét és megreped. Ekkor az alkalmazott citosztatikum az érpályán kívülre jut (paravasatio) és súlyos szöveti nekrózist is okozhat [24].
- Természetesen az is lehetséges, hogy a betegeknek valamilyen veleszületett vagy szerzett okból már a kezelés kezdetekor rossz a perifériás véna-státusza.
A felsorolt problémákra jelenthet megoldást a centrális vénába helyezett tartós vénás port alkalmazása. A gyakorlatban számos típusa létezik, de felépítése lényegében mindegyiknek ugyanaz. Minden vénaport egy vagy két tartályból és a hozzá csatlakozó szilikon vagy poliuretán kanülből áll. A tartály készülhet műanyagból, rozsdamentes acélból, vagy titániumból, és a tetejét egy önzáró szilikon membrán fedi. A kanült általában, percutan punctióval, közvetlenül a centrális vénába helyezik be, ritkábban ez sebészi feltárással történik. A percutan punctio lehet ultrahang vezérelt is, csökkentve ezáltal a beavatkozás idejét és az esetleges artéria-punkció veszélyét. Ez, az ultrahang vizsgálat terén némi jártasságot igényel [5, 6]. Lehetőség van a kanül perifériáról centrális pozícióba történő felvezetésére is. Ez a PICC-line rendszer, de ebben az esetben nincs tartály; a kanül vége egy szeleppel bíró baktériumszűrőben végződik, melyet a bőrfelületre rögzítünk. Ennél a rendszernél gyakrabban fordul elő trombózis, valamint nagyobb az infekció veszélye is, ezért az ilyen kanült legkésőbb 6 hónap elteltével el kell távolítani [23, 30].
A kanülált centrális vénák általában a vena jugularis interna és a vena subclavia [32, 35]. Azon az oldalon célszerű kanülálni, amelyiket nem érint az onkológiai betegség (pl. emlőrák, bőráttét, sugárkezelés utáni hegesedések, stb.). Ha bármely okból (pl. véna cava superior syndroma) az említett vénák nem használhatóak, de mindenképpen szükséges a port behelyezése, ritkán a vena femoralis kanülálására is sor kerülhet [10]. A vena axillaris és vena basilica rendszerén keresztül történő beültetés során speciális, kisebb méretű kamrával ellátott port használatos, és a port kamráját, ilyen esetben a felkar medialis oldalán, a subcutan zsírrétegben kialakított tasakban helyezzük el.
A port vérvétel, transzfúzió, kemoterápia, parenterális táplálás és supportív terápia, ill. a képalkotó vizsgálatok során kontrasztanyag beadására egyaránt használható. Speciális portot lehet még intraarterialisan, intrathecalisan, intraperitonealisan és intrapleuralisan is behelyezni. Mivel mind a tartály, mind a kanül röntgenárnyékot ad, ez a beültetéskor és a későbbiekben, bármely működészavar esetén segíti a kanül helyzetének ellenőrzését. Gyártótól függően, a rendszer 1.5-3T teljesítménytartományban MR-ben is használható, és megfelelő gondozás mellett, akár 25 évig is bent maradhat [5, 16].
1. ábra.
A vezetődrót helyre juttatása Seldinger-technikával.
Indikációk-kontraindikációk
A tartós vénaport behelyezésének speciális onkológiai indikációi a gyakorlatban a következők [26, 33]:
- A leggyakoribb indikáció, a perifériás vénáknak az onkoterápia miatt kialakult károsodása, mely lehetetlenné teszi azok további biztonságos punkcióját.
- A perifériás vénák alkati elégtelensége pl.: gracilis vénák, felső végtagi lymphoedema (általában axillaris block-dissekcio és a hónaljárok sugárkezelése után).
- Indokolt a behelyezés, ha intravénás készítményt szándékozunk adni a betegnek több fázisban vagy ciklusban, és legalább 3 hónapnál hosszabb időre tervezzük az onkológiai kezelést.
- Abban az esetben, ha gyakran van szükség kis lumenű vénát károsító gyógyszerek adására (pl. intravénás vaspótlás).
- Szupportív terápia kapcsán: ha a beteg tartós parenterális táplálásra, tartós intravénás antibiotikus kezelésre, gyakori transzfúzióra és fájdalomcsillapításra szorul - és a várható életkilátás a három hónapot meghaladja.
- Speciális hemato-onkológiai javallatok esetén (pl. őssejt- gyűjtés, plasmapheresis).
- Végül a perifériás vénabiztosítás bármely okból bekövetkezett lehetetlensége esetén.
A centrális vénás port behelyezésének leggyakoribb kontraindikációi a következőkben foglalhatók össze:
- Nem befolyásolható véralvadási zavar (a beavatkozás előtt INR és thrombocyta szám meghatározás minden esetben szükséges).
- Súlyos és nem korrigált neutropenia, neutropeniás szepszis, vagy vérképeltérés nélkül bekövetkezett szeptikus állapot.
- A punkció tervezett helyén, a bőrön vagy a bőr alatti kötőszövetben meglévő gyulladás, hegesedés vagy tumoros infiltráció.
- Vena cava superior syndroma (ha a beültetés elkerülhetetlen, speciális behatolási helyeket kell választani).
- Súlyos tüdőbetegség, következményes légzési elégtelenséggel, mely miatt a beteg nem tud hanyatt feküdni a beavatkozás alatt.
- Rendkívül fontos a beteg kooperációja a kanül behelyezése, viselése, gondozása során. Ezek hiányában nem javasolt a port beültetése.
- Végül - invazív beavatkozásról lévén szó - a hatályos jogi szabályozásnak megfelelően, az orvosi tájékoztatást követően a beteg (vagy helyette a döntésre felhatalmazott személy) írásos beleegyezésének hiánya is kontraindikálja a beavatkozást [36].

2. ábra.
A mellkasi subcutan zsírban, a portkamra befogadására alkalmas tasak kialakítása.
Szövődmények
Tekintettel arra, hogy invazív beavatkozásról van szó, nem hagyhatjuk figyelmen kívül a lehetséges szövődményeket, melyek a beavatkozás alatt vagy közvetlenül utána a korai, illetve később, a port rendszeres használata során alakulhatnak ki.
Korai szövődmények:
- Az egyik leggyakoribb korai szövődmény az aritmia, melyet a vezetődrót vagy a kanül túlvezetése, jobb pitvarba kerülése okoz. Ennek elkerülésére a kanülön hosszúság-jelölés található, további hasznos segítség, ha a beteg a beavatkozás során EKG monitorizálás alatt áll.
- Főleg a vena subclavia punkciója esetén előfordulhat a tüdő, illetve a pleura sérülése, következményes pneumovagy haemothorax, ezért a beavatkozás után 24 órával kontroll mellkasi röntgen vizsgálat kötelező.
- Ritkább szövődmények az artéria-punkció és véna perforációja. Mindkét esetet kísérheti vérzés. A vena subclavia kanülálása esetén a vérzés tamponálása nehézségekbe ütközhet, mivel az említett véna általában a clavicula alatt fut, ilyenkor sebészi (vagy ha a lehetőség adott, érsebészeti) beavatkozásra lehet szükség.
- Igen ritkán előfordulhat katéter-embolizáció is.
Késői szövődmények:
- Az egyik leggyakoribb késői szövődmény a sebfertőzés, mely tályogképződéshez is vezethet. Oka a port használata során az aszepszis előírásainak be nem tartása. Szisztémás antibiotikus kezeléssel, rendszeres sebgondozással az állapot, az esetek nagy részében kezelhető.
- Amennyiben a sebfertőzés kórokozói bejutnak a portba és ezen keresztül a centrális pozicióban lévő kanülbe, súlyos kanül-szepszis, szeptikus thrombophlebitis alakulhat ki. Ilyenkor a centrális vénás port eltávolítása, a kanül-végből kórokozó-tenyésztés és antibiogram, majd ennek megfelelő kezelés kötelező.
- Gyakori probléma, és szintén késői szövődményhez vezethet a hibás punkciós technika. Abban az esetben, ha nem szúrják megfelelő mélyre a tűt a szilikon membránba, vagyis azt nem szúrják át, ezért a port "nem működik". A másik lehetőség, ha túl felületesen szúrják be a tűt a szilikon membránba és így az adagolt intravénás készítmény a porton kívül, a szövetek közé jut. Citosztatikumok esetén ez súlyos szöveti necrosist is okozhat (hazai viszonyok között elképzelhető, hogy a membrán biztonságos punkcióhoz javasolt speciális tű helyett - annak magas ára vagy a beszerzés nehézsége miatt - egyéb tűt kénytelenek alkalmazni).
- Amennyiben bármely okból a beteg testsúlyának jelentős részét elveszíti, a mellkasi subcutan zsír mennyisége is annyira lecsökkenhet, hogy a port tartálya belülről dekubitálja a bőrt, ezáltal bőrelhalást okoz, mely fertőzésveszélyt jelent.
- A kanül működési zavara szintén késői szövődmény forrása lehet. Abban az esetben, ha a kanül gondozása nem megfelelően történt, az agresszív próbálkozások során a nagy nyomással történő átöblítési kísérletek növelik a port szétcsúszásának, esetleges trombus besodrásának az esélyét.
- Késői szövődményként megemlíthető a kanül trombózisa, mely embólia forrása lehet.
- A port-kamra elfordulása.
- Ritkán előfordulhat, hogy a kanül eltörik (pinch-off syndroma) [2].
A felsorolt késői szövődmények kialakulása odáig vezethet, hogy a port-ot el kell távolítani. Különösen igaz ez kanülsepsis, thrombosis vagy a kanül eltörése esetén [6, 12].

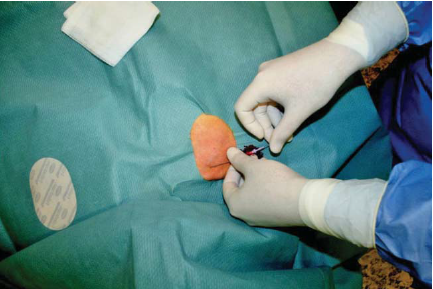
3. ábra.
A kanül bevezetése.
Saját tapasztalataink
A Békés Megyei Pándy Kálmán Kórházban működő Megyei Onkológiai Központ a megye egész területéről nagyszámú beteget lát el, ezért kórházunkban is időszerű volt az eljárás bevezetése. Ezt megelőzően intézetünkben éveken át senki nem érezte magát illetékesnek ebben a kérdésben, ezért azoknak a betegeinknek, akiknek erre az eszközre szükségük volt, a beültetésre Kecskemétre vagy Szegedre kellett utazniuk. Az említett centrumokon kívül az országban több helyen is végeznek tartós vénaport implantációt. Az eljárást végzők személye igen változatos: sebész, érsebész, szívsebész, radiológus, intervenciós radiológus, aneszteziológus szerepelhet a beavatkozást végzők listáján. Kórházunkban aneszteziológus szakorvos végzi a beavatkozást. Intézetünkben az első tartós vénaport behelyezést 2009-ben végeztük el. A port implantációk száma évről-évre nő, 2014. márciusig 70 port behelyezés történt.

4. ábra.
A kanül és a portkamra összeillesztésük után a helyükön.
Módszerünk
A beavatkozást előjegyzés alapján, a Radiológiai Osztály Angiográfiás Laboratóriumában (röntgen-műtőben) végezzük, ahol számunkra hetente egy napon biztosítanak lehetőséget. Ez azért említésre méltó, mert számos intézetben a port behelyezés állandó munkahelye mind a mai napig megoldatlan.
A beavatkozás az asepsis szigorú betartása mellett, lokál-anesztéziában, radiológiai intervenciós szakasszisztens közreműködésével történik. A betegek mintegy 30 perccel az eljárás megkezdése előtt per os anxiolitikumot kapnak. Intézetünkben percutan technikát alkalmazva, a vena subclavia kanülálását végezzük el. A vénát infraclavicularis pozícióból szúrjuk meg, majd Seldinger technikával kanüláljuk. A kanül helyes pozíciójának ellenőrzésére képerősítőt használunk. A véna kanülálása után a mellkason, a punkciós nyílástól kb. 2 cm-re, distálisan, 3-4 cm-es, haránt bőrmetszésből, a port tartályának befogadására alkalmas subcutan tasakot alakítunk ki. A kanült a bőr alatt, a punkció és a bőrmetszés közti szakaszon átvezetjük, majd a helyes pozíciót képerősítőn ismételten ellenőrizzük, ezt követően megfelelő hosszúságúra vágjuk és az implantált tartályhoz applikálju. A port-rendszer tartályát két felszívódó öltéssel rögzítjük. Miután meggyőződtünk arról, hogy a port megfelelően működik, a kanült tartósítjuk és vérzéscsillapítást követően a sebet intracutan damil-varrattal zárjuk. Sebkötözés után a beteget, obszerváció céljából az onkológiai osztályon helyezzük el. Másnap minden esetben kontroll mellkasröntgent készítünk, és csak abban az esetben engedjük haza, amennyiben a korai szövődményeket kizártuk. A varratot 2 hét múlva vesszük ki.

5. ábra.
A behelyezett port röntgen képe.

6. ábra.
Négy héttel a beavatkozás után.
Eredmények
Kezdetben talán a rutin hiánya miatt is, a beavatkozások hosszabb ideig tartottak, mint jelenleg, és az idők folyamán, a technikánkon is tökéletesítettünk, mely folyamat jelenleg is tart.
A 70 beteg nemenkénti megoszlása: 49 nő, 21 férfi. A daganatonkénti eloszlást az 1. táblázat mutatja, mely tükrözi a korábban mondottakat, miszerint főleg emlő-, vastagbél- és petefészek-daganatok esetén a kezelés, akár évekig is történhet és ezekben az esetekben indokolt lehet a vénaport behelyezése.
A beavatkozás során a v. subclaviát kanüláljuk, de 2 esetben a vena femoralis kanülálására kényszerültünk, az előbbi véna alkalmatlansága miatt. A jobb oldali subclavia vénát 66 esetben kanüláltuk és mindössze 2 betegnél a bal oldalit.

1. táblázat.
A beültetett portok megoszlása a primer tumor lokalizációja szerint
Szövődményeink
Szövődményekről természetesen a mi betegeink kapcsán is említést kell tennünk. A korábban felsorolt korai szövődmények közül eddig mindössze 4 betegünk esetében artéria punkció fordult elő. A későbbi időszakban kialakult szövődményeket a 2. táblázat mutatja.
Gyakorlatunkban is a leggyakoribb késői szövődmény a gyulladás, melynek oka feltehetőleg a port szúrása, használata során a nem megfelelő dezinficiálás volt. Egy esetben a sorozatos, inszufficiens "szurkálások" miatt fájdalmas, később begyulladt hematoma alakult ki. Ezeknél a betegeknél a port használata után néhány perccel hidegrázás, majd magas láz lépett fel. Mindegyik beteg intravénás antibiotikum kezelésben részesült, de végül a port-okat el kellett távolítani.
Itt említjük meg a helyes gyógyszeradagolási technikát, mely során a kamrát a kitapintást követően középen, a speciális tűvel, merőlegesen, ütközésig szúrjuk meg ("koppanásig"). Mivel a kamra tűvel szembeni felszíne titániumból van, az nem szúrható át. Szúrás után mindig érdemes vért aspirálni a fecskendőbe, mert ez is megerősíti a szúrást végző személyt abban, hogy jól szúrta meg a port-ot.
Az onkológiai betegség progressziójával, a betegeknél jelentős testsúlyvesztés alakulhat ki, mely során a mellkasi subcutan zsír mennyisége is drasztikusan lecsökke. Ennek az lehet a következménye, hogy a port-kamra felett a bőr megfeszül, nekrotizál. Ez potenciális fertőzési kapunak tekintendő, ezért ebben az esetben a port-okat azonnal eltávolítottuk. Szintén eltávolítottuk annak a betegünknek a port-ját, aki otthonában elesett és pontosan a beültetés sebét ütötte meg, mely szétnyílt. Mivel a beteg csak több, mint egy héttel később jelentkezett, a váladékozó sebre való tekintettel távolítottuk el a port-ot.

2. táblázat.
Késői szövődmények a centrális vénás port beültetését követően
Trombósis egy betegünknél alakult ki. Ebben az esetben sem a kanül trombotizált, hanem a v. subclavia. Az eset után 1 hónappal - bár a port használható volt, - a beteg kérésére azt eltávolítottuk. A port szétcsúszás és a port elfordulása még a korai időszakban fordult elő és talán az általunk végzett beavatkozás "gyermekbetegségének" volt tekinthető. A port-kamra és a kanül szétcsúszásának egyszerű oka az volt, hogy azokat nem megfelelően applikáltuk egymáshoz. A port elfordulásának az oka, pedig az volt, hogy akkoriban a port-kamrát még nem rögzítettük két felszívódó öltéssel. Mióta ezt megtesszük, ez a szövődmény nem ismétlődött.
A késői szövődmények kialakulásának megelőzésében a kanül megfelelő gondozásának kulcsszerepe van. Helyi gyakorlatunk a következő:
- Vérvétel esetén felhasználásra nem kerülő 5 ml vér visszaszívását követően lehet levenni a vérmintát laborvizsgálatokra.
- Vérvétel, transzfúzió, parenteralis táplálás és kemoterápia után 10 ml, 5000 NE Na-Heparint tartalmazó fiziológiás sóoldattal kell átmosni a kanült. Krisztalloid, kolloid infuzió után elég 10 ml fiziológiás sóoldattal átöblíteni.
- Használaton kívüli véna-portot 4-6 hetente 10 ml, 5000 NE Na-Heparin tartalmú fiziológiás sóoldattal kell átmosni. Mindezeket betartva minimálisra csökkenthető a késői szövődmények gyakorisága.
Következtetés
A világban régi, de intézményünkben új eljárás lényegét, az onkológiában betöltött szerepét és az elmúlt 5 évben szerzett helyi tapasztalatainkat foglaltuk össze. Összességében elmondható, hogy az eljárásnak helye van az onkológiai gyakorlatban és tartós onkológiai kezelés tervezésekor gondolni kell a tartós véna-port lehetőségére, különös tekintettel arra, ha a betegnek alkatilag már rossz perifériás véna-státusza van, vagy a kezelések során károsodtak az erek.
A jól funkcionáló és megfelelően gondozott centrális vénás port megkíméli a beteget a többszöri sikertelen vénaszúrástól, csökkenti a paravazációs szövődmények kockázatát, így a beteg életminőségére pozitív hatással van, s nem utolsó sorban megkönnyíti a szakdolgozók munkáját is.
Megoldatlan viszont a portok megfelelő társadalombiztosítási finanszírozása. Annak ellenére, hogy a Megyei Onkológiai Központ betegei esetében a javallatok következetes figyelembe vétele esetén több százas nagyságrendben lenne szüksége centrális vénába történő biztonságos gyógyszer bevitelre, az évente rendelkezésre álló, eszköz-finanszírozásban elszámolható mennyiség (többszöri keretemelés után) 40 db. A betegeknek csak kis része tudja vállalni a beszerzés mintegy 50 ezer forintnyi összegét, így az esélyegyenlőség (ezen a területen is) csorbát szenved.
Irodalom
- Alberts SR, Citrin D, Rodriguez-Bigas M. Colon, Rectal, and Anal Cancers (Cancer Management: Online Edition) Cancernetwork, 2013. http://www.cancer network.com/cancer-management/colorectal/article /10165/180262
- Cho J-B, Park I-Y, Sung K-Y, et al. Pinch-off syndrome, J Korean Surg. Soc. 2013;85:139-144
- Bodoky Gy. A vastagbél daganatai. Klinikai onkológiai kezelés. In: Bodoky Gy, Kopper L (szerk.): Gasztroenterológiai onkológia. Semmelweis Kiadó, Bp., 2009, 235-247. old.
- Boyle HJ, Droz JP. Management of Castration Refractory Prostate Cancer in Senior Adults. Oncol Hematol Rev (US), 2013;9(2):97-101;
- Desruennes E. Type of Devices for Mid- and Long-term Venous Access. In: Di Carlo I, Biffi R (eds.) Totally Implantable Venous Access Devices. Springer-Verlag Italia 2012, pp. 19-29
- Di Carlo I, Pulvirenti E, Mannino M, et al. Increased Use of Percutaneous Technique for Totally Implantable Venous Access Devices. Is It Real Progress A 27-Year Comprehensive Review on Early Complications, Ann. Surg. Oncol. 2010;17: 1649-1656
- European Medicines Agency. Herceptin 150 mg por oldatos infúzióhoz való koncentrátumhoz alkalmazási előírás. http://www.ema.europa.eu/docs/hu_HU/document_ library/EPAR_-Product_Information/human /000278/WC500074922.pdf;
- Gilde K, Plótár V, Remenár É, és mtsaik. Melanoma malignum In: Kásler M (szerk.): Az onkológia alapjai. Egyetemi tankönyv. Medicina Könyvkiadó Zrt., Bp., 2011, 943-963 old.
- Giordano SH, Temin S, Kirshner JJ, et al. Systemic Therapy for Patients With Advanced Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer: American Society of Clinical Oncology Clinical Practice Guideline. J Clin Oncol Published online before print May 5, 2014, doi: 10.1200/JCO.2013.54.0948;
- Goltz JP, Janssen H, Pertritsh B, et al. Femoral placement of totally implantable venous power ports as an alternative implantation site for patients with central vein occlusions, Support Care Cancer 2014;22: 383-387
- Gödény M. Evidenciákon alapuló multimodális képalkotói diagnosztika főbb daganat csoportokban. IME 8(2), Diagnosztikai Különszám 38-42 (2009)
- El Hammoumi M, El Ouazni M, Arsalane A, et al. Incidents and complications of permanent venous central access systems a series of 1,460 cases, Korean J. Thorac. Cardiovasc. Surg. 2014;47:117-123
- Kelleher FC, Colebatch AJ, Rao A. New Molecular Targets in Lung Adenocarcinoma. Oncol Hemat Rev (US), 2013;9(2):122-8;
- Lee AZ, Khorana AA. Cancer-Associated Thrombosis. In: DeVita VT Jr., Lawrence TS, Rosenberg SA (eds.) Cancer. Principles & Practice of Oncology. 9th Edition. Lippincott Wiliams & Wilkins pp. 2314-2321
- Macintyre PE. Safety and Efficacy of patient-controlled analgesia. Br J Anaesth 87(1):36-46, 2001
- Makoto S. Clinical Indications, Preoperative Assessment, Set-up and Organizational Aspects. In: Di Carlo I, Biffi R (eds.) Totally Implantable Venous Access Devices. Springer-Verlag Italia 2012, pp. 37-43
- Marcy PY, Magné N, Castadot P, et al. Radiological and surgical placement of port devices: a 4-year institutional analysis of procedure performance, quality of life and cost in breast cancer patients, Breast Cancer Res Treat 2005;92: 61-67
- Marcy PY. Central venous access: techniques and indications in oncology, Eur. Ra-diol. 2008;18: 2333-2344
- Moldvay J, Rokszin Gy, Abonyi-Tóth Zs, és mtsai.: A tüdőrák hazai gyógyszeres kezelésének elemzése. Magy Onkol 57:3338, 2013;
- Morgan RJ Jr., Armstrong DK, Alvarez RD, et al. Ovarian Cancer (Including Fallo-pian Tube Cancer and Primary Peritoneal Cancer) Version 3.2014 (NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) http://www.nccn.org/professionals/physician_ gls/pdf/ovarian.pdf
- Ottó Sz, Csuka O. A rosszindulatú daganatok laboratóriumi diagnosztikája. Tumormarkerek. In: Kásler M (szerk.): Az onkológia alapjai. Egyetemi tankönyv. Medicina Könyvkiadó Zrt., Bp., 2011, 191-201 old.
- Patak LS, Tait AR, Mirafzali L, et al. Patient Perspectives of Patient-Controlled An-algesia (PCA) and Methods for Improving Pain Control and Patient Satisfaction. Reg Anesth Pain Med 38(4): 326-333, 2013
- Patel GS, Jaln K, Kumar R, et al. Comparison of peripherally inserted central venous catheters (PICC) versus subcutaneously implanted port-chamber catheters by complication and cost for patients receiving chemotherapy for non-haematological malignancies, Support Care Cancer 2014;22: 121-128
- Pikó B, Laczó I, Szatmári K, et al. Overview of extravasation management and pos-sibilities for risk reduction based on literature data. J Nursing Educ Pract 2013, 3(9): 93-105
- Pikó B, Török E, Varga I, és mtsaik. Az onkológiai kezelés hatásosságának lemérése. A WHO- és a RECIST- rendszer. Magy Radiol online. 2012. 3. évfolyam 2. szám. http://www.radiologia.hu/szakma/mro/cikk/ az_onkológiai_kezelés_hatásosságának_lemérése_a_ who__és_a_recist_rendszer.html
- Povoski SP. Long-Term Central Venous Access, Cancernetwork 2013.http://www.cancernetwork.com/cancermanagement/ long-term-central-venous- access
- Schmoll HJ. Mennyi ideig kezeljük a metasztatikus vastagbélrákot? Klin Onkol 2014, 1(1): 33-39
- Sinkó J. A lázas neutropenia ellátása az onkológiai gyakorlatban. Klin Onkol 2014; 1(1): 49-55.
- Solan MJ & Brady LW. Skin. In. Halperin EC, Perez CA, Brady LW. (eds.) Perez and Brady's Principles and Practice of Radiation Oncology, 5th Edition. Lippincott Williams & Wilkins, Philadelphia, Baltimore, New York, London, Buenos Aires, Hong Kong, Sidney, Tokyo, 2008, pp. 690-702
- Sugárterápiás és Onkológiai Szakmai Kollégium, Anaesthesiologiai és Intenzívterápiás Szakmai Kollégium, Sebészeti Szakmai Kollégium: Vénabiztosítás az onkológiában - Szakmai-módszertani levél, Magyar Onkológia 2004;2: 193-196
- Teichgräber UKM, Kausche S, Nagel SN, et al. Outcome analysis in 3,160 implan-tations of radiologically guided placements of totally implantable central venous port systems, Eur. Radiol. 2011;21: 1224-1232
- Vescia S, Baumgartner AK, Jacobs VR, et al. Management of venous port systems in oncology: a review of current evidence. Ann Oncol 19:9-15, 2008
- Wieners G, Redlich U, Dudeck O, et al. First experiences with intravenous port sys-tems authorized for high pressure injection of contrast agent in multiphasic comput- ed tomography. Röfo 181:664-668, 2009
- Wu C-F, Ko P-J, Wu C-Y, et al. A single-center study of vascular access sites for in-travenous ports, Surg. Today, 2014;44: 723-731
- 1997 évi CLIV törvény az egészségügyről 3 § (m); 16. §, 17. § http://net.jogtar.hu/jr/gen/hjegy_doc.cgi?docid=99700154.TV
Dr. Dimák Sándor
Békés Megyei Pándy Kálmán Kórház, Gyula,
Megyei Onkológiai Központ
Érbetegségek: 2015/1. - 3-9. oldal


