1986-ban állították elő az első kis molekulasúlyú heparint (LMWH-t), a nadroparint. 12 év tapasztalatainak tükrében a LMWH-k szerepét és jelentőségét értékeljük a különböző korképekben. A vénás theromoembóliák megelőzésére nagyobb biztonsággal és hatásosabban alkalmazhatók, mint a nemfrakcionált heparin. Napjainkban világszerte kialakult az az irányzat, hogy a mélyvénás trombózist LMWH-val otthon kezeljék. A készítmények a keringés artériás oldalán is előnyösen alkalmazhatók, elsosorban coronariabetegség, akut ischaemiás stroke kezelésére, valamint terhességben. Fontos technikai újítás az LMW biztonsági fecskendők bevezetése a véletlenszerű tűszúrások elkerülésére, amelyek hepatitis-, HIV-fertozésekhez vezethetnek. Feltételezhető, hogy az LMWH-k térhódítása a következő évezredben tovább folytatódik.
Érbetegségek: 1999/2. - 37-44. oldal
KULCSSZAVAK
vénás trombózis-profilaxis, otthoni kezelés, coronaria- betegségek, terhesség, biztonsági fecskendő
12 éves a Fraxiparine
A vénás thromboembóliák (VTE-k) ellen 80 éve eredményesen alkalmazzák a heparint (1).
A trombózis-profilaxis és kezelés területén a legfontosabb előrelépést a kismolekulasúlyú heparinok (low-mo- lecular-weight heparin, LMWH) bevezetése jelentette. A Sanofi párizsi laboratóriumában már 1975-től intenzív kutatómunkával kerestek olyan gyógyszert, amelynek jelentős antithromboti- kus hatása mellett nincs, vagy alig van anticoagulans, vérzést okozó hatása, így állította elő 1986-ban Choay a CY 216 jelzésű LMWH-frakciót, a nadroparint, ami Fraxiparine néven lett a világon az első és azóta is a legelterjedtebb LMWH. Napjainkban már 12 féle LMWH készítménnyel rendelkezünk. A 12 év alatt szerzett tapasztalatok tükrében a IV. Nemzetközi Fraxiparine Symposium összegezte a VTE- k profilaxisának és kezelésének aktuális kérdéseit, 1998 november végén Lisszabonban. Tanulmányunkban a legújabb eredmények alapján tekintjük át a LMWH-k jelentőségét, különböző kórképekben betöltött szerepét.
Új adatok a vénás thromboembóliák epidemiológiájáról
A vénás thromboembólia (VTE) az ischaemiás szívbetegség és a stroke után a harmadik leggyakoribb cardio- vascularis betegség. Európában évente 600 000, Észak-Amerikában 460 000 esetben alakul ki mélyvénás trombózis (MVT). Tüdőembóliában (PE) az Egyesült Államokban 200 000-en, Angliában 20 000-ren halnak meg minden évben (2, 3).
Magyarországon a vénás betegségek mortalitása feltűnően növekedett. Míg 1970-ben a PE-ra visszavezethető halálozás 10,8 / 100 000 volt, 1990-re ez a mortalitás csaknem megduplázódott: 19,8 / 100 000-re növekedett (4). Intenzív megelőzési programok bevezetése nélkül az elkövetkező években a VTE-k prevalenciájának további növekedésére lehet számítani. A népesség ugyanis évente mintegy 2%- ban öregebb lesz, növekszik a műtétre, különösen a traumatológiai és ortopédiai műtétre kerülő betegek száma, ugyancsak szaporodik a malignus betegségben szenvedők száma, az idős kor pedig egyre kevésbé jelent műtéti ellenjavallatot.
Az MVT azonban a PE lehetőségével nemcsak életveszélyt jelent, hanem krónikus következményei is vannak.
Számolnunk kell a véna billentyűk és a vénafal krónikus károsodásának következtében kialakuló postthrombo- tikus szindrómával. Ez a tünetegyüttes három évvel az MVT után a betegek 35-69%-ában létrejön (5).
Proximalis MVT után pedig az esetek 4-8%-ában a lábszáron vénás ulcus keletkezik (6). A lábszárfekély Magyarország egyes vidékein népbetegségnek számít.
Érthető ezek után, hogy a VTE-k megelőzésére világszerte jelentős erőfeszítéseket tesznek. A szaporodó tanulmányok tartalma azonban sokszor nem felel meg a korszerű klinikofar- makológiai vizsgálat követelményeinek. Az ajánlott profilaktikus módszer hatásosságát ugyanis meggyőzően kell bizonyítani. Ezért a trombózisprofilaxis kérdéseivel foglalkozó nemzetközi konferenciák csak azokat a prospektiv, kontrollált, randomizált vizsgálatokat veszik figyelembe, amelynek objektív diagnosztikus módszert (MVT esetén duplex ultrahang scanninget, legalább D-dimer meghatározással kiegészítve, vagy phlebographiát, PE esetén kombinált perfúziós-inhalációs tüdőscinti- graphiát, vagy tüdőangiographiát) használnak, ugyanabban az időszakban identikus populációkat hasonlítanak össze, és az eredményeket statisztikai módszerekkel értékelik. A megfelelő konfidencia-intervallummal készült tanulmányok és meta-analízisek biztosítják a megbízhatóság szintjét és az ajánlások fokát.
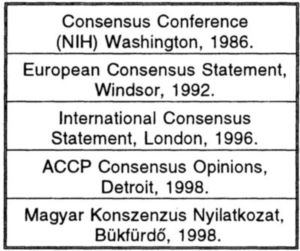
I. táblázat.
Konszenzus konferenciák.
Konszenzus konferenciák a VTE-k profilaxisáról
A VTE-k népegészségügyi jelentőségét egyre több országban ismerték fel, ezért konszenzus konferenciákat szerveztek, hogy meghatározzák a rizikó-faktorokat és segítséget nyújtsanak a hatásos thrombo-profilaktikus módszerek gyakorlati alkalmazásához. Az első konferenciát a National Institute of Health (az Amerikai Egészségügyi Minisztérium) szervezte Washingtonban, 1986-ban. Azóta azonban a VTE- k megelőzésére számos előrelépés történt, az új gyógyszerek és profilaktikus eljárások megjelenése miatt az eredményeket át kellett értékelni és újabb konszenzus konferenciákon kellett aktuális vezérfonalat biztosítani a korszerű klinikai gyakorlat számára (I. táblázat). Valódi konszenzus a thrombo-profi- laxis értékéről elsősorban a postoperatív állapot területén alakult ki. A kisdózisú subcutan LMWH (LDH) általános sebészeti betegeken az MVT kockázatát 60%-kal csökkentette (7, 8). Az LDH profilaxis hátránya három területen jelentkezett.
- A betegek számára meglehetős kellemetlenséget jelentettek a 8, vagy 12 óránként rendszeresen, akár éjjel is adott subcutan injekciók.
- Bár komoly vérzéses szövődmény nagyon ritkán fordult elő, az injekciók beadási helyén suffusiók, a műtéti seb környékén pedig haematomák gyakran alakultak ki.
- Ortopéd-traumatológiai betegeken az eredmények nem voltak meggyőzőek. Napjainkban a profilaktikus módszerek közül világszerte a kismolekulasúlyú heparinok (LMWH) alkalmazása kerül előtérbe (
II. táblázat)
- .
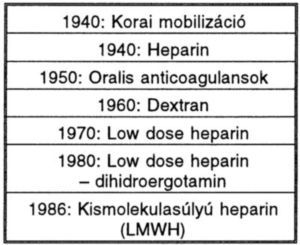
II. táblázat.
A thrombo-prof ilaktikus módszerek történeti áttekintése.
A kis molekulasúlyú heparinok hatásai, előnyök és hátrányok
A heparin nem egységes, jól meghatározott vegyület, hanem különböző számú poliszaharid láncok keveréke. Az egyes láncok hossza és molekulasúlya változó. Ez a molekulasúly 1500-40 000 dalton között van, az átlagos molekulasúly 15 000 dalton. Kiderült, hogy megelőzésre és kezelésre a standard heparinnál előnyösebbek a kismolekulasúlyú heparinok, amelyeket a disznó-, vagy szarvasmarha-bél mucosából származó heparinból, kémiai vagy enzimatikus degradációval, vagy gél filtrációval állítanak elő. A standard, nem frakcionált heparin egyformán hat a koagulációs kaszkádban kulcsszerepet játszó aktivált X faktorra (antithrombotikus hatás - Xa) és az aktivált II faktorra, a thrombinra (anticoagulatiós hatás - Ha). A thrombinra gyakorolt anticoagulatiós hatás abban nyilvánul meg, hogy a vér alva- dási ideje és az aktivált parciális thromboplastin idő (APTT) megnyúlik. Az LMWH-k ezzel szemben lényegesen jobban gátolják a Xa faktort, mint a thrombint, ezért minimális hatásuk van a teljes alvadási időre és az APTT-re: így a vérzés kockázata is kisebb. Az anticoagulatiós hatás ugyanis a poliszaharida lánc hosszától, így molekulasúlyától függ. Minél rövidebb a lánc, annál kisebb a thrombin-ellenes hatás. A 18 szaharida egységnél rövidebb láncnak, amelynek molekulasúlya 5000 daltonnál kisebb, a gyakorlatban nincs thrombin-ellenes hatása.
Későbbi kutatások tisztázták, hogy az LMWH-k hatását nem lehet pusztán anti Xa aktivitással magyarázni. Az összhatásnak csak mintegy 20%-a magyarázható anti Xa aktivitással, a fennmaradó 80%-ért a szövetfaktor-inhibitor (TFPI) felszabadító hatás és más farmakológiai hatások felelősek. A TFPI ugyanis jelentős antithrombotikus szer. Az LMWH-k továbbá módosítják az endothelt, fibrinolitikus aktivátorokat, antithrombocyta anyagokat szabadítanak fel (9). Az LMWH-knak ezenkívül más előnyös biológiai hatásai vannak (III. táblázat).
Az LMWH-k hátránya, hogy egymással nem helyettesíthetők. A farma- kológiailag aktív anyag ugyanis termékenként más és más, az előállítási különbségek miatt a különböző termékek fizikai és kémiai összetétele is különböző. Ennek következtében biológiai hatásukban is eltérések vannak. Az egyes készítmények specifikus dózisait kell használni (IV. táblázat).

III. táblázat.
Az LMWH-k előnyös biológiai hatásai.

IV. táblázat.
Az LMWH készítmények egymással nem helyettesíthetők.
LMWH-k a vénás thromboemboliák megelőzésére
Eddig több mint 50 általános-sebészeti és ortopéd-traumatológiai betegeken végzett objektív klinikai tanulmány és 3 meta-arialízis (10, 11, 12) bizonyította, hogy az LMWH-k a VTE-k profilaxisára hatékonyabbak, vagy legalább olyan hatásúak, mint a nem frakcionált heparin, mellékhatásuk is kevesebb, költségkihatásuk pedig előnyösebb. Ezért egyre inkább átveszik a standard heparin eddigi vezető szerepét a gyógyszeres thrombopro- füaxisban.
Az MVT kezelése korházban, vagy otthon? Legújabb szempontok, jelen helyzet
Nemrégiben három nagy nemzetközi vizsgálat hasonlította össze az MVT kórházban iv. heparinnal és otthon sc. LMWH-val végzett kezelését (13). Az eredmények bizonyították, hogy a terápiás effektus és a szövődmények tekintetében az otthoni kezelés ugyanolyan biztonságos és hatásos, mint a kórházi kezelés.
Az LMWH-val végzett otthoni kezelés vezérfonalának kialakítása érdekében nemrégiben 31 nemzetközileg ismert trombózis-kutató véleményét kérdezték meg. A lisszaboni konferencián az eredményeket Biiller összegezte (14).
A válaszok szerint az MVT-s betegek 20-60%-át lehet otthon kezelni. Kanadában és Hollandiában úgy gondolják, hogy az MVT-ben szenvedő betegek kevesebb mint 20%-át kell hospitalizálni. A kelet-európai országokban, Lengyelországban, Csehországban, Szlovákiában, Romániában, Ukrajnában 40-80%-ban a kórházi kezelés mellett döntenek. Több mint 90%-os konszenzus uralkodik atekin- tetben, hogy az MVT ambuláns kezelése megfelelő alternatívát jelent az otthoni kezeléssel szemben. Az előnyök között elsősorban a költségek csökkenését és a beteg életminőségének javulását említik. Az egyik válasz szerint a beteg nincs kitéve a kórházban szerzett fertőzések veszélyének. A hátrányokat illetően félnek attól, hogy a családorvosok a VTE-s betegséget nem kielégítően ismerik, nincs meg az állandó és rendszeres ellenőrzés lehetősége, félnek a hirtelen, masszív PE- től, valamint attól, hogy a szövődményeket idejében nem ismerik fel. Gondot jelenthet a beteg együttműködése, a mobilizálás, a sc. injekciók technikája, később az orális anticoagulans kezelés ellenőrzése. A szakértők 65%-a úgy gondolja, hogy az akut MVT után kórházból kibocsátott betegek ellenőrzését a kórház, 16%-a szerint a családorvos, 19%-uk szerint pedig mindkettő végezze, rendszeresen, jól meghatározott időpontban. Egyesek azt tanácsolják, hogy az ellenőrzésbe angiológust is vonjanak be. A különösen veszélyeztetett betegeket kórházban kell kontrollálni. A felmérés szerint az otthon kezelt betegeket mindenképpen tájékoztatni kell a következőkről:
- A betegség természete és a szövődmények megértése.
- Azonnali kapcsolatteremtés a kórházzal, ha szövődmény - vérzés, PE stb. - gyanúja merült fel.
- Az orvos, nővér rendszeres ellenőrzése.
- A sc. injekciók technikájának megtanítása.
- 4-5 napos immobilizálás után fokozatos torna, mobilizálás.
- Orális anticoagulans kezelés és annak ellenőrzése, laboratóriumi mo- nitorizálás.
- Kísérő gyógyszeres kezelés, megengedett és tilos gyógyszerek.
- Táplálkozás, mit egyen és mit ne egyen, alkohol- és folyadék-fogyasztás.
- Ellenőrzés, nyomonkövetés, ultrahang- és laboratóriumi kontroll.
- Kompressziós harisnyák használata.
LMWH-k szívbetegségekben, artériás korképekben
12 év tapasztalatai azt mutatják, hogy az LMWH-k adása nemcsak a VTE-k megelőzésében és kezelésében, de szívbetegségekben, a keringés artériás oldalán is előnyös.
Akut coronaria szindrómákban Le- izorovicz meta-analízise értékelte az LMWH-k jelentőségét (15).
6 jelentős tanulmány vizsgálta a különböző LMWH-k szerepét instabil anginában szenvedő betegeken:
- - Gurfinkel a Fraxiparine-t a nem- frakcinált heparinnal és az önmagában adott Aspirinnel hasonlította össze (16).
- A FRISC vizsgálat a dalteparint placeboval szemben (17),
- A FRIC a dalteparint a nemfrakcionált heparinnal szemben (18),
- Az ESSENCE tanulmány az eno- xaparint a nemfrakcionált heparinnal szemben vizsgálta (19).
- A FRAXIS a Fraxiparine két különböző adagolási formáját és a nemfrakcionált heparin egy adagolási formáját hasonlította össze (20).
- A TIMI 11B a hosszú távon adagolt enoxaparint a rövid távú időn át adott, nemfrakcionált heparinnal ösz- szevetve vizsgálta (21).
Az elemzések egyértelműen mutatták, hogy az LMWH-k hatásosabbak, mint a placebo, adásuk legalább olyan biztonságos és hatásos, vagy még hatátosabb, mint a nemfrakcionált heparin alkalmazása az akut fázisban. További előnyös hatást már nem figyeltek meg, ha a kezelést az iniciális fázison túl is folytatták.
Egyre fokozott szerepet kap az LMWH-k alkalmazása az akut myocardialis infarktus (AMI) ellátásában (22). Hatásosan és biztonsággal alkalmazzák, mint kiegészítő kezelést az AMI thrombolysisét követően (23), PTCA után a restenosisok kivédésére (24, 25), az akut ischaemiás stroke kezelésére (26), vagy graftok átjárhatóságának biztosítására; az alsó végtag obliteratív arteriosclerosisa miatt végzett műtétek után (27).
LMWH-k alkalmazása a terhességben
Különböző indikációk, alapján terhesség alatt, mivel nem jut át a placen- tán, a nem-frakcionált heparint ajánlották (28).
A nemfrakcionált hep arinkezelés komoly hátránya volt az esetleges osteoporosis, heparinindukált thrombocytopenia (HIT) kialakulása, a szükséges laboratóriumi monitorizálás és dózis-korrekció. Bár az LMWH-k adását követően alapvetően kevesebb osteoporosis és HIT lép fel és biológiai tulajdonságaik is előnyösebbek, azonban biztonságos alkalmazásukat a terhesség alatt eddig kellően nem demonstrálták.
Nemrégiben Lensing (29) elemezte azokat az elmúlt 12 évben megjelent, mérvadó tanulmányokat, amelyek során a terhesség alatt LMWH-t alkalmaztak. 11 tanulmány és további 10 vezető szülészeti intézet anyagát: 486 terhesség lefolyását vizsgálta. A legtöbben azért kaptak LMWH-t, mert anamnézisükben VTE szerepelt (n=149), a gravidákon autoantitestek jelenlétét mutatták ki (n=163), vagy kellően nem magyarázható magzati veszteségük volt (n=93). Azokon a gravidákon, akiknek jelentős mellékbetegségeik voltak (n=290), a terhességek lefolyása 13,4%-ban kóros volt: abortus, koraszülés, neonatális károsodás, vagy halál, fejlődési rendellenesség jelentkezett. Ha a gravidáknak nem volt mellékbetegségük (n=196), csak 3,1%-ban figyelték meg a terhesség pathológiás kimenetelét. Ez megfelel a normál populációban észlelt értéknek. Nem volt összefüggés az adverz terhességek gyakorisága, valamint az LMWH kezelés tartama és dozirozása között. Egyetlen nőn figyeltek meg szimptómás osteoporosist. 3 terhesség során (0,6%) alakult ki VTE. Egyáltalán nem észleltek klinikailag jelentős vérzést, HIT, vagy con- genitalis malformatio kialakulását.
Tekintetbe véve, hogy a legújabb eredmények alapján az LMWH-k alkalmazása a terhesség alatt a nemfrakcionált heparinnal szemben biztonságos és hatásos alternatívát jelent, az Amsterdam Academic Medical Centre a következő terápiás stratégiát ajánlja:
1. Gondos megfigyelés (tehát nem kezelés) a terhesség alatt, havonta ismételt duplex scanning MVT irányában, majd Fraxiparine profilaxis (0,3 ml) naponta egyszer, a szülés után 6 héten át, azokon a nőkön
- akik thrombophiliások, de sohasem volt VTE-s szövődményük, vagy
- akik nem thrombophiliások, de anamnézisükben VTE-s epizód szerepel.
2. Fraxiparine kezelés (0,4, 0,6 vagy 0,8 ml) naponta kétszer a terhesség alatt, majd azt követően a post-partum periódusban 6 héten át azokon a nőkön
- akiknek anamnézisében VTE szerepel és állapotuk thrombophiliás,
- akiknek anamnézisében recurrens VTE szerepel, vagy
- akiknél terhességük során akut VTE alakul ki.
Technikai újítás: biztonsági fecskendő a véletlenszerű tuszúrások elkerülésére
Egészségügyi dolgozók injekciós tűvel véletlenül megsérthetik kezüket. A sérülés komoly kockázattal jár. Az Európai Közösség tagállamaiban dolgozó ápolónővéreken évente 440 000 véletlenszerű tűszúrás fordul elő. A Mayo klinikán 800 000 punkciót végeznek évente - punkció alatt a vérvételeket és a beadott injekciókat értik - 10 000 punkcióra 1,5 tűszúrásos sérülés esik (30). Összességében az Egyesült Államokban a tűszúrás okozta sérülések számát évi 1 millióra becsülik. Leggyakrabban akkor keletkeznek ilyen sérülések, ha az elhasznált tűket nem a megfelelő konténerbe dobják be, vagy nem használják az előírt tárolót. Másik gyakori sérülési lehetőség a "recapping": mielőtt a használt injekciós tűket a tárolóba dobnák, visszahúzzák a műanyag-hüvelyt az injekciós tűre, eközben szúrják meg ujjukat. Új-Zélandon így sérül az orvosok 60%-a, a nővérek 40%-a (31).
A tűszúrás helyén esetleg kialakuló bakteriális fertőzésen kívül elsősorban háromfajta vírusinfekció átvitelével kell számolnunk (32).
- Hepatitis B vírus (HBV). Az Európai Közösség országaiban tűszúrás útján évente 8200 egészségügyi dolgozó fertőződik HBV-sal (33).
- Hepatitis C vírus (HCV). Francia felmérés alapján fertőződött tű expozíció után a HCV infekció kockázata 10- 15%. Ugyanakkor jelenleg nem rendelkezünk hatásos postexpozíciós profilaxissal hepatitis C ellen.
- HIV vírus. Az AIDS átvitele jelenti a legnagyobb veszélyt. A tűszúrás sérülések 2%-a HIV fertőzött. Az Egyesült Államokban 1997-ben a 45 dokumentált percután úton létrejött HIV infekcióból 41-et okozott injekciós tű, 2-t eltört üveg, 1-et pedig szike (34).
A véletlenszerű tűszúrások elkerülésére fejlesztette ki a Sanofi biztonsági fecskendőjét. Az első ilyen fecskendőben elérhető LMWH a Fraxiparine. Magát a fecskendőt védőhüvely veszi körül. Az injekció beadása után egyik kézzel a hüvely segítségével rögzítjük a fecskendőt, majd másik kézzel visszahúzzuk a fecskendőt, amíg a védőhüvely biztosítéka kiold.
Ezt követően előrecsúsztatjuk a védőhüvelyt, amíg kattanó hangot nem hallunk. A védőhüvely véglegesen befedi és rögzíti a tűt.
Következtetések
12 év tapasztalata megalapozta a LMWH-k helyét az antithrombotics gyógyszerek között. Intenzív laboratóriumi vizsgálatok után számos nemzetközi tanulmány bizonyította, hogy a LMWH-k hatásosan és biztonsággal alkalmazhatók nemcsak a VTE-k megelőzésére és kezelésére, hanem a keringés artériás oldalán is, valamint számos más indikáció alapján. Előnyös biológiai tulajdonságaik miatt Európa után Észak-Amerikában is egyre inkább átveszik a nem-frakcionált heparin helyét. Nem nehéz megjósolni, hogy térhódításuk az új évezredben tovább tart.
Irodalom
- Rék K.: Heparin terápia 1998. (A nyolcvanéves heparin mai alkalmazása). Orv. Hetil., 140: 59-66 (1999).
- Lindblad, B.y Eriksson, A., Bergqvist, D.: Autopsy-verified pulmonary embolism in a surgical department - analysis of the period from 1951 to 1988. Br. J. Surg. 78: 849-52 (1991).
- Nordström, M., Lindblad, B.y Bergqvist, D., Kjellstrom, T.: A prospective study of deepvein thrombosis within a defined urban population. J. Intern. Med. 232: 155-60 (1992).
- Molnár L.y Sándor T., Monos E., Acsády Gy.: A vénás betegségek mortalitásának feltűnő növekedése Magyarországon. Orv. Hetil. 138: 2727- 32 (1997).
- Bergqvist, D.: Prophylaxis against postoperative venous thromboembolism - a survey of surveys. Thromb. Hae- morrh. Disroders 2: 69-73 (1990).
- Franzeck, U., Schalch, I., Juger, K. A. et al: Prospective 12-year follow-up study of clinical and hemodynamic sequele after deep vein thrombosis in low-risk patients. (Zürich study) Circulation 93: 74-79 (1996)
- Sándor T.: A posztoperatív thrombo- embóliás szövődmények megelőzése kisdózisú subcutan heparinnal. In: Az orvostudomány aktuális problémái 38. Szerk.: Káldor A., Gergely, J., Kulka F. Medicina, Budapest, 1980, 90-147.
- Prevention of Venous Thromboembolism. Consensus Statement. Med-Ori- on, Nicosia, 1997, p. 9.
- Fareed, Jeske, W., Hoppensteadt, D. et al: Are the Available Low-Mo- lecular-Weight Heparin Preparations the same? Semin. In Thromb. Hemos- tas. 22: Suppl. 1, 77-91 (1996).
- Leizorovicz A., Haugh, M. C., Cha- puis, F-R. et al: Low molecular weight heparin in prevention of postoperative thrombosis. Br. Med. J. 305: 913-20 (1992).
- Nurmohamed, M., Rosendaal, F., Büller, H.: The efficacy and safety of low molecular weight heparin versus standard heparin in general and orthopaedic surgery. Lancet 340: 152-56 (1992).
- Jorgensen, N. L, Wille-Jorgensen, P., Hauch, O.: Prophylaxis of postoperative thromboembolism with low molecular weight heparins. A review. Br. J. Surg. 80: 689-704 (1993).
- Sándor ?.: A mélyvénás thrombosis otthoni kezelése. Érbetegségek 5: 13-16 (1998).
- Büller, H: DVT treatment in hospital or at home? DVT Forum 1:1-8 (1998)
- Leizoroviczy A.: A meta-analysis of LMWH in the treatment of acute coronary syndromes. IV. International Symposium on Fraxiparine, Lisbon, 1998 Nov., Congr. book. p. 18.
- Gurfinkel, E. P., Manos, E. J., Meja il, R. I. et al: Low molecular weight heparin versus regular heparin or aspirin in the treatment of unstable angina and silent ischaemia. J. Am. Coll. Cardiol. 26: 313-18. (1995).
- Fragmin during Instability in Coronary Artery Disease (FRISC) Study Group: Low molecular weight heparin during instability in coronary artery disease. Lancet 347: 561-68 (1996).
- Klein, W., Buchwald, A., Wilis, S. et al (the FRIC Investigators): Comparison of Low-Molecular-Weight Heparin with Unfractionated Heparin Acutely and with Placebo for 6 Weeks in the Management of Unstable Coronary Artery Disease. Circulation 96: 61-68 (1997)
- Mark, D. ?., Cowper, P. A., Berko- witz, S. D. et al: Economic Assessment of Low-Molecular-Weight Heparin (Enoxaparin) versus Unfractionated Heparin in Acute Coronary Syndrome Patients. Results from the ESSENCE Randomized Trial. Circulation 97: 1702-07 (1998).
- Charbonnier, B., Leizorovicz, A.: Unstable angina and heparin treatment strategy: comparative study between the low molecular weight heparin: nadroparin (Fraxiparine) and unfractionated heparin. IV. International Symposium on Fraxiparine, Lisbon, 1998 Nov., Congr. book, p. 16-17.
- Antman, E. M. and the Thrombolysis in Myocardial Infarction (TIMI) 1 IB Investigators: TIMI 1 IB. Enoxaparin versus unfractionated heparin for unstable angina or non-Q-wave myocardial infarction: a double blind, placebo controlled, parallel group, multicenter trial. Rationale, study design and methods. Am. Heart J. 135: 6 Pt Suppl. 353-60 (1998).
- Savenko, M. P. et al: Experience in the use of Fraxiparine in Myocardial Infarction. Ter. Arkh. 68: 97-14285 (1996).
- Chamuleau, S. A., de Winter; R. J Levi, M. et al: Fraxiparine as adjunctive therapy to thrombolysis for acute myocardial infarction: the FATIMA study. Heart 80: 35-9 (1998).
- Lablanche, J. M., McFadden, E. P., Meneveau, N. et al: Effect of Fraxiparine, a low-molecular-weight heparin on clinical and angiographic restenosis after coronary balloon angioplasty: the FACT study. Circulation 96: 3396-3402 (1997).
- Faxon, D. P., Spiro, T. E., Minor, S. et al: Low molecular weight heparin in prevention of restenosis after angioplasty: results of Enoxaparin Restenosis (ERA) Trial. Circulation 90: 908-14 (1994).
- Kay, R., Wong, K. S.. Yu, Y. L. et al: Low-molecular-weight heparin for the treatment of acute ischemic stroke. N. Engl. J. Med. 333: 1588-93 (1995).
- Edmondson, R. A., Cohen, A. T.t Das, S. K., et al: Low molecular weight heparin versus Aspirin and dipyridamole after femoro-popliteal by-pass grafting. Lancet 344: 914-8 (1994).
- Rákóczi L: Vénás thromboembólia kezelése a terhesség alatt. Gyógyszereink 47: 63-69 (1997).
- Lensing, A. W. A.: The use of low molecular weight heparin in pregnancy. IV. International Symposium on Fraxiparine, Lisbon, 1998 Nov., Congr. book. p. 12.
- Dale, J. C., Pruett, S. K, Maker, M. D.: Accidental Needlestick in the Phlebotomy Service of the Department of Laboratory Medicine and Pathology at Mayo Clinic, Rochester. Mayo Clinic Proc. 73: 611-15 (1998).
- Lum, D., Mason, Z, Meyer-Rochow., G. et al: Needle stick injuries in country general practice. New Zealand Med. J. 110: 122-5. (1997).
- Guillot, F.: Needle stick injuries in health care workers. Epidemiological data. IV. International Symposium on Fraxiparine, Lisbon, 1998. Nov.
- Wuale, J. M., Landman, D., Wallace, B. et al: Déjá Vu: Nosocomial Hepatitis B Virus Transmission and Fingerstick Monitoring. Am. J. Med. 105:296-301 (1998).
- Public Health Service Guidelines for the Management of Health-Care Worker exposures to HIV and Recommendations for Postexposure Prophylaxis. MMWR, CDC Atlanta, 47: 1-33 (1998).
Dr. Sándor Tamás
SOTE II. Sebészeti Klinika
Kútvölgyi Klinikai Tömb
1125 Budapest, Kútvölgyi út 4.
Érbetegségek: 1999/2. - 37-44. oldal


