A krónikus vénás elégtelenség és a szövődmények kezelése komplex, multidisciplináris ellátást igényel. Ez az oka, hogy a legtöbb gyakorló orvos ismeretei és gyakorlati tudása elégtelen a vénás elégtelenségben szenvedő betegek kezeléséhez. A kérdés jelentőségét az határozza meg, hogy a súlyos vénás elégtelenség a fejlett országokban a felnőtt lakosság 5 %-át érinti. A kórok a vénás reflux, ami a vénafal hypoxiáját, gyulladását okozza, a fehérvérsejtek enzimeikkel károsítják a bőr kötőszövetét, a hámsejteket, szövethiány alakul ki. A mikrocirkuláció károsodása és nyiroködéma mindig társul a vénás keringési zavarhoz. Az etiopathogenesis ismerete nélkülözhetetlen a hatékony kezeléshez. A lábszárseb fertőződése gyakori, a szakszerű ellátás megköveteli az evidenciákon alapuló kezelési irányelvek ismeretét. Az ellátás pénz-, és időigényes. Megállapít - ható, hogy Europában és az Amerikai Egyesült Államokban az egészségügyi kötségvetés 1,5-2 %-t fordítják a lábszársebek kezelésére. A szakszerűtlen kezelés megsokszorozza az ellátás költségeit, és a betegség negatív szocio-ekonomiai hatása felmér - hetetlen. A krónikus betegek együttműködésének megnyerése a kezelés folytatásában alapvető. Ez a magyarázata, hogy széles körű a törekvés az új gyógy - szerek alkalmazására. Ilyen a szulodexide, a glükozaminoglikánok osztályába tartozó eredeti molekula.
Érbetegségek: 2012/2. - 41-48. oldal
KULCSSZAVAK
krónikus vénás-lymphás elégtelenség, nem-gyógyuló sebek, infekció, evidenciákon alapuló ellátási irányelvek, multiciplináris ellátás, szocioekonomiai hatás, szulodexide kezelés
Rövidítések
bFGF = fibroblaszt növekedési faktor;
VCAM-1, és ICAM= sejt adhéziós molekulák;
CAMs = sejt adhéziós molekulák;
CEAP = osztályozás a klinikai kép (C), az etiologia (E),
az anatomiai elhelyezkedés (A) és a patofiziologiai
háttér (P) alapján;
IFNγ=interferon gamma;
interleukin (IL)-1ß, MMPs = matrix metalloproteinázok;
PDGF = thrombocyta eredetű növekedési faktor;
ROS = reaktív oxygén csoportok;
TGF-ß1= tumor növekedési faktor-ß1;
TGF-ß1= transzformáló növekedési faktor;
TNF-α= tumor nekrozis faktor
Bevezetés
A vénák működésének elégtelensége, - a krónikus vénás elégtelenség (CVI), a klinikai megjelenés súlyossága szerint, az enyhe kozmetikai problémától az életet is veszélyeztető komplikációkig, - rendkívül különböző lehet. A CVI jelentőségét az orvosok alábecsülik, mert nincsenek figyelemmel a betegség gyakoriságára, nem tudatosul bennük, hogy a vénás elégtelenség kezelése multi - disciplináris ellátást igényel, és a szakszerű kezelés elmaradása súlyos szövődményekkel járhat. Az európai országokban is különböző az incidencia, így a vénás betegségben szenvedőket a lakosság 50-70%-ában határozzák meg. Általában elfogadott, hogy a súlyos vénás elégtelenség a fejlett országokban a felnőtt lakosság 5-10 %-át érinti. A lábszárseb kialakulása súlyos, gyakori szövődmény. A külföldi statisztikák szerint 1,5-3 aktív lábszársebes beteg/100 lakos az arány, de az életkor előrehaladásával a prevalencia növekszik, 60 év felett az ulcus cruris esetek száma 20/100 lakos [1,2,3].
A betegség kezelése költséges, pl. az Egyesült Királyságban évente 300 millió font, és a költségekbe a rehabilitáció, a szociális ellátás és a munkából való kiesés, a rokkanttá válás járulékos költségei nincsenek beleszámítva. A költségek meghatározása nem pontos, de az állapítható meg, hogy a teljes egészségügyi ellátás 1-2 %-át fordítják a lábszársebek kezelésére. A negatív szociális hatás felmérhetetlen.
A bőrgyógyászati és sebészeti problémákon messze túlmutat, hogy a lábszársebek infekciója és a gyakran szükségessé váló szisztémás antibiotikum kezelés olyan következmény, ami beláthatatlan módon befolyásolja a baktériumok rezisztenciájának alakulását.
A vénás eredetű fekélyek nemzetközi és magyarországi epidemiologiája. A civilizált országokban gyakori a CVI, Nyugat-Európában (Franciaország, Németország) varicositas nőkön 25-33%-ban, férfiakon 10-20%-ban található Magyarországon a varicositas prevalenciája megközelíti az 50%-ot [2,4].
A CVI következtében kialakult sebek gyógyulása elhúzódó, ezért az újonnan elfogadott meghatározás a nem-gyógyuló seb elnevezést használja, ami azt a szövethiányt jelenti, ami hat hét után nem gyógyul meg. A nem-gyógyuló sebek a lakosság 1-2%-ánál fordulnak elő. Ez igen magas szám és abban van az orvosok felelőssége, hogy a sebek 75%-a a helytelenül ellátott vénás elégtelenség következtében alakul ki.
A vénás fekélyek etiopathogenezise. Makro-, és mikrocirkulációs elváltozások. A krónikus lábszárseb kialakulásának oka 70 %-ban a vénás elégtelenség, amelyet a vénás reflux következtében kialakult vénás hipertenzió okoz. Patofiziológiai szempontból a CVI négy formája különböztethető meg [4,5,6,7].
- Epifascialis vénás elégtelenség: kiindulópontja az, hogy a sapheno-femoralis junctio billentyűje elégtelenné válik. Az így kialakult reflux az első perforans vénán át a mélyvénák felé terelődik. Amint a szív felé áramló vér újra az elégtelen billentyűhöz ér, a vér egy része ismét az epifascialis saphena vénába kerül, így "privát keringés" alakul ki. A lefelé áramló extra vérmennyiség nagy mennyiségű, és a felületi vénákat kitágítja, a distálisabb billentyűk is elégtelenné válnak. Így jön létre a primer varicositás.
- Subfascialis vénás elégtelenség: kialakulásakor keringési akadály, elzáródás keletkezik a mélyvénákban. Ez a keringési zavar leggyakrabban mélyvénás trombózis rekanalizációja után jön létre. Ilyenkor a billentyűk károsodnak, a véna fala merev csővé alakul át. A vér az elzáródás alatt, a perforáns vénákon át a felületi vénákba terelődik, ezeket kitágítja, szekunder varicositast okoz. A mélyvénák elzáródását okozhatja még tumor, trauma, fejlődési rendellenesség (angiodysplasia). Arteriovenosus fistulák fennállásakor is kialakulhat subfascialis vénás elégtelenség.
- Transfascialis vénás elégtelenség (perforáns elégtelenség): másodlagosan keletkezik a perforáns vénák billentyűinek károsodása következtében. Az ok lehet a mélyvénás trombózis, primér varicositás okozta kóros áramlás. A perforáns vénák elégtelensége miatt a vénás vér a mélyvénák felé áramlik, és ezáltal romlik az izompumpa hatékonysága. Másik hemodinamikai hatás, hogy a vénás vér jelentős része nagy nyomással a felületi vénák felé áramlik. Ilyenkor a tágult vénaszakasz a bőr felszínén félgömbszerűen kiemelkedik és a felette lévő hám elvékonyodik, romlik a hám és a subepidermalis dermis mikrocirkulációja.
A duplex ultrahang vizsgálatok azt igazolják, hogy a vénás eredetű lábszársebek 50 %-át a szuperficiális vénákban kialakult reflux okozza [6, 8].
Fontos kiemelni, hogy mikrocirkulációs zavar, és ezáltal a nyirokrendszer fokozott terhelése miatti nyiroködéma mindig kíséri a nagy vénákban kialakult refluxot. Javasolható a krónikus vénás-lymphás elégtelenség (CVLI) elnevezés, ami pontosan megjeleníti a kórfolyamat lényegét a nomenklaturában [9].
A billentyű elégtelenség következtében hipoxiás területek alakulnak ki, mert az érfal kis erei össze nyomódnak. A véna endothel falán adhéziós molekulák jelennek meg (VCAM-1, és ICAM) melyek a sejtek egymáshoz való kapcsolódását vagy éppen eltávolodását segítik elő. A hipoxiás, gyulladt érfalon a molekulák elősegítik a fehérvérsejtek megtapadását. A fehérvérsejtek enzimeikkel a véna fal valamennyi rétegét károsítják. A szöveti gyulladásos folyamat markerei a sejtek által termelt cytokin családhoz tartozó különböző interleukinek, pl. IL-6, IL-8, IL-10, és ICAM-1, melyek a sejtek között kialakuló, a működéshez szükséges információkat közvetítik. A faktorok száma igen nagy, ezért hatásukat nehéz követni. A gyulladásban aktív cytokinek termelődése krónikus vénás elégtelenségben fokozott (proinflammatory cytokines tumor necrosis factor (TNF)-α interleukin (IL)-ß interferon (IFN)γ és IL-18).
A véna fal átjárhatósága fokozódik, az ér körül ödéma folyadék, majd fibrin gyűrű jelenik meg [10,11]. A fehérvérsejtek enzimeikkel folyamatosan károsítják a kötőszövetet és a hámsejteket. A szövetkárosodás következtében kialakul a lábszárseb (ulcus cruris).
A CVI-ben zajló hemodinamikus és molekuláris folyamatok hatása krónikus gyulladásban nyilvánul meg és kialakulnak a jellegzetes klinikai tünetek: corona phlebectatica paraplantaris, seprűvénák, varicositás, végtag ödéma, nehéz-láb érzés, izomgörcs, fájdalom, pigmentáció, dermatoszklerózis, atrophie blanche, fekélyképződés, gyógyult sebek hegei.
Diagnózis
Azokat a diagnosztikus eljárásokat kell alkalmazni, melyek a seb kialakulásának okáról adnak értékelhető adatokat és ennek alapján teszik lehetővé a kezelés tervezését. Az a. dorsalis pedis és az a. tibialis post. pulzus tapintása tájékoztat a végtag artériás keringéséről.
Funkcionális tesztek:
- Perthes-teszt: egy torniquet (szorítókötés) felhelyezve a térd fölé, majd így sétál a beteg. A mélyvénák megfelelő működése mellett a varixok kiürülnek.
- Palpáció: Schwartz-féle kopogtatási vizsgálat: az insufficiens v. saphena magna beszájadzás esetén a comb distalis részén vagy a térdmagasságában visszerekre gyakorolt nyomás lökéshulláma a lágyékhajlat alatt a v. saphena magna beszájadzásnál kitapintható.
- Valsalva-manőver: ha a beteg köhög vagy haspréselést végez, a visszaáramlás kitapintható, amennyiben a v. saphena magna insufficiens. Ezzel és a kopogtatási vizsgálattal a v. saphena parva is vizsgálható.
- Trendelenburg-teszt: a v. saphena magna varixok fekvő helyzetben kiürülnek. Ekkor kell felhelyezni a szorítókötést a combra, ezután a beteg feláll. Ha a v. saphena magna 30 másodperc alatt nem töltődik fel, akkor a perforánsok megfelelően működnek. Amennyiben a v. saphena magna a szorítás felengedése után gyorsan feltöltődik proximal felől, akkor a beszájadzásnál billentyűelégtelenség van.
Műszeres vizsgálatok:
- Boka/kar (ankle/brachial) vérnyomásindex, Dopplerindex (DI): normál érték 0,9 - 1,2.
- CW- Doppler-vizsgálat.
- Duplex scan ad értékes segítséget a pontos diagnózis felállításához. Ez az ultrahangvizsgálat számos informáciot ad az alsó végtag vénás rendszeréről, kimutatja a reflux jelenlétét és helyét, a proximális vénák esetleges elzáródását.
Nem gyógyuló seb fogalma, etiopathogenesis.
A nem gyógyuló seb a test bármely részén kialakult olyan hám-, és szövethiány, ami több mint hat héten keresztül nem gyógyul. Fiziológiás körülmények között a sebek begyógyulnak, a szövetpusztuláskor termelődő gyulladásos citokinek eliminálódnak, és előtérbe kerülnek a növekedési faktorok, melyek hatására vascularis, kötőszöveti és hámregeneráció következik be. A nem gyógyuló sebek esetében valamilyen okból (infekció, vérellátási elégtelenség, idős kor, alultápláltság, anyagcserebetegség, immundeficiencia, daganat, cito - sztatikus kezelés, stb.) a szövetek újraképződése nem következik be.
A sebgyógyulás rendkívül komplex biológiai folyamatok eredménye. A sebgyógyulásban a gyulladásos fázissal veszi kezdetét a regenerációs folyamat. A gyulladást alkotó fehérvérsejtek - neutrophil leukocyta, macrophag, mastocyta, lymphocyta, - az immunológiai effector, - a gyulladásos citokineket és a növekedési faktorokat termelő sejtek - szerepét töltik be. Az aktivált leukocyták végzik az elhalt szövetek, baktériumok eltávolítását, amihez reaktív oxygén csoportokat (ROS), kationos peptideket, és proteázekat (plasminogén aktivátor, elastase, proteinae 3, stb.) termelnek. A kemokin receptorok a keratinocytákon és az endothel sejteken, fibrocytákon is megtalálhatók, fokozzák a leukocyták átjutását az érfalon. A kemokinek a hámosodásban, angiogenesisben és a kötőszövet remodellációban is szerepet játszanak.
Az akut (normál) sebgyógyuláskor magas koncentrációban vannak jelen interleukinek ( IL-6, IL-8, IL-1ß, PDGF, IFN-γ, és TNF-α) [12,13].
A nem gyogyulo sebek eseteben un. intrinsic faktorok es extrinsic faktorok megvaltoztatjak a sebgyogyulas osszehangolt sejtfolyamatait. Instrinsic faktorok (venas elegtelenseg, diabetes mellitus, ersz.kulet, decubitus, vasculitis, nyirokodema, infekcio) befolyasoljak a verellatast es a cellularis mechanizmusokat. A tartossa valo gyulladas sejtjei altal termelt proteazok, a fokozott proteolyticus aktivitas (neutrophil elastase, MMP-8, gelatinase) roncsoljak a novekedesi faktorokat es az extracellularis matrix proteinjeit, melyek a szoveti regeneracioban fontosak. A megnovekedett mennyiseg. ROS (H2O2, O3) direkt karositjak a szoveti sejteket. Extrinsic faktorok a folyamatosan fennallo fert.zesek, mert a bakteriumok komponensei (extracellularis adherencia protein, N-acetylmuramyl-L-alanyl-D-isogluta mine, toxinok, stb.) gátolják a regenerációban résztvevő sejtek aktivitását és fenntartják a gyulladást. Ezáltal a nemgyógyuló sebeket állandó gyulladás kíséri. A gyulladásban résztvevő fehérvérsejtek aktivitása megnőtt, azonban a gyógyulást reguláló kemokinek termelődése és az egymásra épülő, a szöveti regenerációt elősegítő biologiai folyamatok regulációja megszűnt. Ez a dysreguláció az oka a sebgyógyulás gátlásának.
A nem gyógyuló sebek osztályozása az etiologia alapján igen sokféle lehet pl.: érszűkület, cukorbetegség, decubitus, nyiroködéma, trauma, vasculitis, daganat. A sebek kb. 75%-a krónikus vénás elégtelenség következtében keletkezik [14].
Szocio-ekonómiai vonatkozások
A nem-gyógyuló sebek világszerte súlyos problémát jelentenek. A lábszárseb súlyosan befolyásolja az életminőséget: fájdalom, odorózus seb, fertőzések, mozgáskorlátozottság. Az ellátási szint az állapot súlyosságától függően lehet: járóbeteg ellátás, kórházi kezelés, otthonápolás. Az otthonápolások esetében az aktivitás 80 %-át teszi ki a nem-gyógyuló sebek ellátása. A vénás fekélyek gyógyulása elhúzódó, a sebek 50%-a igényel 1 évnél hosszabb folyamatos kezelést. A seb kiújulásának gyakorisága 1 éven belül 26-79%.
A vénás fekélyek miatti munkanap kiesést évente 2 millióra becsülik. A betegek között gyakori a munkakép - telenség, rokkanttá nyilvánítás, ami magasabb, mint 12,5 %.
Az ellátás költségei rendkívül magasak, az Amerikai Egyesült Államokban 1 milliárd dollár évente, és a fejlett országokban is az egészségügyi ellátás 2 %-a. Ezekben a költségekben nem szerepel a rehabilitáció és a munkából való kiesés költsége. A betegek izolációja a családon és a társadalmon belül is súlyosan érinti az egyént [3].
Az eddig fel nem mért és fenyegető veszély, hogy a bakteriális infekciók és a helytelen antibiotikum politika, azaz a nem megfelelően alkalmazott antibiotikumok hatására növekszik a rezisztens baktériumok száma, ami miatt a különböző baktérium fertőzések "kezelhetetlenné" válnak. Ez beláthatatlan következményekkel fenyegeti nemcsak a fekélyes betegeket, hanem az egész társadalmat.
A nem-gyógyuló sebek szövődményei. A fekélyhez társuló szövődmények elsősorban sebfertőzés következtében keletkeznek: - phlebitis, - phlebotrombosis, - lymphangitis, - lymphadenopathia, - cellulitis, - erysipelas, - abscessus, - sipoly, - fasciitis necrotisans, - gangréna, - szepszis.
Riziko faktorok. A CVI kialaklulásában és a szövődményes sebképződésben a leggyakoribb rizikó tényezők: - pozitiv családi anamnézis, - előre haladott életkor, - rossz általános állapot (tápláltság, sorvasztó betegségek, pszichés állapot), - alkoholizmus, - szisztémás betegségek (szívbetegség, diabetes mellitus, vesebetegség, májbetegség, immunbetegség, thrombofilia, daganat), - trauma, - mozgásszervi megbetegedés (immobilitás, arthrosis), - önellátás hiánya (képes-e önellátásra, fizikai vagy pszichés gátoltság), - rossz szociális helyzet.
A vénás eredetű fekély korszerű kezelése
A sikeres kezeléshez alapvető a pontos diagnózis, és meg kell határozni a seb stádiumát is.
A négy stádium esetében más a sebellátás és a kiegészítő kezelések is.
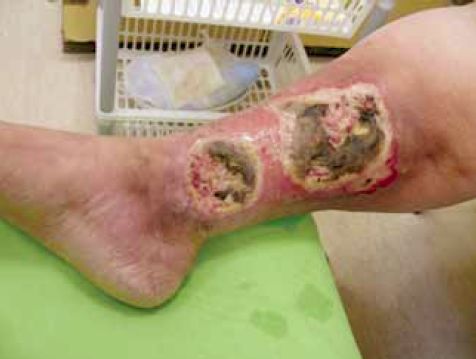
Nekrotikus seb: a szövetkárosodás következtében elhalt szövetek, véralvadék, sebváladék, baktériumok alkotják a nekrotikus felrakódást a sebalapon és a sebszéleken (1. ábra).
Váladékozó, fertőzött seb: a sebalapon a váladék nyirokfolyadékból, a gyulladásos sejtekből és az elhalt szövetek autolitikus anyagaiból képződik. Infekcióról akkor beszélünk, ha a baktériumok mennyisége a szövetben >105/mg.
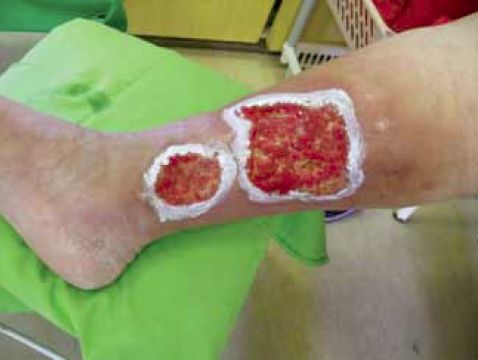
Granulálódó seb: a növekedési faktorok hatására megindul az új szövetek képződése. Ez eredményezi az érdús, vörös színű granulációs szövetet a sebalapon (2. ábra).
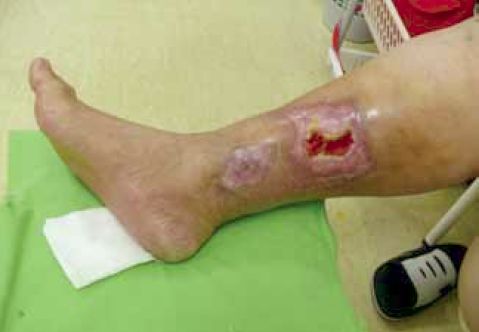
Hámosodó seb: a sebalapon kialakult granulációs szövet megteremti az alapot az epidermális-dermalis kapcsolódás számára, és megindul a hámsejtek osztódása és a hámosodás. A sebek széle menetelessé válik, látható a gyöngyházfényű új hámszövet (3. ábra).
A nem gyógyuló sebek szakszerű kezelésének elemei:
A szakszerű kezelés irányelvei tapasztalatokon és evidenciákon alapulnak. Az irányelveket szakmai csoportok dolgozzák ki és ezeknek ismerete és követése ajánlott az alapellátásban, házi ápolásban dolgozó családorvosoknak, a szakrendelőben, kórházban dolgozó bőrgyógyászoknak, sebészeknek, érsebészeknek, a diagnosztikai eljárásokat végző belgyógyászoknak, angiológusoknak, diabetologusoknak, infektologusoknak, radiológusoknak és idős - otthonokban, ápolási intézményekben dolgozóknak [15,16,17].
- Diagnózis (vénás, artériás, nyiroködémához, dia - beteshez társuló, neuropathia, stb.).
- A seb típusának megállapítása (nekrotikus, fertőzött, granulálódó, hámosodó).
- Az ellátási szint megállapítása (alapellátás, szak - rendelő, kórház, otthonápolás, ápolási otthon).
- Debridement - nekrotomia - sebészi, mechanikus, autolytikus, lárva kezelés módszerei alkalmazhatók az elhalt szövetek eltávolítására [18].
- Infekció kontroll, bakteriológiai leoltás (ha szükséges), antibiotikum választás.
- Váladékkontroll, a sebkörnyék ellátása [19].
- Fájdalomkontroll, a fájdalom kezelése fontos, erősíti a beteg bizalmát és együttműködését, a stressz csökkenti a növekedési faktorok termelődésében szerepet játszó immunrendszer aktivitását.
- A helyi kezelés elemeinek meghatározása: fertőtlenítés, kötszerek, bőrápolás.
- Nyiroködéma kezelése: az ödémamentesítésben a kompressziós pólya alkalmazása, gyógytorna elengedhetetlen, - ez "A" evidencia. A rövid megnyúlású kompressziós pólya csökkenti a vénás hipertenziót, fokozza az izompumpát, oki kezelést jelent a vénás keringési elégtelenség miatt kialakult sebekben. Az alkalmazást nehezíti, hogy a szakszerű pólyázást a betegnek meg kell tanítani, ami időigényes. A betegek nehezen fogadják el a pólya viselését és rossz a beteg compliance [20].
- Sebészeti eljárások (sebek fedése, transzplantáció), érsebészeti eljárások (varicektomia, sclerotizáció, endovascularis beavatkozások, mélyvénák műtétei, stb.).
- Gyógyszeres kezelések:
- Venotonikumok: flavonoidok [16] és pentoxifyllin. A seb "okának", a krónikus vénás elégtelenségnek a kezelése: a komplex patogenetikai folyamatban fontos szerepet játszanak az endothel sejtek közötti kapcsolatok, és az endothel sejtek luminális membránjának, a membrán receptoroknak a károsodásai. Ezek a változások a fehérvérsejtek kitapadását, az endothel sejtek közötti kapcsolatok meglazulását, fibrin- és gyulladásos sejtek érfalon való átjutását, érkörüli gyulladásos gyűrű kialakulását eredményezik. Az un. venotonikumok vagy kapilláris stabilizáló gyógyszerek jó hatásúak az érfal károsodásban, és enyhítik a nehézláb-érzés, fájdalom és ödéma tüneteit. A vénás eredetű sebek kezelésében nemzetközi ajánlások alapján hatékony a pentoxifyllin, a flavonoidok [21], kiemelendő a mikronizált tisztított flavonoid frakció hatékonysága [16].
- Szulodexide alkalmazása: Magyarországon új lehetőség a vénás fekély kezelésében.
A vénás nyomás emelkedése következtében károsodik az erek endothel bélése, a gyulladás következtében aktiválódnak a leukocyták, trombocyták. Ez a mechanizmus időben kezelendő, hogy ne alakuljon ki az endothel tartós károsodása, mikrothrombusok és következményes mikrocirkulációs zavar a bőr kapilláris hálózatában, amit krónikus gyulladás, szövetelhalás, fekélyképződés követ.
A szulodexide a glükozaminoglikánok (GAG) osztályába tartozó eredeti molekula. A GAG egy természetes poliszaharida származék, ami különböző szulfatált diszaharid láncokból áll. A GAG a szervezetben mindenhol megtalálható és egy protein maghoz kötött, amivel a komplex proton glikán molekulát alkot, ami igen sok biológiai funkciót közvetít. A legismertebb, terápiában is használt GAG a heparin - Iduronil-glükozaminilglikánból (IGS; molekulájának 80%-a) és dermatán szulfátból (DS; 20%) áll, melyet trombozisveszéllyel járó érbetegségek kezelésére alkalmaznak. Két típusa használatos: 1. nem frakcionált heparin (UFH) és 2. az alacsony molekulasúlyú heparin (LMWH). A szulodexide a keringési rendszerben fejti ki hatását, azonban hatás - profilja eltér az UFH és LMWH hatásától.
A farmakokinetikai vizsgálatokazt mutatják, hogy a heparinoktól eltérően, orális alkalmazásnál a szulodexide a bélnyálkahártyán keresztül jelentős mértékben felszívódik. Nagy affinitást mutat az érfal iránt, amelyben a felszívódás után kimutatható. Az orális alkalmazhatóság lehetősége növeli a beteg compliance-t.
Parenteralis alkalmazás esetén a vérzési kockázat, más terápiás GAG-okhoz hasonlítva, kisebb. Ennek az a magyarázata, hogy nem kifejezett a kapcsolódás az antitrombin 3-al, és ugyanakkor gátolja a heparin cofactor 2-t, ezáltal szignifikáns trombin gátlás alakul ki minimális szisztémás alvadásgátló hatással. Ennek alapján a szulodexide képes akadályozni a trombus kialakulást és a trombus növekedését is. Ez a hatás azáltal érhető el, hogy a gyógyszer védi az endothel sejtek lumen felé néző membránjának glükokalix rétegét, és hat az endothelium és a szubendotheliális kötőszövetek, valamint a sima - izomszövetek szintjén is. Ez azzal a hatással jár, hogy a szulodexide javítja a véráramlást és védi az érfalat is a károsodástól.
Orális alkalmazás esetén (Vessel Due lágy kapszula) gyakorlatilag nem alakulnak ki vérzéses mellékhatások. Ez azt jelenti, hogy a szisztémás hemokoagulációs paramétereket (aPTT, PT) nem szükséges folyamatosan monitorozni akkor, ha a gyógyszert a javasolt dózisban adják. Azokban az esetekben, ha más, potenciálisan vérzést okozó gyógyszerekkel kombinálják, mint a trombocita gátlók (szalicilsav, non-steroid gyulladáscsökkentők, ticlopidine, stb.), akkor laboratoriumi ellenőrzés javasolt. A szulodexide kezeléskor akkor javasolt a véralvadási paraméterek rendszeres monitorozása, ha együtt adják antikoagulánsokkal (heparin, LMWH) melyek fokozhatják a heparin-jellegű molekula hatását.
Hatásmechanizmus: a szulodexide antitrombotikus hatása felülmúlja egyéb GAG származékok hatásait. Míg a heparin csak az antitrombin III-al kapcsolódik, ami a keringő trombinra hat, a szulodexide képes aktiválni a heparin cofaktor II-t, ami egy olyan protein, mely képes inaktiválni a fibrinhez kötött trombint. Ez a tulajdonság különösen az ischemiás szindromákban fontos, melyekben a trombus növekedése még az akut epizódok után is folytatódhat. A szulodexide hatásmechanizmusát a következő aktivitásokkal lehet magyarázni: - antitrombin (szabad trombin és fibrinhez kötött trombin), - profibrinolitikus aktivitás: aktiválja a szöveti plazminogén aktivátort (tPA) és csökkenti a plazminogén aktivátor gátlást (PAI), - trombocita aggregáció gátlás: azáltal, hogy gátolja a polimorfonukleáris leukociták cathepsin G enzimet, - antiviszkozitási aktivitás: a vér fibrinogén tartalmának csökkentésével fokozza a vér áramlás sebességét, - anti - proliferativ hatás: a simaizom sejtek és mezangiális sejtek érfalban történő proliferációját gátolja azáltal, hogy néhány növekedési faktort gátol, - biztosítja az érfal normál átjárhatóságát azáltal, hogy akadályozza az érfal sejtjei közötti extracelluláris matrix felszaporodást, - gyulladáscsökkentő aktivitás: csökkenti a C-reaktív protein (CRP) szintet és csökkenti a membrán attakk komplex (MAC) lerakódást. A fenti hatásmechanizmusok következtében az érfal károsodás mind a vénákban mind az artériákban csökken [22].
Az orális alkalmazhatóság és a vérzések alacsony kockázata teszik alkalmassá a Vessel Due kapszulát a krónikus betegségek elhúzódó kezelésére. Összefoglalva a szulodexide hatását: antitrombin, anti-FaktorXa, profibrinolytikus aktivitás, trombocita aggregáció gátlás, vér viszkozitás csökkentés, gyulladáscsökkentő aktivitás, az érfal átjárhatóságnak a normalizálása, növekedési faktorok termelődésének visszaszorítása révén az érfal proliferációjának gátlása. A betegségek súlyossága határozza meg az esetleges parenterális (intravénás vagy intramuszkuláris) vagy az orális alkalmazást. Elhúzódó alkalmazás esetén az orális kapszula részesítendő előnyben. Mindezek a hatások azzal a klinikai eredménnyel járnak, hogy a szulodexide hatására a szubjektív és az objektív tünetek javulnak, az érbetegség progressziója lassul [23]. A következő esetekben alkalmazható: artériás trombózis, atheroszklerózis, krónikus vénás elégtelenség, mikrocirkuláció károsodása.
A szulodexide mellékhatásokról, ha az ajánlott dózisban alkalmazzák, igen kevés közlemény van. Leírtak fájdalmat, égő érzést, bőrpírt az injekció helyén, - hányingert, hányást, epigasztriális fájdalmat és pontosan nem meghatározott bőrtüneteket.
A szulodexide klinikai hatásának vizsgálata vénás eredetű ulcus esetében: 235 beteget kezeltek randomizált multicentrikus, placebo kontrollált, kettős vak vizsgálat keretében. A kezelés első fázisában naponta 2-4 kapszula (50mg/kapszula), míg a parenterális adagolásnál 1 ampulla naponta izomba vagy vénába (2 ml oldat, 600 LSU hatóanyag). Elhúzódó kezelés esetén (2x50 mg kapszula naponta) a seb lokális kezelése megfelelt a nemzetközileg elfogadott standard kezelésnek, amit kompressziós pólya kezeléssel egészítettek ki. A sebgyógyulási ráta 52,5% volt a szulodexiddel kezelt betegeknél, és 32,7% a placebo kontrollos esetekben [23]. A kezelés 3 hónapig tartott.
Az eredmények azt bizonyították, hogy a vénás eredetű sebek kezelésében helye van a szulodexid keze - lésnek. Azáltal hogy képes megváltoztatni az endothel működést, a mikrotrombusok kialakulását, a perikapilláris fibrin felszaporodását, gyorsabb sebgyógyulás érhető el, javulnak a szubjektív panaszok is (izomgörcs, nehéz láb érzés, fájdalom). Az a tény, hogy kapszula formában is adható, nemcsak parenterálisan, növeli a betegek együttműködését. - Granulocyta macrophag colonia stimuláló faktorok (rHuGM-CSF): Növeli a seb feltisztulását végző fagocita aktivitását, megindítja a növekedési faktorok képződését (magas eveidencia). Különböző növekedési faktorok (keratinocyta, thrombocyta eredetű) lokális alkalmazása nagyon költséges.
- Vacuum alkalmazása (Vacuum-Associated Closure- VAC): Elsősorban ödémával kísért vénás eredetű és diabeteses fekélyek esetében hatékony. Cukorbeteg láb sebeinek kezelésében a negatív nyomás csökkenti a sebkörnyéki ödémát, és meggyorsítja a váladék távozását a sebből. A vacuum által létrehozott microdeformitások elősegítik a szöveti proliferációt a sebágyban, és a granulációs szövet kialakulását. A mellékhatások lehetősége fertőzött sebek esetén igen jelentős, ezt figyelembe kell venni. Ez a magyarázata, hogy szisztémás antibiotikummal és lokálisan, ezüst ionokat tartalmazó kiegészítőkkel javasolt a módszer.
- Oxygén kezelés: Hyperbarikus oxygén kezelést (HBO) elsősorban cukorbeteg láb sebeinek kezelésében alkalmaznak. A transzcután oxygén több vizsgáló szerint hatékonyan javítja a nem gyógyuló, kóros nyomáspontok területén kialakuló fekélyeket. Több megfigyelés és randomizált tanulmányok szükségesek, melyek a végtag tehermentesítése és a szisztémás antibiotikum kezeléssel szemben, bizonyítják a módszer elsődlegességét. Nem javasolt az eljárás önálló alkalmazása, hanem a sebkezelési módszerek (debridement, antimikróbás kezelés, kompressziós kezelés, stb.) sorába való beillesztése ajánlott.
- Fénykezelés: Nincsenek összehasonlító vizsgálatok, melyek bizonyítanák, hogy lézerfény vagy a polarizált rezgő fény elősegíti a sebgyógyulást. A természet - gyógyászok jó eredményekről számolnak be, amit azzal magyaráznak, hogy a lézerfény elősegíti a kötőszöveti sejtek és a hámsejtek újraképződését, és ezáltal a szövethiányok gyorsabb gyógyulását.
- Kísérőbetegségek kezelése: A kísérő betegségek fennállásáról az anamnézis tájékoztat. A leggyakoribb társbetegségek: hipertónia, ischaemiás szívbetegség, diabetes mellitus, rheumatoid arthritis, máj-, vesebetegség, immunbetegség, thromboembolia, pajzsmirigy betegség. Ezen betegségek kezelése folyamatosan szükséges.
Irodalom
- Carpentier, P. H., Maricq, H. R., Biro, C. és mtsai: Prevalence, risk factors and clinical patterns of chronic venous disorders of lower limbs: a population based study in France. J. Vasc. Surg., 2004; 40: 650-659.
- Bihari I., Tornóci L., Bihari P.: Az alsó végtagi varicositas hazai epidemiologiai felmérése. Érbetegségek, 2002; 9:57–62.
- Evans, C.J., Fowkes, F.G., Ruckley, C.V. és mtsai: Prevalence of varicose veins and chronic venous insufficiency in men and women in the general population. J. Epidemiol. Community. Health., 1999; 53:149-153.
- Sándor, T.: Pathomechanism of chronic venous insufficiency and leg ulcer. Acta. Physiol. Hung., 2004; 91;131-145.
- Daróczy, J.: A krónikus nyiroködéma. Háziorvos Továbbképző Szemle, 2000; 6:344-347.
- Sándor, T.: Krónikus vénás betegség - ahogy ma látjuk. Orv.Hetil., 2010; 151:131-139.
- Daróczy J.: A krónikus vénás elégtelenség - ulcus cruris betegség korszerű szemlélete. Háziorvos Továbbképző Szemle, 1997; 2:58-63.
- Caggiati, A., Bergan, J.J., Gloviczki, P. és mtsai: International Interdisciplinary Consensus Committee on Venous Anatomical Terminology. Nomenclature of the veins of the lower limbs: an international inter disciplinary consensus statement. J. Vasc. Surg., 2002; 36:416–422.
- Daróczy, J.: A krónikus vénás-lymphás elégtelenség kezelése. Praxis, 2006; 5:51-54.
- Coleridge Smith, Ph.: Deleterious effects of white cells in the course of skin damage in CVI. Int. Angiol., 2002; Suppl 1.,26-32.
- Smith, PC.: The causes of skin damage and leg ulceration in chronic venous disease. Int. J. Low Extrem Wounds, 2006; 5:160-168.
- Eming, SA., Krieg, T., Davidson, JM.: Inflammation in wound repair: molecular and cellular mechanisms. J. Invest.Dermatol., 2007; 127:514-525.
- Reilkoff, RA., Bucala, R., Herzog, EL.: Fibrocytes: emerging effector cells in chronic inflammation. Nat.Rev.Immunol., 2011; 11:427-435.
- Daróczy, J.: Az ulcus cruris differenciáldiagnosztikája és ellátása a háziorvosi gyakorlatban. Háziorvos Továbbképző Szemle 2005; 10:497-503.
- Gottroup, F., Apelquist, J., Price, P.E.: Outcomes in controlled and comparative studies on non-healing wounds: recommendations to improve the quality of evidence in wound management. J. wound Care., 2010; 19:237-68.
- Editorial: Management of chronic venous disorders of the lower limbs: guidelines according to scientific evidence. Int. Angiol., 2008; 27:1-58.
- Daróczy, J.: Krónikus bőrsebek korszerű kezelésének irányelve. IME, 2008; 3:30-35.
- Daróczy, J.: Vénás eredetű fekélyek korszerű kezelése. I. rész . Praxis,2009; 4:37-43.
- Daróczy, J.: Vénás eredetű fekélyek korszerű kezelése II. rész. Praxis, 2009; 5:31-36.
- Daróczy, J.: Bőr és lágyrészfertőzések nyiroködémában. Bőrgyógy. Vener. Szle., 2009; 85:164-168.
- Daróczy, J., Pál, A., Blaskó, Gy.: Krónikus vénáslymphás elégtelenség következtében kialakult „nehéz láb” tünetegyüttesben szenvedő betegek mikrocirkulációjának változása flavonoid-származékkal (procyanidol oligomerek) végzett kezelés hatására (lézer-Doppler módszer alkalmazása). Orv.Hetil., 2004; 145:1177-1181.
- Mauro, M., Ferraro, G., Palmieri,G.:Profibrinolytic and antithrombotic effects of sulodexide oral administration: a double blind, crossover, placebo controlled study. Curr.Ther.Res., 1992; 51:342-350.
- Coccheri S.,Scondotto G., Agnelli G. és mtsai: Randomised, double blind, multicentre, placebo controlled study of Sulodexide in the treatment of venous leg ulcers. Thromb. Haemost., 2002; 87:947-52.
Dr. Daróczy Judit
Egyesített Szent István és Szent László Kórház Ri.
Bőrgyógyászati Osztály és Lymphoedema
Rehabilitációs Osztály, Budapest
Érbetegségek: 2012/2. - 41-48. oldal