A pulmonális embólia képi diagnosztikájának csapdái és intervenciós kezelésének lehetősége: A szerzők a mindennapos klinikai rutinban gyakran előforduló tüdőembólia kimutatásának nehézségeit szemléltetik egy nyelőcső daganatos beteg példáján. A ma már hazánkban is rendszeresen használt spirál CT-vizsgálat diagnosztikus, de csak akkor, ha megfelelő protokollal végezzük cl. A szisztémás trombolízist súlyos embólia kapcsán rutinszerűen hajtjuk végre. Daganatos betegben, amikor e kezelési mód vérzést okozhat, sikerrel alkalmazható a katéteres kezelés, a szelektív trombolízis.
Érbetegségek: 2005/1. 3-8. oldal
KULCSSZAVAK
Pulmonális embólia, spirál-CT, pulmonális angiográfia, szelektív trombolízis
Bevezetés
A pulmonális embólia az egyik leggyakoribb, változó súlyosságú kórkép. Mellkasi panaszok, fulladás jelentkezésekor sürgősségi felvételi és intenzív osztályok, belgyógyászati osztályok orvosai, oxiológusok sokszor találkoznak azzal a problémával, bogy igazolni vagy kizárni kell e betegség fennállását. A pulmonális embólia kimutatásában az izotóp-diagnosztika, a pulmonális szcintigráfia szerepe ismert, a radiológiai módszerek - a katéterezéssel járó angiográfiát nem számítva - nemigen adnak segítséget a kezelőorvosnak (1-5). Az 1990-es évek eleje óta a radiológia eszköztárában a spirál vagy helikális CT, amely - mint számos vascularis betegségben, így - a pulmonális embólia tekintetében is szinte forradalmi előrelépést jelentett: gyorsan, a beteget kevésbé terhelő módon tudja a truncus pulmonalis fő ágaiban, a segmentalis artériákban kimutatni a thrombust. Az elmúlt években számos közlemény foglalkozott e betegség diagnosztikájával, a radiológiai vizsgálatokkal (6-13), illetve kezelésével (2, 9, 12, 14), a Medicina Thoracalis 1999. szeptemberi számának témája is e betegség kórismézése, kezelése volt (5-9). Egy nyelőcső daganatos beteg esetével kívánjuk bemutatni a pulmonális embólia képi diagnosztikájának módszertani problémáit, a kezelésben az intervenciós radiológia eszközeinek lehetőségét.
Esetismertetés
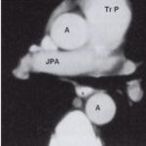
K. L. 53 éves férfi beteget kb. 1,5 hónapos időtartam alatti 3-4 kg-os fogyás miatt kezdték el vizsgálni. Nyelési panasza nem volt, gasztroszkópia során derült fény a nyelő-cső középső harmad határi, hátsó fali polipoid tumorra. A szövettani vizsgálat eredménye laphám sejtes rák volt. A tervezett műtét előtti vizsgálatok, majd műtét, nyelőcső resectio elvégzése miatt vették fel a Pécsi Sebészeti Klinikára. Az anamnéziséból kiemelendő még alsó végtagi varicectomia, alsó végtagi thrombosis, amelyet megfelelően beállított antikoaguláns szerrel kezeltek. Kórházi felvételét követően légzés funkciós vizsgálat, nyelőcső endoszonográfia, hasi UH, nyelőcső röntgen és EKG vizsgálat, aneszteziológiai konzílium történt. A rutin preoperatív vizsgálat része volt a mellkas CT-vizsgálat is. A vizsgálatot megelőző hajnalon a betegnél rossz közérzet alakult ki, fulladás jelentkezett. Mivel a vizsgálat idején a korábban, a rosszullét előtt megírt vizsgálatkérő nyomtatvány állt rendelkezésre, amelyekben a nyelőcső daganattal kapcsolatos anamnesztikus információk szerepeltek, ezért a mellkas CT-vizsgálat a megszokott módon zajlott le. A leletben a nyelőcső felső harmadában a fal egyenetlen megvastagodásáról, a normális nagyság felső határán lévő mediastinalis nyirokcsomókról esett szó (1. ábra).
|
|
|
|
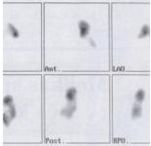
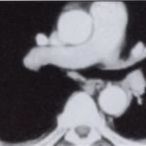
A vizsgálatot Picker PQ 5000 típusú, IV. generációs spirál CT berendezéssel végeztük el, spirál üzemmódban, a tüdőcsúcsok és a rekeszkupola között, 10 mm-es szeletvastagsaggal, kb. 55 másodperces késleltetési idővel, 2 ml/s injektálási ütemmel. (A késleltetési idő az az időtartam, amennyi a kontrasztanyag beadás kezdete és az adatgyűjtés, a mérés között telik el.) A CT-vizsgálat után, tekintettel az akut légzőszervi tünetekre, tüdő perfúziós szcintigráfiára is sor került. A vizsgálat során a jobb tüdő vetületében nem volt kimutatható perfúzió, baloldalon a tüdőben több gócú, nagy kiterjedésű perfúziós defektus ábrázolódott (2. ábra). Az ismertté vált szubtotális embólia kórisméjére való tekintettel intenzív terápiás konzíliumra került sor. Tekintettel a malignus alapbetegségre, a nagy dózisú fibrinolitikus keze-lés esetén reális lett volna a vérzéses szövődmény veszélye, ezért az aneszteziológusok alternatív kezelési módot javasoltak. A katéteres kezelés előtt egy ismételt mellkas CT-vizsgálat történt, amelyet már a pulmonális embólia fennálIásának ismeretében végeztünk el. Minden ilyen esetben a megszokottól eltérő módon kell elvégezni a mellkas CT-vizsgálatot: a natív mérés után 3-5 mm-es metszetek készül-nek az aortaív és a tüdő hilusok alsó pólusa között az arté¬riás fázisban, kb. 20 másodperces késleltetési idővel, 3-4 ml/s kontrasztanyag adagolási ütemmel. Ez a vizsgálat világosan mutatta, hogy a jobb a. pulmonalis lumenét csaknem teljesen elzárta a vérrög, baloldalon az elzáródás csak kisebb mértékű volt, a segmentalis ágakat érintette. Az ilyen módon elvégzett vizsgálat során a kontrasztanyagot intenzíven halmozó érben telődési hiányként ábrázolható az embolus (3. ábra). E vizsgálat eredményét is figyelembe véve, intervenciós radiológiai beavatkozás mellett döntöttünk.
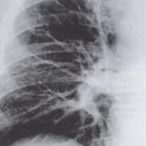
A pulmonális angiográfiát és trombolízist pigtail katéterrel végeztük el. A beavatkozás négy napot vett igénybe, a kezelés hatásosságát meghatározott időközönként kontroll-vizsgálatok segítségével állapítottuk meg (6, 12, 24, 36, 48, 60, 72, 84 óra). Ez idő alatt összesen 3.250.000 IU Streptokinase-t és 30.000 IU Heparint adtunk. A kezelés 4. napján az alacsony plazminogén szint miatt 700 ml friss fagyasztott plazmát is kapott a beteg. A kezdeti állapothoz képest a 24 órás kontroll is jelentős javulást mutatott, a 84 órás kontroll felvétel a lebeny artériák teljes megnyílását igazolta, a segmentalis artériák szintjén néhány reziduális thrombussal (4. és 5. ábra). A kezelés végén, a 4. napon kontroll CT-vizsgálat bizonyította a javulást, a jobb oldali pulmonális artéria rekanalizacióját (6. ábra).
Körülbelül öt héttel az embólia sikeres kezelése után került a beteg ismételten felvételre, majd az alábbi beavatkozások történtek: első lépésben a bal vena femoralis communis lekötése, v. iliaca thrombectomia zajlott le. Az ezt követő műtét legfontosabb mozzanatai: a nyelőcső resectiója, a tápcsatorna folytonosságának gyomorral történő pótlása, a gyomor kisgörbűletének Akiyama szerinti resectiója után azt a hátsó mediastinumba vezetve, a nyakon oesophago-gastricus anastomosist képeztek a sebészszerzők. A posztoperatív szakban többszörös sebészi szövődmény alakult ki (a felhúzott gyomron necrosis, később neooesophago-trachealis fistula), ezért reoperációkat kellett végezni. Átmenetileg a beteget intenzív osztályon is ápolták, de felépült, elhagyta a klinikát, s folyamatosan szedte a Syncumart. Megközelítőleg fél évvel a nyelőcső resectio után a kapcsolat megszakadt a beteggel; információink szerint néhány hónappal később életét vesztette.
|
|
|
|
Megbeszélés
A pulmonális embólia fontos közegészségügyi probléma. Gyakoriságát nehéz pontosan meghatározni, már csak azért is, mert a pulmonális érképletek elzáródásának helye szerint a perifériás elzáródás, multiplex embolizáció és az azonnali halált okozó teljes elzáródás között igen széles spektrummal jellemezhető a klinikum.A kórkép diagnosztikája nagy nehézséget jelent mind a beteget kezelő orvos, mind a felmerült gyanút igazolni vagy eloszlatni szándékozó diagnózist meghozó orvos számára. A diagnózis felállításában szerepe van az EKG-nak, a thrombosis meglétét jelző laboratóriumi vizsgálatnak (D-dimer) (2, 9, 12, 14, 15, 16) és a különböző képalkotó diagnosztikai vizsgálatoknak.
A közelmúltban Bodrogi és munkatársai (1), Juhász és munkatársai (8), valamint jelen dolgozat szerzőinek egyike (13) részletesen foglalkozott a képalkotó diagnosztikai módszerek lehetőségeivel, a pulmonális embólia kimutatásában betöltött szerepükkel. Ismert tény az, hogy a bárhol elvégezhető mellkas röntgen vizsgálat érzékenysége, fajlagossága nem jó. Bizonyos aspecifikus jelek hívhatják fel a figyelmet a pulmonális embólia lehetőségére, például emelkedett rekeszállás, rekesz feletti atelectasiás csíkárnyék, kevés pleuralis folyadék. Egyes esetekben lokális hipovaszkularizáció ismerhető fel, vagy a pulmonális keringés súlyos beszűkülésének következtében a hilus érképleteinek kóros megjelenése, a jobb szívfél érintettségének jelei mutathatók ki (I, 9, 12, 14). E módszer, mint ahogy a mellkas CT-vizsgálat is kimutathat olyan eltérést, például pneumothoraxot, súlyos mellkasi aorta elváltozást (például dissectiót) stb., amelyek okai lehetnek a mellkasi panaszoknak.
A pulmonális embólia klasszikus vizsgálati módszere az angiográfia, amely igen érzékeny és magas specificitású módszer, de invazív (1, 9), jól képzett radiológiai munka-csoportot és jó felszerelést igényel, jellege miatt nem alkalmas szűrőmódszernek, az enyhébb esetek gyanújakor nem végezzük el. Napjainkban e módszer azonban biztonságosan alkalmazható és a kis érképletek állapota is tisztázható. Az angiográfia gyors és biztos diagnózist ad, valamint általa katéter terápia is végrehajtható (7).
Tankönyvi megállapításnak tekinthető, hogy a perfúziós (és lehetőség szerint a ventillációs) szcintigráfia eredménye alapvető a kórkép diagnosztizálásában, a szenzitivitás magas, elfogadható a specificitás. A (perfúziós) szcintigráfia mindig más módszer (például mellkas felvétel, inhalációs szcintigráfia) eredményének ismeretében ad korrekt diagnózist (1, 4, 5). E tárgykörben sokat idézik a PIOPED tanulmányt (3), amelyben több mint ezer tüdőembólia gyanúja miatt vizsgált beteg adatait tekintették át. A vizsgálatba bevont betegek szcintigráfián és többségükben angiográfián is átestek. A multicentrikus tanulmány eredményei azt mutatták, hogy amikor a kombinált szcintigráfiás vizsgálat eredménye a pulmonális embólia magas valószínűségét mutatta, angiográfiával igazolható volt a pulmonális érrendszer elzáródása. Normális, közel normális izotóp vizsgálati eredmény esetén igen nagy a valószínűsége annak, hogy nem áll fenn pulmonális embólia. Közbülső esetben az izotópdiagnosztika módszerei nem diagnosztikusak. Azóta a képalkotó módszerekben bekövetkezett fejlődés segítheti a klinikust a terápiás döntés meghozatalában. A spirál CT megjelenése óta a radiológusok kezében van egy olyan eszköz, amely gyorsan, a beteget kevéssé megterhelő módon, csak perifériás véna punkcióját igénylő invazivitással képes kimutatni a nagyobb érképletekben magát a thrombust (3. ábra), és idővel kisebb-nagyobb infarktusok is láthatóvá tehetők. Alkalmas a választott terápia eredményességének vizsgálatára is (1, 8, 10, 11). Harkányi és munkatársai 1995-ben megírt, a spirál CT sajátságait ismertető dolgozatukban utalnak arra, hogy az új módszer indikációs körébe tartozik a tüdőembólia is (17). A világirodalomban egy francia munkacsoport közölt az elsők között a spirál CT diagnosztikus szerepéről, a vizsgálattal kapcsolatos metodikai problémákról, csapdákról (10, 11). Nem szabad azonban megfeledkezni arról, hogy körülbelül egy évtizeddel a számítógépes rétegvizsgálat mint vizsgálati módszer leírása után már megjelentek közlemények arról, hogy az 1980-as évek mai szemmel igen lassú CT-készülékeivel is felismerhetőek voltak a tüdőembólia elsődleges, vaszkuláris eltérései, a másodlagos, a tüdő parenchymában jelentkező, kimutatható elváltozások (18, 19). Számos hazai radiológiai témájú közleményben olvashatunk e témával kapcsolatos tapasztalatokról (I, 8, 13) és néhány, a közelmúltban megjelent, a pulmonális embólia klinikumával, kezelésével kapcsolatos dolgozatban, összefoglaló referátumban szerepel e diagnosztikus módszer (2, 12). Ismerni kell a módszer sajátságait, azt, hogy a napjainkban használt CT-berendezésekkel a centrálisan elhelyezkedő, truncus pulmonalis ágaiban lévő, a segmentalis ágakban elhelyezkedő thrombus ismerhető fel. El kell kerülni a pulmonalis érképletek közvetlen közelében lévő, apró nyirokcsomók tévesen thrombuskénti interpretálását vagy a fal mellett elhelyezkedő krónikus embolizáció friss thrombembolizációkénti diagnosztizálását. Teljes egészében szakmai kérdés a vizsgálat paramétereinek helyes megválasztása, mint például a késleltetési idő optimális megállapítása, kis szeletvastagság, azaz kis kollimáció, a mérés caudocranial irányú megválasztása, a kontraszt-anyag beadási ütem megszokottnál nagyobb volta stb. Nevezhetők ezek „szakmai belügynek”, de azt a tüdőembóliára gyanús beteget kezelő klinikusnak is tudnia kell, hogy a vizsgálat lebonyolítása nem teljesen azonos egy általánosságban elvégzett mellkas CT-vizsgálatéval! Ezért fontos a radiológus és klinikus közötti jó kapcsolat, kommunikáció, a radiológusnak ismernie kell az anamnézist, a feltételezett diagnózist, diagnózisokat.
Most már hazánkban is természetes, hogy a CT-vizsgálatokat spirál vagy helikális (vagy a ritkábban használt jelzővel: volumetrikus) CT-berendezéssel végezzük el. A radiológus számára ismert, hogy a fejlett egészségügyi rend-szerekkel rendelkező országokban már nem a korszerűtlennek nevezhető egy-szeletes, azaz single-slice, hanem több-szeletes, multi-slice vagy multirow spirál CT-berendezések használatosak. Ezek annyiban térnek el az esetismertetésben szereplő CT-berendezéstől, hogy a röntgencső egyetlen kör-befordulásával 4, 8, vagy akár 16, 32 0,5-1-4 mm vastagságú szelet leképezésére alkalmas. A pulmonális embólia diagnosztikájával kapcsolatban ez azt jelenti, hogy igen rövid idő, néhány másodperc alatt 1-2 mm vastag metszeteket lehet készíteni az egész mellkas területén, ezáltal a kisebb erek is ábrázolhatók, igen diszkrét tüdő parenchyma eltérések is kimutathatók. Ráadásul nemcsak a mérés, az adatgyűjtés síkjában, hanem gyakorlatilag ugyanolyan minőségű síkokban rekonstruált metszetek nyerhetők e módszer által (21, 22).
Pulmonális embólia diagnosztizálása után a vérrög eredetének kimutatására számos módszer bevethető: alapmódszernek, "gold standard"-nek tekinthető az alsó végtagi angiográfia, amelyet egyre ritkábban végzünk el, helyette a Doppler UH-vizsgálat a preferált eljárás (1, 6). Az amerikai radiológus irodalomban ismert a mellkas CT-vizsgálat kiterjesztésének lehetősége, a kontrasztanyag beadása után, néhány perces késleltetési idővel végezve a metszetek készítését. Telődési hiány formájában ábrázolódik a comb, kismedence nagyobb vénáiban a thrombus (22). A mai, korszerű, gyors képalkotási idejű MRI-készülékek, hasonlóan a spirál CT-berendezésekhez, alkalmasak a nagyobb pulmonális erekben lévő vérrög kimutatására és természetesen a kismedencei vénás thrombosis kórismézésére. Az MRI kontrasztanyag adása nélkül DSA-hoz hasonló képi megjelenítést is lehetővé tesz (1, 23).
A tüdőembólia antikoaguláns, fibrinolitikus kezelésének részletei jól ismertek (2, 9, 12, 14). Az eset másik tanulsága az, hogy fibrinolitikus kezeléssel összefüggő szövődményre (vérzésre) hajlamosított betegek esetén gondolni kell a katéteres kezelés lehetőségére is. A mechanikus thrombus roncsolás, katéteres trombolízis részleteiről a nemzetközi radiológiai szakirodalomban olvashattunk (24-26), Boda a közelmúltban megjelent összefoglaló munkájában említi meg e speciális kezelési módot (12), Battyány és munkatársai közleményben számoltak be e kezelési móddal kapcsolatos tapasztalataikról (27), amelyek alapján a szelektív fibrinolitikus kezelés jó hatásfokú, kevés, nem súlyos szövődménnyel jár, a beteg részéről jól tolerálható, lehetőséget biztosít a tüdő perfúzió azonnali javítására és cava filter felhelyezésére.
A tüdőembólia diagnosztikájában előrelépést jelentő spirál CT-berendezések hazánkban is széles körben elterjedtek, igaz ugyan, hogy sok beteg csak mentőszállítással juthat el non-stop működő CT-laborba. Ezzel szemben a kevés vérzéses szövődményt okozó lokális kezelésre alkalmas radiológiai osztályok száma csekély, ahol katéter terápiában járatos munkacsoportok bármikor elérhetőek. Ebben kívánatos lenne az előrelépés, hogy napjaink magyar radiológusa ne csak a pulmonális embólia kórismézésében kapjon a korábbinál nagyobb szerepet, hanem az intervenciós radiológiai módszerekkel a beteg kezelésében is!
Irodalom
- Bodrogi N., Baranyai T., Vargha A., Radics Zs., Mészáros Á. és mtsaik.: Lehetőségek a tüdőembólia diagnosztikájában a modern képalkotás birtokában. Magyar Radiológia, 74: 35-44. (2000).
- Boda Z.: Az akut pulmonalis embolia diagnosztikája és te¬rápiája. Orvosi Hetilap, 145: 967-969. (2004).
- PIOPED Investigators: Value of the ventilation/perfusion scan in acute pulmonary embolism: result of the prospective investigation of pulmonary embolism diagnosis (PIOPED). JAMA, 263: 2753-2759. (1990).
- Worsley, D. F., Alavi, A.: Radionucleide Imaging of Acute Pulmonary Embolism. Rad. Clin. N. Am., 39: 1035-1052. (2001).
- Nemessányi Z.: A tüdőszcintigráfiás eredmények értékelése. Medicina Thoracalis, 52: 158-160. (1999).
- Battyány l., Harmat Z., Rostás T., Horváth L., Nijatti M., Erményi Á., Gasztonyi B., Schubert J.: Az alsó végtagi duplex szonográfia értéke a mélyvénás trombózis diagnosztikájában és a tüdőembólia kockázatának megítélésében. Medici-na Thoracalis, 52: 161-165. (1999).
- Battyány I., Horváth L., Harmat Z., Rostás T., Erményi Á., Gasztonyi B., Sárosi 1.: A pulmonális angiográfia mint a tüdőembólia diagnosztikájának „gold standard"-je. Medicina Thoracalis, 52: 166-170. (1999).
- Juhász E., Vadon G.: A hagyományos és HRCT jelentősége pulmonális embóliában. Medicina Thoracalis, 52: 171-174. (1999).
- Sárosi l.: A nagy kiterjedésű pulmonális embólia diagnózisa és intenzív terápiás kezelése. Medicina Thoracalis, 52: 175-178. (1999).
- Remy-Jardin, M., Remy, J., Wattinne, L., Giraud, F.: Central Pulmonary Thrombembolism: Diagnosis with Spiral Volumetric CT with the Single-Breath-Hold Technique — Comparison with Pulmonary Angiography. Radiology, 185: 381-387. (1992).
- Remy-Jardin, M., Remy, J., Deschildre, F., Dominique, A., Beregi, J. P., Hossein-Foucher, C., Marchandise, X., Du¬hamel, A.: Diagnosis of Pulmonary Embolism with Spiral CT: Comparison with Pulmonary Angiography and Scin¬tigraphy. Radiology, 200: 699-706. (1996).
- Boda Z.: Újabb lehetőségek az akut pulmonalis embolia diagnosztikájában és terápiájában. Orvosi Hetilap, 143: 2717-2721. (2002).
- Weninger Cs., Hegedüs K., Csere P.: Radiológiai módszerek a pulmonális embólia diagnosztikájában, kezelésében. Magyar Mentésügy, 22: 21-29. (2002).
- Mühl D., Sárosi I., Udvaros E.: Nagy kiterjedésű tüdőembólia tünetei, diagnosztikája és sürgősségi ellátása. Magyar Mentésügy, 24: 23-35. (2004).
- Gál É., Litter I.: A D-dimer vizsgálatok helye és szerepe a pulmonális embólia elkülönítő diagnosztikájában. Medici-na Thoracalis, 52: 152-154. (1999).
- Radnai B., Goják 1., Pintér T., Bódis L.: Az EKG és az echokardiográfia szerepe a tüdőembólia diagnosztikájában. Medicina Thoracalis, 52: 155-157. (1999).
- Harkányi Z., Balázs Gy., Hrabák K., Arany A.: Spirál CT: új radiológiai módszer a régi alapokon. LAM, 5: 426-433. (1995).
- Breatnach, E., Stanley, R. J.: CT Diagnosis of Segmental Pulmonary Artery Embolus. J. of Comput. Assist. Tomogr., 8: 762-764. (1984).
- Chintapalli, K., Kristin Thorsen, M., Olson, D. L., Goodmann, L. R., Gurnly, J.: Computed Tomography of Pulmonary Thrombembolism and Infarction. J. of Comput. Assist. Tomogr., 12: 553-559. (1988).
- Schoepf, U. J., Kessler, M. A., Rieger, C. T, Herzog, P., Klotz, E., Wiesgigl, S., Becker, C. R., Exarhos, D. N., Rei¬ser, M. F.: Multislice CT imaging of the pulmonary embo¬lism. Eur. Radiol., 11: 2278-2286. (2001).
- Schoepf, U. J., Holzknecht, N., Helmberger, T. K., Crispin, A., Hong, C., Becker, C. R., Reiser, M. F.: Subsegmental Pulmonary Embolism: Improved Detection with Thin-Collimation Multi-Detector Row Spiral CT. Radiology, 222: 483-490. (2002).
- Katz, D. S., Loud, P. A., Bruce, D., Gittleman, A. M., Mueller, R., Klippenstein, D. L., Grossman, Z. D.: Combined CT Venography and Pulmonary Angiography: A Comprehensive Review. RadioGraphics, 22: S3-S24. (2002).
- Gupta, A., Frazer, C. K., Ferguson, J. M., Kumar, A. B., Davis, S. J., Fallon, M. J., Morris, I. T., Drury, P. J., Cala, L. A.: Acute Pulmonary Embolism: Diagnosis with MR Angiography. Radiology, 210: 353-359. (1999).
- Vujic, 1., Young, J. W. R., Gobien, W. T, Dawson, W. T, Liebscher, L., Shelley, B. E.: Massive Pulmonary Embolism: Treatment with Full Heparization and Topical Low-Dose Streptokinase. Radiology, 148: 671-675. (1983).
- Rocek, M., Peregrin, J., Velimsky, T.: Mechanical thrombectomy of massive pulmonary embolism using an Arrow-Trerotoloa percutaneous thrombolytic device. Eur. Radiol., 8: 1683-1685. (1998).
- Schmitz-Rode, T., Janssens, U., Hanrath, P., Günther, R. W.: Fragmentation of massive pulmonary embolism by pigtail rotation catheter: possible complication. Eur. Ra¬diol., 11: 2047-2049. (2001).
- Battyány I., Horváth L., Sárosi I., Nemessányi Z., Enyezdi J.: Lokális fibrinolyticus kezelés szubtotális tüdőembóliában. Orvosi Hetilap, 140: 873-879. (1999).
Érbetegségek: 2005/1. 3-8. oldal