Számos kísérletes és humán vizsgálat eredménye valószínűsíti, hogy cardiovascularis betegségekben a myocardialis endothelin-1 produkció növekedése szerepet játszhat a coronaria rendszer kóros válaszaiban és az ischaemiás szöveti károsodás fokozódásában. Kísérleteinkben az ET-1 coronariahatás jellemzőit vizsgáltuk in situ kutyaszíven, művileg előidézett regionális myocardialis ischaemiában az ép vérellátású és ischaemiás területek válaszreakcióinak elemzésével három kísérleti csoportban a coronaria volumenáramlás (I., II.), a perifériás (retrográd) coronarianyomás (I.), az áramlásfüggő epicardialis hőemisszió (II.) és a coronaria rezisztencia (III.) mérése útján. Az eredmények szerint a coronaria rendszerbe juttatott ET-1 közel egyforma mértékben szűkíti a normál vérellátású és az ischaemiás myocardium ereit. Korábbi adataink alapján valószínűsíthető, hogy ennek a jelenségnek hátterében a kompenzatorikus vasodilatátor nukleozidok coronaria hatásának csökkenése áll. Az ET-1 ép és ischaemiás szívizomban egyaránt kifejtett, szokatlanul hatékony coronaria effektusa felhívja a figyelmet az endogén ET-1 egyes cardialis kórállapotokban való fokozott felszabadulásának patofiziológiai szerepére mind a kompenzációs mechanizmusok csökkent hatékonysága, mind a technikailag sikeres revascularisatiós beavatkozások funkcionális elégtelensége terén.
Érbetegségek: 2007/1. 57-61. oldal
KULCSSZAVAK
endothelin-1 coronaria vasoconstrictio, myocardialis vérellátás, regionális ischaemia
Bevezetés
Az endothelin peptidcsalád legerőteljesebb vascularis hatással bíró tagja az endotelin-1 (ET-1) különösen jelentős, az eddig ismert endogén vasoconstrictor ágenseknél nagyobb és tartósabb érszűkítő hatást képes kiváltani számos érterületen, beleértve a coronaria rendszert is (1). Az ET-1 valószínű szerepét a coronaria betegség több típusában, így akut coronaria syndromában (2), PTCA utáni myocardialis stunning alatt (3) és korai restenosis után (4), ischaemiás cardiomyopathiában (5) számos oldalról alátámasztották. Kimutatták, hogy myocardialis ischaemiában (6) és más cardiovascularis kórképekben is (7) nő az ET-1 produkció, amit az emelkedett plazmaszintek is jeleznek (8, 9). A szisztémás vérben mérhető koncentrációknál azonban az endothelin-1 jóval magasabb szöveti koncentrációt érhet el a myocardiumban, ami részben (az endotheliális képződés mellett) a szívizomsejtek általi termelődéséből részben endothelsejtekből való abluminális leadódásából eredeztethető. Erre utalnak azok az eredmények, amelyek szerint az ágensnek mind a humán kamrai szövetmintákban mért mennyisége (10), mind pedig a természetes úton képződő myocardialis transsudatumban, a pericardialis térben levő folyadékban mért koncentrációja - hasonlóan jónéhány más szíveredetű anyaghoz - a plazmaértékeket jelentősen, szignifikánsan meghaladja (11, 12). Ezen túlmenően ischaemiás szívben a szöveti ET-1 koncentráció jelentős inhomogenitást mutat: az ágens képződése szignifikánsan nagyobb a károsodott vérellátású myocardiumban, mint az ép vérellátású területeken (13).
Felmerül tehát a kérdés, hogy a megemelkedett ET-1 szintek milyen hatást fejtenek ki a regionálisan ischaemiás szív különböző területein, és milyen szerepe van e válaszok módosulásában a myocardialis kompenzációs mechanizmusoknak. Ezért kísérletesen előidézett a. coronaria (LAD) occlusio mellett vizsgáltuk az intracoronariasan (i.c.) adott endothelin-1 volumenáramlásra és szöveti vérellátásra, valamint szívműködésre kifejtett hatásait in situ kutyaszíven.
Anyag és módszer
A vizsgálatokat 26, pentobarbitallal (30 mg/kg, i.v.) altatott, nyitott mellkasú kutya szívén végeztük, három kísérleti csoportban.
I. Az első csoportban az endothelin-1 dózis-hatás összefüggéseket a volumenáramlással (elektromágneses áramlásmérő, Statham SP2202) jellemeztük a LAD coronaria artéria középszakaszú occlusiója előtt és után, mikor is a teljes LAD véráramlás és az occlusio után, attól proximalisan mérhető ún. residualis (az ischaemiás régió táplálását szolgáltató collateralis) beáramlás változásait vetettük össze, míg az ischaemiás terület érreakcióit a retrográd coronaria nyomás mérése útján követtük.
II. Ugyanilyen preparátumon a volumenáramlás mérések mellett a szívszöveti vérellátás és véreloszlás szemikvantitatív vizsgálatát végeztük computeres cardiothermográfiával (AGA 750 Thermovision), és a folyamatosan rögzített felvételeken a LAD artéria ellátási területéhez tartózó ischaemiás és nem-ischaemiás régiókat, valamint az occlusio által nem érintett jobb kamrai területek áramlásfüggő hőemisszióját értékeltük.
III. A harmadik csoportban a LAD artéria izolált (carotico-coronaria) perfusiója mellett négy konstans áramlási szinten, normo-, hipo- és hiperperfundált (Masterflex roller pumpa) érrendszerben vizsgáltuk az i.c. Et-1 hatását a perfusiós nyomásértékekből (elektromanométer, SP 23Db) számított érellenállás-változások követése révén.
Az endothelin-1 emelkedő bólusait a coronaria érbe szúrt vékony (26 Ga) tűn keresztül (I. és II. csoport), illetve közvetlenül a perfúziós rendszerbe (III.) adtuk. A kísérletek során folyamatosan mértük a szisztémás nyomást (a. femoralis) és a szívfrekvenciát, valamint az I. csoportban a bal kamrai kontraktilitás változásait (Walton-Brodie strain gauge).
Az adatokat átlag SEM formában adtuk meg, a statisztikai értékelés Student t teszttel végeztük, szignifikáns eltérésnek fogadva el a p
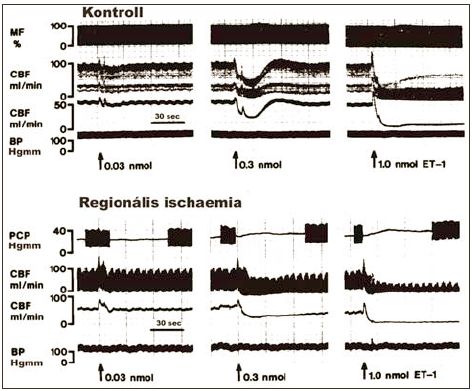
1. ábra.
Intracoronariasan adott endothelin-1 (ET-1) hatása a coronaria áramlásra ép vérellátás mellett (felül) és regionális myocardialis ischaemiában (alul). Eredeti regisztrátumok. Jelölések: MF - regionális kontrakciós erő a LAD artéria ellátási területén mérve, CBF (felső panel) - coronaria áramlás (LAD) pulzatórikus és közép-értékeinek görbéi, BP - artériás nyomás, PCP - perifériás (retrográd) coronaria nyomás a LAD artéria középszakaszú occlusiójától disztálisan mérve, CBF (alsó panel) - a coronaria áramlás a LAD occlusiótól proximálisan mérve (residualis áramlás). Magyarázat a szövegben. Fig. 1. Effect of the intracoronarially administered
Eredmények
Az i.c. ET-1 dózis-hatás összefüggéseket az ágens 0,01- 1,0 nmol dózisainak adásával vettük fel. Az ET-1 a vérnyomás, a szívfrekvencia és a kontraktilitás változatlansága mellett jellegében és mértékében azonos mérvű csökkenést idézett elő a volumenáramlásban kontroll körülmények között és regionális ischaemiában (1. ábra), azzal a kis különbséggel, hogy a residualis áramlás restitúciója az ET-1 közepes dózisainál elnyújtottabbnak bizonyult. Az ET-1 hatás maximumán (1,0 nmol) a normál coronaria áramlás kiindulási értékének tizedére esett viszsza (9,3%) és a vasoconstrictiót sosem követte kompenzatorikus (hyperaemiás) értágulat. További jellegzetesség, hogy - amint az a hatások időbeliségének értékeléséből kitűnik - egy kritikus ET-1 dózis (0,3 nmol) adása felett az érválasz tartós, kompenzálatlan vasopasmusba torkollott (2. és 3. ábra).
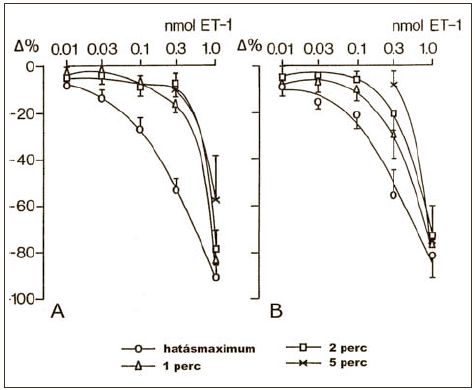
2. ábra.
ET-1 coronaria dózis-hatás összefüggések és a hatások időbeli változása normál vérellátás esetén (teljes LAD áramlás, A) és regionális ischaemiában (residualis áramlás, B). Adatok: coronariavolumen áramlás relatív változása, átlagértékek SEM, n = 8-11, p<0,01 valamennyi hatásmaximum értékre, p<0,02 a residualis áramlás 1-5 perces értékeire >0.1 nmol ET-1 dózisoknál.
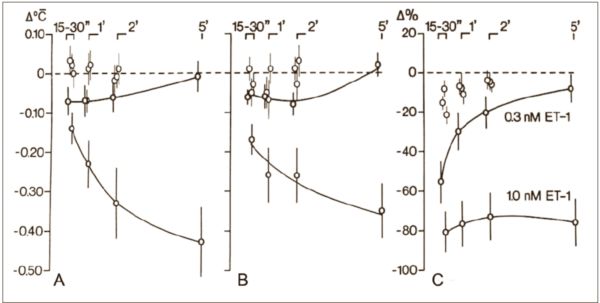
3. ábra.
Az ET-1 hatás időgörbéi ischaemiás és nem ischaemiás bal kamrai régiókban: a thermográfiás adatok (normál, A és ischaemiás, B régiók), valamint a residualis volumenáramlási adatok (C) parallel változásai. Különálló szimbólumok: <0,3 nmol ET-1 dózisokra kapott változások. Átlagértékek SEM, n = 8-11, p<0,01 a hőemisszió adatokra és p<0,001 a residualis áramlás értékeire az 1.0 nmol ET-1 hatásgörbén.
A LAD artéria lezárása után adott i.c. ET-1 az ischaemiás (collateralis beáramlástól függő) és az occlusiótól proximalisan lévő (a collateralis áramlást szolgáltató) területek vérellátását (áramlásfüggő hőemisszióját), valamint az ugyanitt mérhető residualis volumenáramlást hasonlóképpen csökkentette (3. ábra). Ugyanakkor a lezárt coronaria ágban mért perifériás coronaria nyomás értéke emelkedett (4. ábra), ami az ischaemiás terület ereinek ET-1-re adott direkt constrictor válaszát jelzi, és az ischaemiás régió hűlésével együtt arra utal, hogy az e területen egyébként jellemző értágulat nem képes mérsékelni az ET-1 által kiváltott coronaria szűkület mértékét.
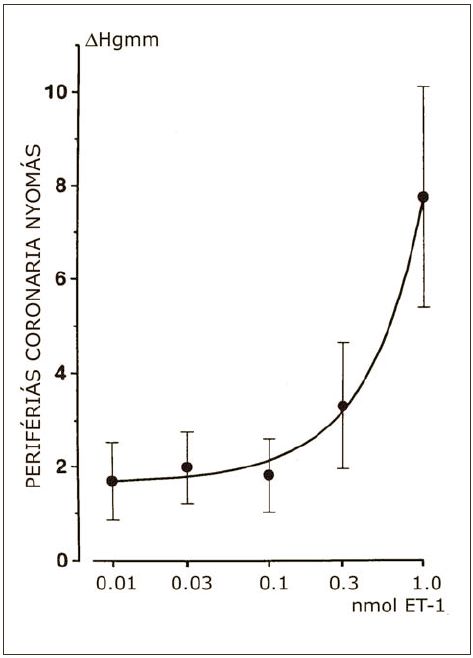
4. ábra.
Az ET-1 hatása a LAD occlusio helyétől disztálisan mérhető perifériás coronaria nyomásértékekre. Átlagértékek SEM, n = 6, p<0,05 az 1,0 nmol ET-1 adására utáni nyomásnövekedésre.
A művileg beállított áramlási szinteken perfundált coronaria rendszerben kapott érellenállás változások adatai (Rmax: +59, 16%) is megerősítették, hogy a hypoperfundált vasculatura is jelentős mértékben megőrzi ET-1 válaszkészségét (5. ábra).
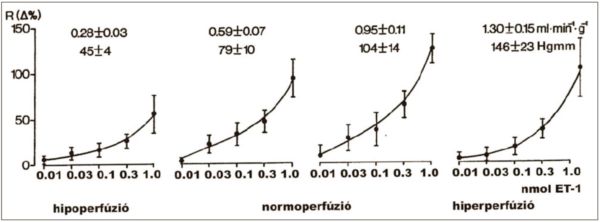
5. ábra.
Az ET-1 által kiváltott relatív vascularis rezisztencia növekedés a művi coronaria perfúzió különböző szintjein. A feltüntetett számok a coronaria áramlás és a hozzátartozó perfúziós nyomásértékeket mutatják. Átlagértékek SEM, n = 6, p<0,05 a <0,1 nmol ET-1; p<0,01 a 0,1 nmol ET-1 és p<0,001 a >0,1 nmol ET-1 dózisokra kapott válaszokban.
Megbeszélés
Korábbi megfigyelésekkel (1) összhangban vizsgálataink eredményei megerősítik a coronaria vasculatura igen nagy endothelin-1 érzékenységét. Jelen vizsgálatainkban kimutattuk, hogy az ET-1 i.c. adása során teljes vasoconstrictor dózis-hatás görbét ír le, és hogy az érszűkítő hatás a myocardialis kompenzatorikus mechanizmusok aktivációja mellett is érvényre jut. Ezt igazolja a coronaria szűkület tartós fennmaradása, vagyis az ET-1 hatás mértékének és időtartamának ugrásszerű fokozódása a peptid nagyobb dózisainak i.c. bevitelénél, a collateralis beáramlástól függő ischaemiás régiók erőteljes vasoconstrictor válasza ET-1 adására, valamint a számottevő mértékben megtartott ET-1 tónusfokozódás a hypoperfundált coronaria ereken.
Az ET-1 vasoconstriktor effektusának szokatlan hatékonysága hátterében - legalábbis jelentős részben - a metabolikus kompenzációs mechanizmusok gátlása áll. Korábbi vizsgálatainkban kimutattuk, hogy normál vérellátás mellett az ET-1 hatásra csökken a myocardium metabolikus válasza (az akut coronaria occlusióra fellépő reaktív hyperaemia), míg a kompenzációs értágulat túlnyomó hányadáért felelős vasodilatátor adenin nukleozidok (adenozin és inozin) szívszöveti felszabadulása fokozódik (14). Következésképpen az ET-1 reaktív hyperaemia választ korlátozó hatása nem a transzmitter felszabadulás gátlásán keresztül valósul meg. A másik lehetőség a coronaria rendszer ET-1 hatására kialakuló adenin nukleozidok iránti csökkent érzékenysége. Erre utal az a megfigyelésünk, mely szerint az adenin nukleozid kiváltott coronaria vasodilatációt közvetítő KATP membráncsatornák specifikus gátlószerrel (glibenklamid) való blokkolásával hasonlóképpen csökkenthető a reaktív hyperaemia válasz, mint az ET-1 esetén, miközben az adenin nukleozid produkció nő; a két szer egymás melletti alkalmazása esetén pedig jelentős hatástani átfedés észlelhető (14). Más szóval a KATP-csatorna blokkoló glibenklamid és az ET-1 valamely közös intracelluláris mechanizmuson osztozik a nukleozidok által kiváltott vasodilatatio csökkentésében. Feltételezhető, hogy az ET- 1 fenti hatásai az ischaemiás myocardiumban akár fokozottan érvényesülnek a coronaria dilatátor rezerv kihasználtsága és a coronaria reaktivitás károsodása miatt.
Összefoglalva, a coronaria rendszerbe juttatott ET-1 nem csak a normál vérellátású myocardium ereit szűkíti, hanem gyakorlatilag ugyanolyan mértékben képes korlátozni az ischaemiás régiók véráramlását is, mivel számottevően csökkenti a kompenzatorikus vasodilatátor nukleozidok coronaria hatását. Ez magyarázatot adhat az ET-1 szokatlanul hatékony coronaria hatásaira ép vérellátású és ischaemiás szívizomban egyaránt, és felhívja a figyelmet az endogén ET-1 ischaemiás myocardiumban való fokozott felszabadulásának és lokális coronaria hatásainak valószínű patofiziológiai szerepére mind a kompenzációs mechanizmusok csökkent hatékonysága és az ischaemiás károsodás következményes fokozódása, mind a revascularisatiós beavatkozások elégtelensége, a "no-reflow" jelenség terén.
Irodalom
- Rubanyi G.M., Polokoff M.A.: Endothelins: molecular biology, biochemistry, pharmacology, physiology, and pathophysiology. Pharmacol. Rev. 46: 325-415. (1994).
- Noll G., Luscher T.F.: The endothelium in acute coronary syndromes. Eur. Heart J. 19(Suppl C): C30-38. (1998).
- Lanza G.A.., Shaw S., Romagnoli E., Gioia D., Burzotta F., Trani C., Mazzari M.A., Mongiardo R., De Vita M., Rebuzzi A.G, Luscher T.F., Crea F.: Endothelin-1 and acute myocardial infarction: a no-reflow mediator after successful percutaneous myocardial revascularization. Eur. Heart J. 27: 1793-1798. (2006).
- Takase H., Sugiyama M., Nakazawa A., Toriyama T., Hayashi K., Goto T., Sato K., Ikeda K., Ueda R., Dohi Y.: Increased endogenous endothelin-1 in coronary circulation is associated with restenosis after coronary angioplasty. Can. J. Cardiol. 19: 902-906. (2003).
- Schmitz-Spanke S., Schipke JD.: Potential role of endothelin-1 and endothelin antagonists in cardiovascular diseases. Basic. Res. Cardiol. 95: 290-298. (2000).
- Serneri G.G., Cecioni I., Vanni S., Paniccia R., Bandinelli B., Vetere A., Janming X., Bertolozzi I., Boddi M., Lisi G.F., Sani G., Modesti P.A.: Selective upregulation of cardiac endothelin system in patients with ischemic but not idiopathic dilated cardiomyopathy: endothelin-1 system in the human failing heart. Circ. Res. 86: 377-385. (2000).
- Schiffrin E.L.: Role of endothelin-1 in hypertension and vascular disease. Am. J. Hypertens. 14: 83S-89S. (2001).
- Wieczorek I., Haynes W.G., Webb D.J., Ludlam C.A., Fox K.A.: Raised plasma endothelin in unstable angina and non-Q wave myocardial infarction: relation to cardiovascular outcome. Br. Heart J. 72: 436-441. (1994).
- Setsuta K., Seino Y., Tomita Y., Nejima J., Takano T., Hayakawa H.: Origin and pathophysiological role of increased plasma endothelin-1 in patients with acute myocardial infarction. Angiology. 46: 557-565. (1995).
- Zolk O., Quattek J., Sitzler G., Schrader T., Nickenig G., Schnabel P., Shimada K., Takahashi M., Bohm M.: Expression of endothelin-1, endothelin-converting enzyme, and endothelin receptors in chronic heart failure. Circulation 99: 2118-2123. (1999).
- Horkay F., Laine M., Szokodi I., Leppaluoto J., Vuolteenaho O., Ruskoaho H., Juhasz-Nagy A., Toth M.: Human pericardial fluid contains the highest amount of endothelin-1 of all mammalian biologic fluids thus far tested. J. Cardiovasc. Pharmacol. 26: S502-504. (1995).
- Namiki A., Kubota T., Fukazawa M., Ishikawa M., Moroi M., Aikawa J., Ebine K., Yamaguchi T.: Endothelin-1 concentrations in pericardial fluid are more elevated in patients with ischemic heart disease than in patients with nonischemic heart disease. Jpn. Heart J. 44: 633-644. (2003).
- Zeiher A.M., Ihling C., Pistorius K., Schachinger V., Schaefer HE.: Increased tissue endothelin immunoreactivity in atherosclerotic lesions associated with acute coronary syndromes. Lancet 344: 1405-1406. (1994).
- Fazekas L., Szabo T., Barat E., Huszar E., Kekesi V., Juhasz- Nagy A.: Compensation of endothelin-1-induced coronary vasoconstriction. J. Cardiovasc. Pharmacol. 31: S106-108. (1998).
Dr. Kékesi Violetta
Ér- és Szívsebészeti Klinika
1122 Budapest, Városmajor u. 68.
Érbetegségek: 2007/1. 57-61. oldal