Az antiphospholipid antitestek jelenléte artériás és vénás thromhosisok kialakulására hajlamosít. A thrombosis valamennyi szervben kialakulhat, számos klinikai manifesztációi észleltek antiphospholipid antitestekkel kapcsolatban, ezért a haematológián kívül a medicina csaknem minden ágában gondot okozhat az antiphos- pholipid-syndroma.
Érbetegségek: 1995/3. 9-13. oldal
KULCSSZAVAK
antiphospholipid antitest, lupus anticoagulans, anticardiolipin antitest
Az antiphospholipid antitestek (APA-ek) klinikai jelentősége az utóbbi években egyre nyilvánvalóbbá vált. Az ismeretek gyarapodásával azonban a téma is egyre bonyolultabb lett, és ma már szinte áttekinthetetlen irodalom foglalkozik vele. Az első hazai közlés egy fiatal lány multiplex thromboembóliái kapcsán a mi munkacsoportunktól származik (1), és a fiatalkori thrombosisok vizsgálata során számos esetben volt alkalmunk azóta is az APA jelenlétét igazolni. Jelen közleményünkben elsősorban az angiológiai vonatkozások szempontjából kívánjuk a kérdést összefoglalni, a patofiziológiai, laboratóriumi diagnosztikai, illetve az egyéb vonatkozásokat csak röviden érintjük, amennyiben azok a megértéshez szükségesek. Az egyéb vonatkozásokat illetően utalunk a hazai és külföldi irodalomban nemrég megjelent összefoglaló közleményekre (2, 3).
Az APA fogalmi meghatározása
Az antiphospholipid antitest elnevezés tulajdonképpen gyűjtőfogalom, mert különböző immunglobulinokat (IgG, ritkábban IgM, IgA) sorolunk e kategóriába, amelyek közös jellemzőije azonban az, hogy egy vagy több, elsősorban negatív töltésű phospholipid struktúra ellen irányulnak (4). Ezek a phospholipidek jelentős szerepet játszanak a véralvadás folyamatában, így nem meglepő, hogy az ellenük ható antitestek a haemostasis zavarát idézik elő. Ma már csak történeti érdekessége van az eredeti elnevezésnek, a "lupusanticoagulant"-nak, mivel systemás lupus erythematodes kapcsán ismerték fel először (5), és az alvadási tesztek (elsősorban a partialis thromboplastin idő) megnyúlása miatt véralvadási inhibitornak gondolták. Hamar kiderült az is, hogy egyes esetekben a lues-tesztek, melyek cephalint használnak a reagensekben, álpozitív reakciókat adnak, vagyis ilyenkor anticephalin tulajdonságú antitestek képződnek (6). Más esetekben más phospholipid struktúrák (phosphatidilserin, phosphatidil-inozitol stb.) ellen képződnek az ellenanyagok. A különböző antigénekkel szemben termelődött különböző antitestek messzemenően magyarázzák azt a heterogenitást, amely a patofiziológiai részleteket jellemzi.
Mivel a különböző phospholipidek a haemostasis bonyolult rendszerében sok helyütt fontos szerepet játszanak, nem meglepő, hogy mind az érfal, mind a vérlemezkék, illetve a véralvadás különböző aktivációs lépéseinél találtak eltéréseket, amelyeket az APA jelenlétére vezettek vissza (7).
A gyakorlat számára tehát úgy összegezhetjük, hogy az APA-ek olyan immunglobulinok, amelyek különböző phospholipid struktúrák ellen termelődnek, és ezáltal a haemostasis-rendszerben zavart, elsősorban thrombosist, vagy ritkán - hypoprothrombinaemia (8) és thrombopathia (9) kapcsán - vérzékenységet hoznak létre.
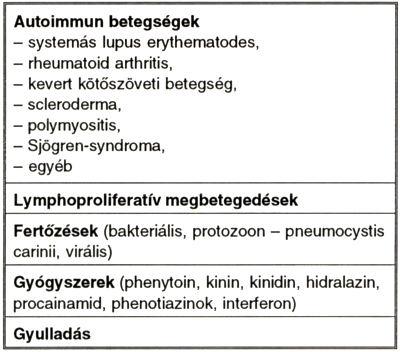
I. táblázat.
Megbetegedések, amelyekhez AP-syndroma társulhat.
Az APA által kiváltott klinikai tünetek
Mielőtt a klinikai részletekre térnénk, először azt kell megjegyeznünk, hogy az APA megjelenése történhet minden egyéb megbetegedés nélkül, azonban gyakoribb az, hogy valamely más, rendszerint autoimmun megbetegedés kapcsán képződik. Az előbbi esetben primer, az utóbbi esetben secunder antiphospholipid syndromáról beszélünk (6). Az I. táblázat mutatja a különböző megbetegedéseket, amelyekhez AP-syndroma társulhat.
Nyilvánvaló, hogy az AP-syndroma tünetei a secunder megjelenési formákban társulnak az alapbetegséghez, azonban azokban az esetekben, ahol ilyen alapbetegség nincsen, a meglehetősen jellegzetes tünetek alapján gondolhatunk az APA-ek pathogen szerepére.
Az AP-syndroma kiemelkedően jellegzetes tünete a thrombosis. Ez rendszerint az alsó és a felső végtag mélyvénáiban lép fel, amely tüdőembóliát okozhat. Az alsó végtagi thrombosis már fiatal korban is súlyos chronicus vénás insufficienciára vezethet, ha a kórképet nem diagnosztizálják időben, és nem kezdik el a megfelelő kezelést.
Mivel a thrombosis nemcsak a végtagokban és vénákban, hanem artériákban és a keringés más helyein is felléphet, ezért a medicina csaknem minden ágában gondot okozhat az AP-syndroma.
így a neurológiában az intracranialis artériákban, vagy a sinusokban fellépő thrombosis magyarázatát adhatja az APA kimutatása (10).

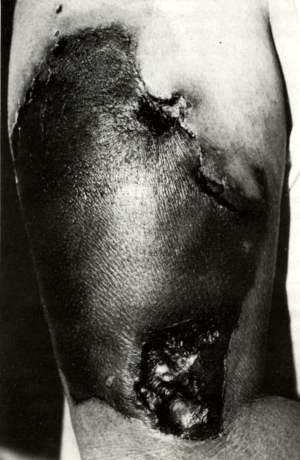
1. ábra.
AP-syndromában fellépő bőrnekrózis. A jobb oldali glutealis régióban már gyógyult formában, alatta a comb dorsalis felszínén egy kezdődő nekrotikus folyamat képét láthatjuk.
A vénás thrombosisnak fiatal korban artériás thrombosissal való társulása differenciál-diagnosztikai jelentőségű lehet; a veleszületett thrombosis-hajlam (thrombophilia) okai közül szinte kizárólag csak a protein S hiányra jellemző a vénás és artériás thrombosis társulása. Fiatal betegben fellépő myocardialis infarctus oka lehet az APA által kiváltott coronaria thrombosis. Azt is megfigyelték, hogy a coronaria betegségben végzett bypass műtétek késő eredményét rontja az APA jelenléte, mert ilyen esetekben gyorsabban bekövetkezik a graft elzáródása (11).
Vannak, akik a thrombosis megjelenési formájától függően alcsoportokat különböztetnek meg, mondván, hogy egyes esetekben csak a vénás, máskor meg csak az artériás thrombosisok jellemzőek. Saját tapasztalatunk ennek ellene szól. Egyik betegünkben a 15 éves korban fellépő első vénás thrombosist követően 15 év múlva, a beteg 30. életévében alakult ki mellsőfali myocardialis infarctus.
A retina ereinek (artériák és vénák egyaránt) elzáródását magyarázhatja az APA syndroma, de a veseerek, tüdőartériák, májvénák (Budd-Chiari syndroma) elzáródását is észlelték (12).
Az APA syndroma másik fő jellegzetessége, amely azonban nem mindig alakul ki, a thrombocytopenia (6). A chronicus ITP kb. harmadában lehet az APA jelenlétét igazolni (13).
Meglehetősen sajátságos tünete még az AP-syndromának a fiatal nőbetegekben a terhesség különböző szakaszaiban fellépő spontán abortus, illetve koraszülés (14). Ezekben az esetekben az érelzáródás a méhlepényben következik be, és vezet a magzat elhalásához. Ha a betegnek előzőleg thrombosisa is volt, könnyű az AP-syndromára gondolni, azonban gyakran egyedüli tünete az AP-syndromának!
Az APA olykor, szerencsére ritkán, különleges, súlyos tüneteket okoz. Ezek közül az egyik a bőrnekrózis (15). Saját betegeink között három ilyen esetet láttunk. Ezek közül az egyik esetet mutatja az 1. ábra, másik betegünkről készült a 2. és 3. ábra.
2. ábra.
AP-syndromában fellépő symmetrikus bó'rnekrózis. A betegnek, akinek anamnézisében évek óta tartó arthritises panaszok, májlaesio, magas vérnyomás betegség szerepelt, lázas infekció kapcsán jelentkezett mindkét karján a progrediáló bőrnekrózis. Képünkön a beteg jobb karja. Tünetei hátterében laboratóriumunkban lupus anticoagulans jelenlétét igazoltuk.
Jellegzetes bőr (livedo reticularis) és neurológiai (ischaemias cerebrovascularis) tünetek együttese a Sneddon által 1956-ban leírt syndroma, melynek hátterében szintén APA- ek jelenléte állhat (16). Hazánkban is közöltek ilyen esetet (17).
Ugyancsak ritkán fordul elő, de fatalis kimenetelű a kiterjedt, hirtelen kialakuló occlusív vasculopathia (18), melyben az autopsia során nem lehet a vasculitisre jellemző elváltozásokat kimutatni, hanem az APA-val hozzák összefüggésbe, és a DIC-től, illetve a TTP-től is elkülöníthető.
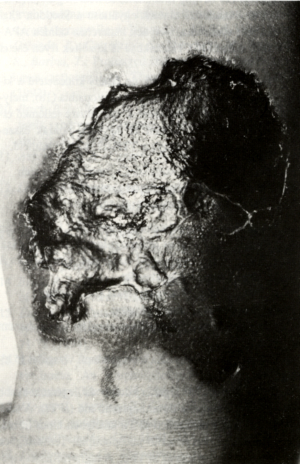
3. ábra.
Ugyanezen beteg bal karja.
Az antiphospholipid antilestek laboratóriumi kimutatása
A laboratóriumi vizsgálatoknak alapvetően két irányban kell történniük: első a lupus anticoagulant (LA) kimutatása, a második az antiphospholipid antitestek kimutatása. A diagnózis kritériumai a következők:
- phospholipid-függő alvadási teszt kóros volta;
- a kóros eltérést inhibitor okozza;
- az inhibitor nem egy specifikus alvadási faktor, hanem phospholipid ellen irányul.
A fentiekből következnek a laboratóriumi vizsgálat fő lépései (19):
- Szűrő tesztek. A legelterjedtebb és legérzékenyebb teszt az aktivált partialis thromboplastin idő (aPTI). A kaolin idő (KCT) egy módosított aPTI, amelyben nincs hozzáadott thrombocyta helyettesítő phospholipid. Terhességben érzékenysége meghaladja az aPTI-ét. A hígított Russel viperaméreggel mért alvadási idő (dRVVT) jól alkalmazható szűrő és megerősítő tesztként is. Fontos figyelembe venni azt a tapasztalaton alapuló szabályt, hogy legalább két különböző szűrőtesztet kell alkalmazni a LA kizárására.
- Keveréses (korrekciós) tesztek. Céljuk az inhibitor jelenlétének bizonyítása és az alvadási faktorhiány kizárása. A vizsgálat lényege, hogy a beteg plazmájához normál plazmát adunk különböző arányokban, és próbáljuk korrigálni a megnyúlt aPTI-t. Az inhibitor kimutatásának sine qua non- ja a korrekció elmaradása a keveréses tesztben.
- Megerősítő tesztek. Két elven alapulnak. Az első megközelítésben a phospholipid mennyiséget csökkentjük, így az inhibitor hatás jobban érvényesül. Erre legalkalmasabb a hígított thromboplastin idő. A második megközelítésben növeljük a phospholipid mennyiséget, így eltöröljük az inhibitor hatást, az eredmény normalizálódik. Ilyen teszt a thrombocyta neutralizációs procedúra (PNP).
Ott, ahol a klinikai kép szuggesztív, már a szűrő lépésben alkalmazni kell az ELISA tesztet az antiphospholipid antitestek kimutatására (20).
Tudni kell, hogy a különböző tesztek, különböző minőségben és konfigurációban tartalmaznak phospholipideket, spektrumuk igen eltérő lehet.
Az AP-syndroma terápiája
Az APA-ek jelenlétével összefüggő thrombosisok kezelésében a következő alapelveket kell figyelembe vennünk.
A kórkép pathogenetikai és klinikai heterogenitása miatt eleve nem deklarálhatok olyan terápiás elvek, amelyek minden esetben egyformán alkalmazhatóak lennének. A thrombosissal vagy egyéb klinikai tünettel nem is járó, véletlen laboratóriumi vizsgálattal kimutatott APA képezi az egyik végletet; más esetekben súlyos, akár fatalis artériás és vénás thrombosisokkal (tüdőembóliákkal) járó eseteket látunk, amelyekhez az SLE legkülönbözőbb szervi maifesztációi is társulnak. Külön problémát jelent az APA és a terhesség együttese, melyben a thrombosishajlam fokozódásán kívül a korai vetélés veszélyét is figyelembe kell vennünk, és lehetőség szerint azt is el kell hárítanunk.
Kiindulási pontként azt mondhatjuk, hogy ha a fiatalkorban fellépő, vénás vagy artériás thrombosis hátterében nagy valószínűséggel az APA jelenléte kimutatható, de egyéb, systemás immunpathogenesises tünetek nem társulnak hozzá, ugyanúgy be kell állítanunk a tartós orális alvadásgátló kezelést (Syncumar), mint az egyéb thromboembóliák esetében. A klinikai tapasztalat szerint azonban "élesebbre" kell állítanunk az alvadásgátló kezelést, vagyis nem elégedhetünk meg a szokásos INR: 2,0-3,0 közötti értékekkel, hanem lehetőleg 3,0-3,5 közé kell állítsuk azt (11). Artériás thrombosis esetén egy újabb recidiva megelőzésére az orális alvadásgátlás szokásos szintje (INR: 2,0-3,0) mellett kisdózisú acetylszalicil savat is adhatunk egyidejűleg a betegnek (21). Amennyiben az SLE egyéb jelei is fellépnek, az alvadásgátló kezelést immunsuppressiv kezeléssel is ki kell egészítsük (prednisolon, Imuran) (21). Ez utóbbiakra különösen akkor van szükség, ha thrombocytopenia is fellép az immunopathogenesis alapján; ilyenkor természetesen nem adunk a vérzésveszély miatt alvadásgátlót, de ha a beteg anamnézisében már volt thrombosis, a vérlemezkeszám normalizálódásával egyidejűleg célszerű megindítani az óvatos antikoagulálást.
E sémától akkor kell eltérnünk, ha a kumarin kezelés bőrnekrózist idéz elő (22). Ilyenkor a thrombosis megelőzésére a tartós kis molekulatömegű heparin (LMW heparin, Fraxi- parin) szolgál.
Speciális problémát jelent, ha olyan nőbeteg lesz terhes, vagy kíván gyermeket világra hozni, akinek anamnézisében thrombosis, spontán abortusok és APA szerepel. Ilyen esetekben azt is fontos megállapítani, hogy a systemás autoimmun megbetegedés (SLE) egyéb tünetei is jelen vannak-e, mert ez módosítja a kezelési stratégiát. Mivel terhességben, különösen annak első trimesterében az embryopathia miatt nem adhatunk Syncumart, ezért már a tervezett koncepció idején állítsuk át az előzőleg thrombosist szenvedett nőbeteget valamely más alvadásgátlóra. Az egyik lehetőség a kis dózisú aspirin (kb. 80 mg per nap), vagy a kisdózisú s.c. heparin (Calcium-heparin). Ma egyre inkább tért hódít, és magunk is arra hajlunk, hogy a Syncumar kezelés felfüggesztésével Fraxiparinra térünk át. A kis molekulatömegű heparin készítmények az irodalmi adatok többsége szerint nem jutnak át a magzati vérkeringésbe, így magzati vérzéses szövődményektől nem kell tartanunk (23). A különböző kis molekulatömegű heparin készítmények közül többet a gyártók a terhességben biztonsággal alkalmazhatónak deklarálnak (például a Snadoparint), míg a hazánkban elérhető Fraxiparin esetében a jelenlegi alkalmazási előirat a nem kellő tapasztalatra hivatkozva terhességben nem ajánlja, noha ezzel a készítménnyel is bizonyították, hogy nem jut át a magzati vérkeringésbe és külföldön is sokan adják a terheseknek. A calcium-heparin készítmények a terhesség egész időtartama alatt nemcsak a gyakori szúrás miatti kényelmetlenség miatt kerültek háttérbe, hanem azért is, mert a tartós heparin kezelés osteoporosist okoz; ez különösen akkor súlyos probléma, ha az SLE és a velejáró egyéb tünetek miatt pred- nisolont is adnunk kell. Magunk is sikerrel segítettük elő élő, egészséges gyermek születését steroid-Fraxiparin kombinációval olyan fiatal nőbeteg esetében, akinél előzőleg az SLE-s polyarthritis súlyos ízületi deformitást okozott, többszörösen szenvedett mélyvénás thrombosist, és korábban 5 alkalommal lépett fel a terhesség különböző időszakaiban vetélés.
Köszönetnyilvánítás
A közlemény a 017735 nyilvántartási számú OTKA-pályázat támogatásával készült.
Irodalom
- Pető I., Sas G.: Ismétlődő mély vénás trombózis SLE kapcsán. Orv. Hetil., 122: 2665-2666 (1981).
- Gergely P.: Antifoszfolipid szindróma. LAM 3 (2): 104- 108 (1993).
- Ford, S. E., Kennedy, L., Ford, P. M.: Clinicopathological correlations of antiphospholipid antibodies. Arch. Pathol. L. Med., 118: 491-495 (1994).
- Triplett, D. A.: Antiphospholipid antibodies and trombosis - A consequence, coincidence or cause? Arch. Pathol. Lab. Med., 117: 78-82 (1993).
- Feinstein, D. I., Rapprot S. I.: Acquired inhibitors of blood coagulation. Progress in haemostasis and thrombo- sis, 1: 75-95 (1972).
- Vianna, J. L., Khamasíhta, M. A., Ordiros, J., Font, J., Cervara, R. et al.: Comparison of the primary and secondary antiphospholipid syndrome: A European Multi- centre Study of 114 patients. The American Journal of Medicine, 96: 3-9 (1994).
- Brighton, T. A., Chesterman, C. N.: Antiphospholipid antibodies and thrombosis. Bailliere's Clinical Haematology, 541-556 (1994).
- Hift, R. .J., Bírd, A. R., Sarembock, B. D.: Acquired hypoprothrombinaemia and lupus anticoagulant: response to steroid therapy. Br. J. Haematol., 30: 308-310 (1991).
- Orlando, E., Cortelazzo, S., Marchetti, M" Sanfratello, R., Barbui, T.: Prolonged bleeding time in patients with lupus anticoagulant. Throm. Haemost., 68: 495-499 (1992).
- Brick, R. L., Baker, W. F.: Antiphospholipid and thrombosis syndromes. Seminars in thrombosis and hemosta- sis, 20: 3-15 (1994).
- Asherson, R. A., Cervera, R.: Antiphospholipid antibodies and the heart. Circulation, 84: 920-923 (1991).
- Eeader, A.: The antiphospholipid syndrome: a syndrome in evolution. Annals of the rheumatic disorders, 51: 147-150(1992).
- Harris, E. N., Gharavi, A. E., Hedge, U" Derue, G., Morgan S. H. et al: ACAs in autoimmune thrombocytopenic purpura. Br. J. Haematol., 59: 231-234 (1985).
- Brick, R. L., Baker, W. F.: Hematology/oncology clinics of clinics ofNorth America, 6: 1287-1299 (1992).
- Eng, A. M.: Cutaneous expressions of antiphospholipid syndrome. Seminars in thrombosis and hemostasis, 20: 71-78 (1994).
- Levine, S. R., Langer, S. L., Albers, J. W.: Sneddon's syndrome: An antiphospholipid antibody syndrome? Neurology (Cleve.), 38: 798 (1988).
- Mojzes J., Battyani Z., Grexa E.: Sneddon-syndroma, mint az antiphospholipid antitest syndroma klinikai megnyilvánulása. Orv. Hetil., 134: 251-255 (1993).
- Graisman, S. G., Thayaparan, R. S., Godwin, T. A., Locksin, M. D.: Occlusive vasculopathy in systemic lupus erythematousus: association with anticardiolipin antibody. Arch. Intern. Med., 151: 389-392 (1991).
- Exner, T., Tripplet, D. A., Taberner, D., Machin, S. J.: Guidelines for testing and revised criteria for lupus anticoagulants. Thromb. Hemost., 65: 320-322 (1991).
- Harris, E. N.: Serological detection of antiphospholipid antibodies. Stroke (Suppl. I.), 23: 1-4, 1-6. (1992).
- Babikian, V. L., Levine, R. R.: Therapeutic considerations for stroke patients with antiphospholipid antibodies. Stroke (Suppl. I.), 23: 1-33,1-37. (1992).
- Moreb, J., Kitchens, C. S.: Acquired functional protein S deficiency, cerebral venous thrombosis, and coumarin skin necrosis in association with antiphospholipid syndrome: report two cases. The American Journal of Medicine, 87: 207-210 (1989).
- Fejgin M. D" Lourwood D. L.: Low molecular weight heparin and their use in obstetrics and gynecology. Obstet. Gynecol. Surv., 49 (6): 424-431 (1994).
Dr. M. A. Lateiwish
HIETE Haematológiai Tanszék
1113 Budapest, Daróczi út 24.
Érbetegségek: 1995/3. 9-13. oldal