Az V. alvadási faktor Leiden mutációja egy gyakori, öröklött thrombophilia, amely fokozza a vénás thrombo-emboliás betegségek rizikóját. E genetikai elváltozás jelentősége az artériákat érintő betegségekben még pontosan nem ismert. Korábbi vizsgálatok arra utaltak, hogy fiatal, myocardialis infarctusban szenvedő egyénekben a Leiden mutáció gyakrabban fordul elő. Jelen vizsgálatunkban a Leiden mutáció szerepét tanulmányoztuk, elsosorban súlyos, alsó végtagi atherosclerosisban és reconstruction érmutétet követő restenosisban szenvedő betegekben. Százhét beteget tanulmányoztunk, akik korábban femoropoplitealis és iliofemoralis rekonstrukciót követően 5 éven belül restenosis miatt ismételt (redo) műtétre szorultak. A Leiden mutáció frekvenciája a betegcsoportban magasabb volt, mint 253 kontroll véradó egyénben, de a különbség nem bizonyult szignifikánsnak (p=0,l). A 60 év alatti betegekben a Leiden mutáció alléljának szignifikánsan (p=0,016) magasabb frekvenciáját észleltük az előbbi kontrollcsoporthoz viszonyítva. Az allélfrekvencia korfüggő divergenciája felhívja a figyelmet a genetikai tényezők szerepére és a restenosisra hajlamosító tényezők esetleges korfüggóségére is.
Az előadás a MÁÉT pályázatán III. dijat nyert.
Érbetegségek: 1999/3. 95-98. oldal
KULCSSZAVAK
Leiden mutáció, thrombotikus hajlam, restenosis, génfrekvencia
Bevezetés
Az V. alvadási faktor Leiden mutációja egy gyakori, öröklött thrombophilia, mely fokozza a vénás thrombo-emboliás betegségek rizikóját. (I. táblázat.) E genetikai elváltozás jelentősége az artériákat érintő betegségekben még pontosan nem ismert. Előző vizsgálatok arra utaltak, hogy fiatal, myocardialis infarctusban szenvedő egyénekben a Leiden mutáció gyakrabban fordul elő. A femoro-poplitealis atherosclerotikus érbetegség a fejlett államok jelentős morbiditási tényezője. Astenotikus tünetek esetén rekonstrukciós érműtét szükséges, mely adott esetben vénát, vagy heterograftot alkalmaz. Az esetek egy jelentős részében néhány héttől több évig terjedő időszakon belül restenosis alakul ki, amely miatt korrekciós műtétre ("redő műtétre") van szükség. A súlyos atherosclerosis és a restenosis ismert rizikófaktorai részben megegyeznek, és ezek közé soroljuk a nemet, az anamnaesisben szereplő restenosist, diabetest, hyperlipoproteinaemiát, hypertoniát, vesebetegséget, dohányzást, hyperviscositast, csökkent fibrinolytikus aktivitást (1., 2.). Újabban felmerült annak a gyanúja, hogy a genetikai thrombophiliák is jelentős szerepet játszhatnak mind a gravis atherosclerosis, mind a restenosis létrejöttében.
Vizsgálatunkban a Leiden mutáció szerepét tanulmányoztuk, elsósorban súlyos, alsó végtagi atherosclerosisban és rekonstrukciós érműtétet követő restenosisban szenvedő betegeknél.
Betegcsoport
Százhét beteg vizsgálatát végeztük el, akik iliofemoralis és femoropoplitealis érműtétet követő 5 éven belül, restenosis miatt ismételt (redo) műtétre szorultak. A betegek az MH Központi Honvédkórházában random, az elsőérműtétet követően restenosis miatt ismételten operált betegek közül származtak, akiket kórtörténetük alapján választottunk ki, és utólagosan hívtunk vissza vizsgálataink elvégzésére. A betegek a kontrollvizsgálatokba, illetve az általunk végzett genetikai vizsgálatba beleegyezésüket adták. (II. táblázat.)
Öt éven belül restenosis miatt operált 198 beteg közül az utólagos behívás során 107 beteg jelentkezett vizsgálatra. Huszonegy beteg meghalt, hívásunkra hetven nem jelent meg. A betegek közül a nő/férfi arány 70/37 volt, korban 39-78 év közöttiek voltak, átlagéletkor 58 év. Tizenkét órás éhezést követően, fekvő helyzetben vettünk vénás vért rutin laboratóriumi vizsgálatokra, a lipoprotein anyagcsere paramétereinek meghatározására, a szérum húgysav mérésére, valamint a DNS preparálásra alkalmas, EDTA-val alvadás- gátolt vérmintát. Standard kérdőívet fektettünk fel a betegek anamnesisére, vénás thromboembóliás szövődményekre vonatkozóan. Az összes betegünk dohányos volt betegsége idején. Kontroll csoportként 253 önkéntes véradó vérmintáinak laboratóriumi adatait alkalmaztuk.
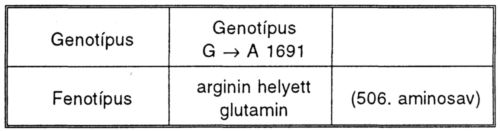
I. táblázat.
V. alvadási faktor Leiden-mutációja.
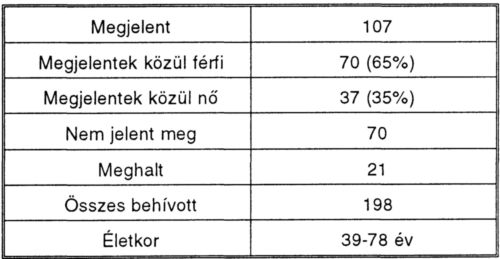
II. táblázat.
Beteganyag 1990. 01. 01. - 1995. 12. 31. között.
Módszerek
A vérmintákat szilikonozott üvegcsövekbe (vacutainer, Beckton Dickinson) vettük, melyek 0,129 M EDTA-t tartalmaztak. A szérum teljes cholesterin, triglycerid, HDL-cholesterin szintet a kereskedelmi forgalomban kapható Boehringer Mannheim GmbH kittekkel határoztuk meg. Az apolipoprotein AL AH és B koncentrációkat immunefelometriás módszerrel mértük (Boehringer Mannheim GmbH). Az V. faktor Leiden mutációját PCR technikai alkalmazásával detektáltuk (3) (1. ábra).A DNS standard módszerrel történő preparálását követően 50 µl mennyiségben 500 ng DNS- t, Taq polimeráz puffert (Perkin Elmer), 200Jµ dNTP-t, 10 pmol prímért (PR-6967 és PR-990), 1,5 mmol MgCl2-t, 2% DFMSO-t és 1,25 U AmplitaQ-ot (Perkin Elmer) tartalmazó eleggyel végeztük el a PCR reakciót. Öt perces, 95 °C-osdenaturációt követően, 36 ciklust végeztünk el 95 °C-on 30 másodpercig, illetve 55 °C-on 45 másodpercig és 72 °C-on 45 másodpercig Perkin Elmer 2400-as készülékben. A végső kiterjesztést 10 percen keresztül 72 °C-on végeztük e-1. Tíz µl PCR terméket 1,0 U MnlI enzimmel emésztettünk 37 °C-on egy éjszakán keresztül. A fragmenteket 6%-os polyacrylamid gélen futtattuk, és ethidium bromiddal festettük meg.
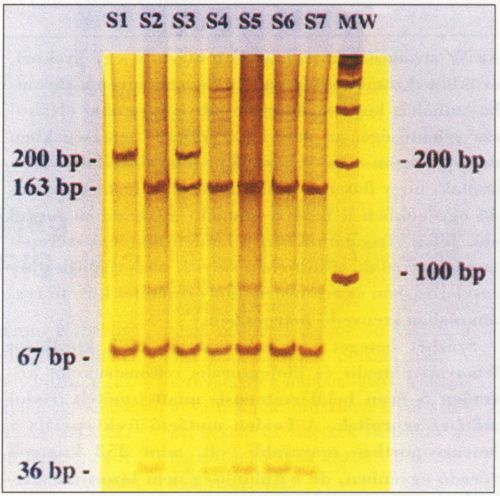
1. ábra.
A V. faktor Leiden mutációját PCR technika alkalmazásával detektáltuk.
Eredmények
A betegcsoportban szignifikánsan emelkedett szérum cholesterin, triglycerid és apolipoprotein B szintet észleltünk a kontrollcsoporthoz viszonyítva. A betegcsoportban magasabb arányban észleltünk Leiden mutációt (14/213, 7,0%), a kontrollcsoporthoz viszonyítva (20/506, 3,95%). A különbség nem bizonyult szignifikánsnak (p = 0,117, OR = 1,819, Cl 95% = 0,9-3,67). A férfiak és nők között az eloszlásban különbséget nem észleltünk. Amennyiben életkor szerint osztottuk fel a beteg, illetve kontrollcsoportban a Leiden mutáció gyakorisága közel kétszerese volt a 60 év feletti csoportnak, illetve a kontrollcsoportban észlelt frekvenciának (III. táblázat). Ezzel szemben a 60 év feletti csoportban a Leiden mutáció gyakorisága közel megegyezett a kontrollcsoportéval.
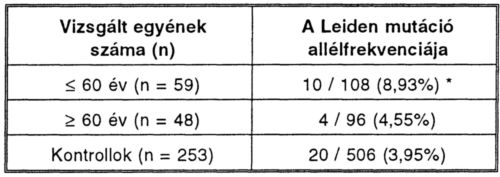
III. táblázat.
A Leiden mutáció gyakorisága a kontrollcsoporthoz viszonyítva.
* p 0,047, OR 2,382 (Cl 95% = 1,083 - 5,243)
Megbeszélés
Vizsgálatunkban a lipoprotein anyagcsere adataiban szignifikáns különbséget észleltünk a betegcsoport és a kontroll egyének csoportja között. A Leiden mutáció a teljes betegcsoportban nem különbözött szignifikánsan, de a 60 év alatti csoportot figyelembe véve a Leiden mutáció szignifikánsan gyakrabban fordult elő. A kontrollcsoportunk átlagéletkora még a 60 év alatti betegcsoport átlagos életkoránál is fiatalabbnak bizonyult (42, illetve 53 év). A Leiden faktor és az életkor közötti összefüggést az eddigi vizsgálatok különböző populációkban nem igazolták. Ezek alapján megállapítható, hogy a 60 évnél fiatalabb korosztály súlyos femoropoplitealis atherosclerosisában, mely restenosis veszélyével is jár, a Leiden faktor, mint thrombophilia, jelentőséggel bír. Sajnos azt a tényt, hogy a Leiden faktor elsősorban a restenosis rizikótényezője lenne, csak abban az esetben lehetne igazolni, ha érrekonstrukciós műtéten egy alkalommal átesett restenotikus jeleket nem mutató csoport allélfrekvenciáját vizsgálnánk. Azonban ilyen betegcsoport felmérése évtizedekbe telne, hiszen ezek a betegek intenzív antilipidaemiás, antiaggregációs kezelésnek vannak kitéve, vagy egyszerűen - betegség tüneteinek hiányában - nem vesznek részt rendszeres orvosi gondozásban.
Ridker és munkatársai a vénás thromboemboliás betegségekben a Leiden mutáció fokozott gyakoriságát észlelték (4), de myocardialis infarctuson átesett egyének esetében ezt igazolni nem tudták. Fiatal, erősen dohányos, infarctust szenvedett nőkben azonban mások igazolták a mutáció szignifikánsan nagyobb gyakoriságát (5). Eritsland és munkatársai vizsgálatukban az aktivált protein C rezisztencia (melyek az esetek jelentós részében a Leiden mutációnak felelnek meg) gyakoriságát nem találták szignifikánsan emelkedettnek koszorúsér betegekben (6). Ourel és munkatársai az aktivált protein C rezisztencia előfordulását gyakoribbnak találták infrainguinalis bypass műtétet követő ismételt műtétek során (7). Érdekes módon ezek a betegek az ő vizsgálatukban inkább az idősebbek közül kerültek ki.
Az eddigi populációs vizsgálatok alapján a Leiden mutáció nem tekinthető az atherosclerosis független rizikófaktorának. Azonban mint egy prothrombotikus tényező, fokozza érrekonstrukciós műtéteket követően a restenosis valószínűségét, feltehetően az aktivált X-es faktor és a thrombin fokozott termelődése útján (8). A fokozott fibrin depozíció, a megnövekedett thrombocyta aggregációs képesség, a fokozott celluláris proliferációs hajlam az atherothrombotikus jelenségeket elősegítő tényezőknek minősíthető. A postoperatív szakban a Leiden faktor által kiváltott fokozott thrombusképződés lehet az a centrális motívum, mely az artériafal pathológiás elváltozásait befolyásolhatja. E prothrombotikus tényezőre való szűrés, majd az azt követő anticoagulációs kezelés az infrainguinalis bypass graftok hosszabb nyi vamaradásához járulhat hozzá.
Irodalom
- Isner, J. M.:Mechanisms of restenosisafterlowerextremity angioplasty. J. Vasc. Surg., 1995. 22: 114-115.
- Faxon, D. P.: identifying the predictors of restenosis. Do we need new glasses? Circulation, 1997; 95: 2244-2246.
- Bertina, R. M., Koeleman, P. C., Koster, T., Rosendaal, F. R., Din 7 en, R. ./., Ronde, H., van der Veld en, P. A. and Re- itsmay P. H.: Mutation in blood coagulation factor V associated with resistance to activated protein C. Nature 1994; 369: 64-57.
- Ridker, P. M., Hennekens, C. H., Lindpaintner, K., Stampfer, M. J., Eisenberg, P. R., Miletich, J. P.: Mutation in the gene coding for coagulation factor V. and the risk of myocardial infarction, stroke, and venous thrombosis in apparently healthy men. N. Engl. J. Med. 1995; 332: 92-97.
- Rosendaal, F. R., Siscovick, D. S., Schwartz, S. M., Beverly, R. K., Psaty, B. M., Longstreth, W. T. Jr., Raghimathan, T. E., Koepsell, T. D., Reitsma, P. H.: Factor V. Leiden (resistance to activated protein C) increases the risk of myocardial infarction in young women. Blood 1997; 89: 2817-21
- Eritsland, J., Gjonnes, Sandset, P. M., Seljefot, I., Amesen, H.: Activated protein C resistance and graft occlusion after coronary bypass surgery. Thromb. Res. 1995; 7: 223-226.
- Ourel, K., Green, R. M., DeWeese, J. A., Cimino, C.: Activated protein C. resistance: Prevalence and implications in peripheral vascular disease. J. Vase. Surg. 1996; 23: 46-52.
- Bachhuber, B. G., Sarembock, L J., Mcnamara, C. J. et a I: Thrombin induced proliferation of cultured vascular smooth muscle cells requires prolonged exposure to thrombin. Circulation 1993; 88 (Suppl L): 468 (A).
Dr. Vallus Gábor
MH Központi Honvéd Kórház
Érsebészeti Osztály
1134 Budapest, Róbert Károly krt. 44.
Érbetegségek: 1999/3. 95-98. oldal